Факторы врожденного иммунитета клеточные гуморальные
На сегодняшний день выявлен широкий перечень видов иммунных систем человека, среди которых необходимо выделить клеточный и гуморальный. Взаимодействие обоих видов обеспечивает распознавание и уничтожение инородных микроорганизмов. Подробнее рассмотреть особенности, принципы действия внеклеточной системы защиты поможет представленная публикация.
Что такое гуморальный иммунитет?
Гуморальный иммунитет — это защищенность человеческого организма от регулярного попадания во внутреннюю среду чужеродных возбудителей инфекций и заболеваний. Защита осуществляется посредством растворимых во внутренних жидкостях, крови человека белков — антигенов (лизоцим, интерферон, реактивный белок).
Принцип действия заключается в регулярном формировании веществ, способствующих предотвращению и распространению вирусов, бактерий, микробов вне зависимости от того какого рода микроорганизм попал во внутреннюю среду опасный или безвредный.
Гуморальное звено иммунитета включает в себя:
- Сыворотка крови — в состав входит С — реактивный белок, деятельность которого направлена на ликвидацию патогенных микробов;
- Секреты желез, препятствующие развитию инородных тел;
- Лизоцим — стимулирует растворение клеточных стенок бактерий;
- Муцин — вещество направлено на защиту оболочки клеточного элемента;
- Пропердин — отвечает за свертываемость крови;
- Цитокины — соединение белков, выделяемых тканевыми клетками;
- Интерфероны — выполняют сигнальные функции, оповещающие о появлении чужеродных элементов во внутренней среде;
- Комплементая система — общая численность белков, содействующая обезвреживанию микробов. В систему входят двадцать белков.

Механизмы
Механизм гуморального иммунитета представляет собой процесс, в течение которого формируется защитная реакция, направленная на предотвращение проникновения в организм человека вирусных микроорганизмов. От того каким образом протекает процесс защиты зависит состояние здоровья и жизнедеятельности человека.
Процесс защиты организма заключается в следующих этапах:
- Происходит формирование В — лимфоцита, который образуется в костном мозге, где созревает лимфоидная ткань;
- Далее осуществляется процесс воздействия антигена на плазматические клетки и клетки памяти;
- Антитела внеклеточного иммунитета распознают инородные частицы;
- Формируются антитела приобретенной иммунной защиты.

Механизмы иммунной системы делятся на:
Специфические — действие которых направлено на уничтожение конкретного возбудителя инфекции;
Неспецифические — отличаются универсальным характером направленности. Механизмы распознают и борются с любыми инородными антителами.
Специфические факторы
Специфические факторы гуморального иммунитета вырабатываются В — лимфоцитами, которые формируются в костном мозге, селезенке, лимфоузлах в течение двух недель. Представленные антигены реагируют на появление инородных частиц в жидкостях организма. К специфическим факторам относят антитела и иммуноглобулины (Ig E, Ig A, Ig М, Ig D). Действие лимфоцитов в человеческом организме направлено на блокировку чужеродных частиц, после этого процесса в действие вступают фагоциты, которые ликвидируют вирусные элементы.
Этапы формирования антител:
- Скрытая фаза (индуктивная) — в течение первых дней элементы вырабатываются в небольшом количестве;
- Продуктивная фаза — образование частиц происходит в течение двух недель.
Неспецифические факторы
Перечень неспецифических факторов гуморального иммунитета представлен следующими веществами:
- Элементы тканевых клеток;
- Сыворотка крови и содержащиеся в ней белковые элементы, стимулирующие противодействие клеток возбудителям;
- Секретами внутренних желез — содействуют уменьшению численности бактерий;
- Лизоцим — вещество, обладающее противобактериальным эффектом.
Показатели гуморального иммунитета
Действие гуморального иммунитета осуществляется путем выработки необходимых для защиты организма элементов. От количества полученных антител и правильности их функционирования зависит общее состояние и жизнеспособность человеческого организма.
При необходимости определить показатели внеклеточной иммунной системы требуется провести комплексный анализ крови, по результатам которого определяется общее количество формируемых частиц и возможные нарушения действия иммунной системы.
Клеточный и гуморальный иммунитет
Благоприятное функционирование внеклеточного иммунитета обеспечивается только посредством взаимодействия с клеточной защитой. Функции иммунных систем отличаются, но имеются схожие характеристики. Они оказывают эффективное воздействие на внутреннюю систему организма человека.
Отличие гуморального иммунитета от клеточного заключается в их объекте воздействия. Клеточный функционирует непосредственно в клетках организма, предотвращая размножение инородных микроорганизмов, а гуморальный оказывает влияние на вирусы и бактерии во внеклеточном пространстве. Одна система иммунной защиты без другой не может существовать.
Большое значение в жизни каждого человека играет жизнеспособность его внутренней среды. Укрепление иммунной защиты и поможет обезопасить человеческих организм от болезнетворных бактерий и вирусов.
 Автор материала — Самолетова Даная Яковлевна, эндокринолог и терапевт, кандидат медицинских наук. Имеет более 10 лет опыта работы с пациентами. Узнайте здесь, как попасть к ней на прием (город Уфа, РФ) или получить консультацию через Интернет. Не принимайте сильнодействующие лекарства по своей инициативе. Это опасно! Не пытайтесь заменить лечение, назначенное врачом, приемом БАДов.
Автор материала — Самолетова Даная Яковлевна, эндокринолог и терапевт, кандидат медицинских наук. Имеет более 10 лет опыта работы с пациентами. Узнайте здесь, как попасть к ней на прием (город Уфа, РФ) или получить консультацию через Интернет. Не принимайте сильнодействующие лекарства по своей инициативе. Это опасно! Не пытайтесь заменить лечение, назначенное врачом, приемом БАДов.
Источник
В
естественном иммунитете против
микроорганизмов активно участвуют
белки острой (ранней) фазы воспаления:
С-реактивный
белок (СРБ),
фибронектин,
сывороточный
амилоид,
альфа2-макроглобулин,
фибриноген,
фермент
лизоцим и
др.
Одной
из важнейших систем, обеспечивающих
естественный иммунитет, является система
комплемента.
Система комплемента
Комплементом
называют сложную систему ферментативных
и рецепторных белков (более 30) сыворотки
крови.
Основные
13 компонентов системы комплемента
обозначаются буквой C с соответствующим
номером (C1, С2, С3 и т.д.) Они образуются в
печени и секретируются макрофагами.
Активация системы комплемента протекает
классическим,
очень сходным с ним лектиновым,
а также альтернативным
путями.
Процесс имеет вид цепной
реакции,
управляемой регуляторными белками. При
этом каждый предыдущий компонент каскада
активирует несколько последующих за
счет их ферментативного расщепления.
При
распаде компонентов комплемента обычно
образуется 2 фрагмента. Больший фрагмент
обозначается малой латинской буквой
«b»
и является активным, продолжая каскад
расщепления. Меньшие фрагменты в
дальнейшей активации комплемента обычно
не участвуют, однако проявляются
многообразными биологическими функциями.
Они обозначаются малой латинской буквой
«а». Единственное исключение из этого
правила – фактор С2. Комплексы
активированных компонентов обозначаются
сверху чертой.
Белки
альтернативного пути активации получили
название факторов и обозначаются
большими латинскими буквами (В, Н, I
и т.д.)
Среди
регуляторных белков различают естественный
ингибитор компонента комплемента С1
(С1-ингибитор),
который тормозит спонтанную активацию
C1q компонента. При его дефиците возникает
наследственный
ангионевротический отек.
Кроме этого существует фактор
DAF,
ускоряющий деградацию С3b
компонента комплемента на мембранах
собственных клеток организма, предотвращая
их лизис.
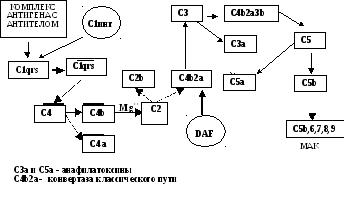
Классический
путь активации
запускается комплексом
антиген-антитело
в присутствии катионов Ca и Mg обычно на
поверхности клетки-мишени (см. рис. 1.1.)
Эффективными активаторами данного пути
являются АТ классов IgG
и IgM.
Комплекс «антиген-антитело» связывается
с компонентом С1q, который присоединяет
С1rs, а затем активирует и расщепляет С4
на С4а и С4b (рис.11). С4b присоединяется
либо к С1, либо к поверхности клетки-мишени.
Далее к нему присоединяется С2. Он, в
свою очередь, расщепляется на С2а и С2b
предыдущим компонентом. С2а остается
связанным с С4b. Этот комплекс получил
название конвертазы
классического пути
активации комплемента. Она расщепляет
С3 компонент на С3а и С3b. С3b присоединяется
к конвертазе классического пути,
образуется конвертаза С5 компонента, и
этот макромолекулярный комплекс
активирует компонент С5. Он распадается
на С5а и С5b. К С5b на мембране клетки-мишени
последовательно присоединяются С6, С7,
С8. Этот комплекс встраивается в мембрану
клетки-мишени и к нему может присоединиться
до 20 молекул С9 компонента.


Са++
Mg++

Рис.
1.1. Классический путь активации
комплемента
Комплекс
С5b-C9
получил название мембраноатакующего
комплекса
(МАК).
В механизме его литического действия
много общего с цитотоксическим белком
перфорином.
МАК встраивается в мембрану клетки-мишени
за счет гидрофобных взаимодействий,
образуя трансмембранный канал. Через
него в клетку поступают ионы натрия и
вода, а выходят ионы калия, что приводит
к цитолизу.
Для
того чтобы МАК не разрушал собственные
клетки организма, его образование может
быть блокировано растворимыми
сывороточными факторами (S-фактор
– белок витронектин).
Кроме того, имеющийся на мембранах
клеток рецептор CD59
препятствует присоединению к МАК
компонента С9.
Лектиновый
путь активации комплемента отличается
только природой иммунного комплекса,
запускающего начальный этап активации.
Со стороны иммунной системы здесь
участвуют белки-лектины,
связывающие
полисахаридные компоненты бактерий
(например, маннансвязывающий
лектин,
С-реактивный
белок и т.д.)
Активация происходит через компонент
С1, и ее ход не отличается от классического
пути.
Альтернативный
путь активациикомплемента
(рис. 1.2) является неспецифическим.
Центральным
звеном альтернативного пути является
С3b компонент.
Следовые его количества постоянно
присутствуют в сыворотке вследствие
спонтанного гидролиза С3. Этот процесс
запускается и усиливается липополисахаридами
клеточной стенки бактерий
(эндотоксинами), агрегированными
иммуноглобулинами, лекарственными
препаратами и т.д. Образующийся при этом
С3b-компонент в присутствии ионов магния
связывается с фактором В сыворотки
(неактивная сериновая протеаза). На
комплекс С3bB действует фактор D – активная
сывороточная протеаза. Она расщепляет
фактор В на Ва и Вb. Образующийся комплекс
С3bBb представляет собой конвертазу
альтернативного пути
активации. В норме она неустойчива, но
стабилизируется белком пропердином
(белок P). Конвертаза альтернативного
пути присоединяет еще одну молекулу
С3b, образуется конвертаза
С5 компонента
С3bBbС3b, которая активирует С5. Дальнейшая
активация комплемента не отличается
от классического пути. Таким образом,
С3-компонент является ведущим в активации
комплемента по обоим путям, определяя
процессы цитолиза.
В
процессе активации комплемента образуются
биологически активные фрагменты. Так,
компоненты С3а, С4а и С5а служат
анафилатоксинами,
действуя на макрофаги, гранулоциты,
тучные клетки. Они вызывают выделение
из них медиаторов, дегрануляцию тучных
клеток. Возникающий патологический
процесс клинически проявляется
аллергическими (шок и др.), псевдоаллергическими
реакциями, воспалением и повреждением
тканей.
При
заболеваниях, сопровождающихся
образованием иммунных комплексов
(аутоиммунные болезни, инфекции), уровень
белков комплемента снижается –
гипокомплементемия. Уровень комплемента
наиболее высок у морских свинок, поэтому
их сыворотка крови используется как
«комплемент» в серологических
реакциях.
Компоненты
активированного комплемента связываются
с рецепторами комплемента, имеющимися
на лейкоцитах. Основной рецептор CR1
(CD35) связывает C3b, кроме того, рецепторами
к компонентам комплемента являются
лейкоцитарные интегрины. Взаимодействуя
с этими рецепторами клеток продукты
активации комплемента стимулируют
функции лейкоцитов, запускают воспаление;
усиливают противомикробный иммунитет.
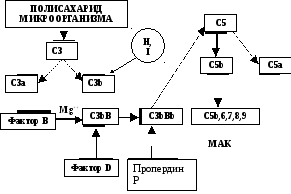

Рис. 1.2.
Альтернативный путь активации комплемента
Функции системы
комплемента
Лизис
клеток-мишеней
(бактериальных, зараженных вирусом,
опухолевых и др.)Опсонизация,
т.е. усиление фагоцитоза через рецепторы
комплемента.Растворение
иммунных комплексов,
что препятствует их отложению в тканях.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Неспецифическая устойчивость организмов к инфекционным агентам передается по наследству. Процесс не требует подготовительной реакции и является первым барьером для микробов. Особое внимание ученые уделяют гуморальным факторам врожденного иммунитета, включая систему комплемента, пептиды, интерфероны.

Основные понятия
Врожденный неспецифический иммунитет сформировался на первых этапах эволюции живого организма. Ученые иммунологии придерживаются мнения, что защитная функция формировалась с зарождением паразитов. У них присутствовали зачатки клеточных и гуморальных защитных факторов. С эволюцией развивалась и совершенствовалась система неспецифического иммунитета (СНИ).
К ее первым компонентам могут относиться:
- барьерная защита кожного покрова;
- специфическое строение слизистых.
Микроорганизму проблематично проникнуть в макроорганизм из-за высокого защитного действия ресниц, влияния бактерицидных секреции. После прохождения выделенных элементов микробы встречаются с защитными клетками. Свойства врожденного иммунитета:
- распознавание антигена;
- прямой контакт с возбудителем с последующим ответом;
- отсутствие иммунной памяти;
- купирование действий любых возбудителей.
Принципы классификации
Кроме врожденного, медики различают искусственный и естественный приобретенный иммунитеты. Первое определение используется в период формирования невосприимчивости клеток организма к конкретному агенту за счет ввода вакцины. Естественный иммунитет можно приобрести после невосприятия инфекции в случае повторного заражения.

С учетом компонента, который играет главную роль в формировании защиты от антигена, для активного иммунитета характерно:
- гуморальная среда;
- клеточная функция.
В зависимости от природы инородного тела, можно перечислить следующие виды защиты: антибактериальная, противогрибковая, противоопухолевая. Если иммунитет поддерживается и сохраняется в отсутствии чужеродного тела, тогда он может являться стерильным. При наличии возбудителя в организме иммунитет считается нестерильным.
Определение системного механизма защиты используется в случае, когда в опасности находится весь организм. При местной защите происходит выраженная резистентность определенных тканей, органов. Основная характеристика местного и системного иммунитетов — возможность быстро переходить друг в друга.
Линии защиты
При рассмотрении траектории перемещения патогенных клеток в динамике инфекционного процесса необходимо учесть, что на пути выстраивается несколько линий защиты. Предварительно возбудитель распознает покровный эпителий. На следующем этапе встречаются слизистые оболочки, для которых характерна колонизационная резистентность.

При наличии инвазивных факторов возбудитель проникает в субэпителиальную ткань. Развивается воспаление, воспаляются регионарные лимфатические узлы. По соответствующим сосудам возбудитель может передаваться другим клеткам через соединительную ткань.
После преодоления барьера инородное тело проникает в кровь, провоцируя системное воспаление. Если оно не гибнет, развивается генерализованная видовая инфекция.
Кратко к факторам врожденного иммунитета относят:
- кожу со слизистыми оболочками;
- клеточные элементы: макрофаги, нейтрофилы, эозинофилы;
- гуморальные адаптивные: рецепторы, которые растворяются на поверхности, интерфероны, пептиды.
Интерфероны являются биологически активными компонентами, которые обеспечивают взаимодействие между клетками. Классификация, характерная для интерферонов: комплект альфа и бета (1 класс), гамма (2 класс), омега (3 класс). Представители первого класса выполняют одинаковые функции:
- синтез клетками, которые поражены вирусом;
- влияние на окружающие ткани при выделении в межклеточное пространство (формирование гипериммунитета).

Активация интерферонов начинается с синтеза 2-х ферментов. Они оказывают прямое влияние на метаболизм. В процессе разрушаются вирусные нуклеиновые кислоты. На фоне воздействия элементов 1-го класса углубляется синтез белка. Интерфероны одновременно выполняют биологическую роль, воздействуя на клетки, которые еще не инфицированы.
Под влиянием веществ первого класса клетки, окружающие возбудитель, приобретают временную устойчивость к инфицированию. Подобный эффект называется неспецифическим. Таким способом появляется резистентность к вирусу. В физиологии продукция интерферона осуществляется во время размножения вируса.
Максимальная концентрация вещества наблюдается в области размножения возбудителя. Факторы, от которых зависит уровень сыворотки:
- связка интерферонов в месте образования;
- диффузия в крови.
Подобные факторы отличаются у пациентов, поэтому сывороточные уровни могут не отражать действительную картину инфицирования. Одновременное влияние интерферонов на организм не относится к физиологическим процессам.
Продолжительность воздействия носит ограниченный характер, так как на фоне длительного влияния нарушаются многие функции интерферонов. Происходит массовая гибель клеток, рецепторов.

Представители 2-го класса формируют специфический приобретенный иммунитет. Он влияет на макрофаги, способствуя активации процесса уничтожения микробов. За счет цитокина завершается фагоцитоз (захват клетками твердых веществ). Третий класс включает в себя вещества, схожие на тканевые ферменты.
На фоне их воздействия уничтожаются микробы. В процессе эволюции патогенные микробы приобрели устойчивость по отношению к защитным функциям. В современной диагностике белки острой фазы применяются в качестве маркеров острого воспаления, что позволяет назначить адекватную терапию.
Источник
1. ВРОЖДЕННЫЙ ИММУНИТЕТ
2 курс, лечебный факультет
2. План лекции
ЦЕЛЬ: научить студентов пониманию
особенностей строения и функционирования
врожденного иммунитета.
Понятие о врожденном иммунитете и его
особенностях и функциях
Клеточные и гуморальные факторы врожденного
иммунитета
Характеристика клеток, участвующих в реакциях
врожденного иммунитета
Рецепторы врожденного иммунитета
3.
CD – антигенные маркеры клеток иммунной
системы
МНС- главный комплекс гистосовместимости
Адгезия — прикрепление к объекту фагоцитоза
РАМР (pathogen-associated molecular patternsпатоген-ассоциированные молекулярные
образцы) – консервативные патогенные
структуры микроорганизмов, общие для разных
патогенов.
Хемокины – регуляторы хемотаксиса
различных клеток
Хемотаксис – направленное движение клеток,
определяемое градиентом химических
факторов (хемоаттрактантов)
4. ВИДЫ ИММУНИТЕТА
Врожденный иммунитет – наследственно
закрепленная система защиты многоклеточных
организмов от патогенных и непатогенных
микроорганизмов, а также эндогенных продуктов
тканевой деструкции.
Приобретенный (адаптивный) иммунитет формируется в течение жизни под влиянием
антигенной стимуляции.
Врожденный и приобретенный иммунитет
– это две взаимодействующие части
иммунной системы, обеспечивающие
развитие иммунного ответа на
генетически чужеродные субстанции.
5. Особенности врожденного иммунитета
распознавание и элиминация патогенов в
первые минуты или часы после их
проникновения в организм
отсутствие клональности — не образуют клонов,
каждая клетка действует индивидуально
распознавание патогенов через рецепторы,
экспрессированные на клетках (рецепторы «мусорщики», маннозные, лектиновые,
комплемента, Toll-подобные и др.)
Рецепторы системы врожденного иммунитета
эволюционно законсервированы
6. ОСОБЕННОСТИ ВРОЖДЕННОГО ИММУНИТЕТА
факторы врожденного иммунитета не
изменяются в процессе жизни,
контролируются генами зародышевой
линии и наследуются
активация врожденного иммунитета не
формирует иммунологической памяти, но
является обязательным условием
развития адаптивного иммунного ответа
7. ОБЩИЕ ПОЛОЖЕНИЯ О ВРОЖДЕННОМ ИММУНИТЕТЕ
8. ФУНКЦИИ ВРОЖДЕННОГО ИММУНИТЕТА
9. механизмы ВРОЖДЕННОГО ИММУНИТЕТА
КЛЕТОЧНЫЕ :
Клетки врожденного иммунитета: мон/мф,
дендритные клетки, NK, NKТ -клетки, НФ, ЭФ,
БФ, тучные клетки, В1-клетки
Неиммунные клетки: эпителий слизистых
оболочек, эндотелий, клетки зпидермиса,
фибробласты и др.
ГУМОРАЛЬНЫЕ: белки острой фазы,
провоспалительные цитокины и хемокины,
комплемент и др.
10.
11. ФАГОЦИТАРНАЯ СИСТЕМА
Представлена происходящими из
миелоидной стволовой клетки
«профессиональными фагоцитами»:
циркулирующими в крови (моноцитами и
нейтрофилами)
тканевыми фагоцитами (МФ и ДК)
Функции:
— участие в реакциях врожденного
иммунитета (фагоцитоз)
— регуляция адаптивного иммунитета (АГпредставляющая функция, активация Т-лф)
12. Этапы развития макрофагов
13. ХАРАКТЕРИСТИКА МОН/МФ
компактное ядро округлой формы
размеры — 10-18 мкм
содержат
ряд ферментов
(кислая
гидролаза, пероксидаза, неспецифическая
эстераза и др)
моноциты составляют 5-10% лейкоцитов
периферической крови
циркулируют в крови около суток, затем
мигрируют в ткани, превращаясь с
тканевые макрофаги
14. ТКАНЕВЫЕ МАКРОФАГИ
Печень: Купферовские клетки (мф синусов)
Легкие: альвеолярные макрофаги
(подвижные)
Селезенка: макрофаги селезенки (свободные,
подвижные и фиксированные)
Лимфоузлы: макрофаги лимфоузлов
Костная ткань: остеокласты
Нервная ткань: микроглия
Соединительная ткань: гистиоциты
Серозные полости: подвижные макрофаги
плеврального и перитонеального экссудата
15.
16. Основные рецепторы и маркеры мон/мф
1. Рецепторы для:
— Fc-фрагментов иммуноглобулинов
— компонентов комплемента (С3, С4)
2. Тoll-рецепторы (взаимодействуют с
соответствующими рецепторами бактериальной стенки)
3. Рецепторы – «мусорщики» (связывают компоненты
поврежденных и стареющих клеток)
4. Молекулы адгезии
5. Рецепторы, осуществляющие взаимодействие с
лимфоцитарным иммунитетом:
— рецепторы для цитокинов
— CD40, B7, MHC I – II – мембранные молекулы для
контактов с комплементарными мембранными
молекулами лимфоцитов
17. Паттернраспознающие рецепторы (PAMPs)- консервативные структуры микробов общие для разных патогенов, распознаваемые с помощью паттернраспо
Паттернраспознающие рецепторы (PAMPs)- консервативные
структуры микробов общие для разных патогенов,
распознаваемые с помощью паттернраспознающих рецепторов
(PRRs)
Мембранные:
-Толл-подобные рецепторы (TLR) – распознают ПАМП (образцы
патогенности)
-С-лектиновые рецепторы – углеводы
-Рецепторы «мусорщики» — распознают ЛПС, липотейхолиевую кислоту,
апоптотические клетки
-Интегрины – распознают рецепторы из суперсемейства
иммуноглобулинов, белки межклеточного матрикса
Внутриклеточные: NOD-подобные (нуклеотид-связывающийся
олигополимеризующийся домен)
и др. – локализуются внутриклеточно,
распознают вещества, образующиеся при повреждении клеток
Эти рецепторы эволюционно законсервированны, распознают PAMPs,
включающие различные компоненты бактериальной стенки – ЛПС,
пептидогликан, липотейхоевые кислоты, флагеллин, бактериальную ДНК,
вирусные РНК, глюканы и др.
18. Функции активированных фагоцитов
хемотаксис
Фагоцитоз
Роль клеток — «мусорщиков», разрушающих и
элиминирующих поврежденные, дефектные, старые
клетки организма
Секреция биологически активных веществ
(компоненты комплемента, метаболиты арахидоновой
кислоты, ферменты, цитокины, ПМП, гормоны и др.)
Процессинг и представление антигена (ДК, МФ)
Бактерицидность (кислородзависимая и
кислороднезависимая)
Участие в процессах регенерации и инволюции тканей
Цитотоксичность по отношению к опухолевым клеткам
19. ЭТАПЫ ФАГОЦИТОЗА
Активация фагоцита (распознавание
хемотаксических сигналов)
Хемотаксис — направленная миграция в сторону
увеличения хемотаксических факторов
(эндогенных — С5а, лейкотриен В4, ИЛ-1,
иммунные комплексы; экзогенных – ЛПС,
мурамилдипептид, денатурированные белки);
Адгезия (прикрепление к объекту фагоцитоза)
Эндоцитоз (поглощение объекта)
Процессинг (переработка) объекта фагоцитоза и
выведение продуктов распада из клетки
20. Опсонины
Процесс фагоцитоза усиливают
опсонины – белки,
обволакивающие микробы,
корпускулярные антигены и
усиливающие их фагоцитоз.
Роль опсонинов выполняют
иммуноглобулины (IgG1, IgG3, IgA),
белки острой фазы, фибронектин,
компоненты комплемента (C3b,
C4b)
21. Адгезия (типы молекул адгезии)
Селектины – инициируют взаимодействие
лейкоцит-эндотелий (экспрессируются на
эндотелии)
Интегрины – связываются с молекулой
клеточной адгезии (эксперессируются на
Мон/мф, НФ, ДК, NK, Т-лимф.)
Суперсемья иммуноглобулинов –
лиганды для интегринов
(экспрессируются на активированных
МФ, ДК, эндотелии сосудов)
22. Нейтрофилы — 60-70% лейкоцитов крови, циркулируют в крови 8-10 часов
Этапы адгезии НФ:
роллинг (перекатывание – с участием селектинов)
адгезия – образование прочных связей между НФ и эндотелием
трансэндотелиальная миграция в ткани за счет хемокинов
23. Механизмы бактерицидности фагоцитов
Кислородзависимые – связанные с
усилением окисления глюкозы и
образованием перекиси, гидроксильных
радикалов, супероксидных анионов,
оксида азота
Кислороднезависимые – связанные со
снижением рН (до 4,0), синтезом
лизоцима, протеолитических ферментов,
липаз, катионных белков, лактоферрина
24. Дендритные клетки (две линии развития из ГСК)
25. Виды дендритных клеток
Миелоидные ДК
локализация: дерма (клетки Лангерганса), эпителий
слизистых, интерстиций паренхиматозных
органов
Функции: «неиммунный надзор» в нелимфоидных
органах и тканях (захват и процессинг АГс
молекулой МНС→миграция в региональные
лимфоузлы→представление АГ наивным Тлимфоцитам)
Плазмоцитоидные (лимфоидные) ДК
локализация: Т-зоны периферических органов
иммунной системы, кровь, лимфатические узлы,
селезенка
Функции: в тимусе участвуют в негативной
селекции Т-лимфоцитов (элиминации Тлимфоцитов, реагирующих на собственные АГ)
26. Лимфоидные дендритные клетки (ДК) — антигенпредставляющие клетки, активирующие наивные Т-лимфоциты
Лимфоидные дендритные клетки (ДК) антигенпредставляющие клетки,
активирующие наивные Т-лимфоциты
Функции:
— поглощение АГ путем фагоцитоза,
—
—
пиноцитоза, через FcR
процессинг АГ (переработка АГ до пептидов,
формирование комплекса с молекулой МHС 2
класса, эксперссия на ЦПМ клетки)
переход из незрелых в зрелые ДК
миграция в дренирующие лимфоузлы
представление АГ Т-лимфоцитам
27. NK- клетки (Natural killer)
большие гранулярные лимфоциты, составляют 10-
12% лимфоцитов периферической крови,
содержат цитотоксические белки (перфорин,
гранзимы)
распознают и убивают опухолевые,
инфицированные вирусом, трансплантированные и
др. клетки
NKT- неклассическая субпопуляция Т-лимфоцитов,
сочетающая признаки Т-лимфоцитов и NK- клеток
28. В1- клетки субпопуляция В-лимфоцитов, занимающая промежуточное положение между клетками врожденного и приобретенного иммунитета
Особенности:
независимость синтеза антител от Тлимфоцитов
отсутствие иммунологической памяти
синтез низкоаффинных IgM – антител к
бактериальным ЛПС
первая линия защиты от капсульных
микроорганизмов
29. Гуморальные факторы врожденного иммунитета
Ферменты (способны расщеплять
клеточные стенки патогенов) – лизоцим,
хитиназа, фосфолипаза А2
Белки и пептиды, нарушающие
целостность микробной стенки – ПМП
(дефензины, кателицидины),
комплемент, эозинофильный катионный
протеин
Микробицидные сериновые протеазы
30. Гуморальные факторы врожденного иммунитета
Белки, связывающие ионы металлов (Fe,
Zn), необходимых для жизни патогенов –
лактоферрин, кальпротектин, мембранный
белок — ионный насос фагосом МФ и НФ,
выкачивающий ионы Fe, без которых не могут
размножаться микроорганизмы
Ферменты, генерирующие О2 и NO
(NADFH-оксидазная система,
миелопероксидаза, индуцибельная NO-синтаза
и др.)
31. Литература:
1. Хаитов Р.М. Иммунология: учеб. для студентов
мед Вузов.- М.: ГЕОТАР-Медиа, 2011.- 311 с.
2. Хаитов Р.М. Иммунология. Норма и патология:
учеб. для студентов мед Вузов и ун-тов.- М.:
Медицина, 2010.- 750 с.
3. Иммунология: учебник / А.А. Ярилин.- М.:
ГЕОТАР-Медиа, 2010.- 752 с.
4. Ковальчук Л.В. Клиническая иммунология и
аллергология с основами общей иммунололгии:
учебник. – М.: ГЕОТАР-Медиа, 2011.- 640 с.
Источник
