Фиброзный кортикальный дефект на мрт
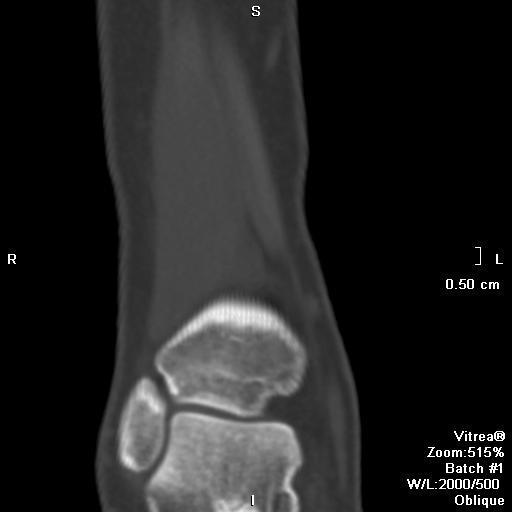
Неоссифицирующая фиброма — это наиболее распространённое неопухолевое фиброзное поражение костей. По своей природе это более крупный вид фиброзного кортикального дефекта (< 3 см); оба состояния отражают термин фиброксантома или метафизарный фиброзный дефект.
Эпидемиология
Неоссифицирующая фиброма очень часто встречается у детей и подростков и является наиболее частыми фиброзным поражением костей в этой возрастной группе, с пиком выявляемости 10-15 лет [4]. Распространенность составлеят до 30-40% среди здоровых детей. У мальчиков встречается в два раза чаще чем у девочек [6]. Обычно не встречается после 30 лет, поскольку самостоятельно спонтанно излечивается, постепенно замещаясь костной тканью.
Клиническая картина
Большинство неоссифицирующих фибром бессимптомны. Крупные поражения могут быть болезненными и, ослабляя кость, являться предрасполагающим фактором для возникновения патологического перелома. Множественные неоссифицирующие фибромы сочетаются с нейрофиброматозом I типа, фиброзной дисплазией и синдромом Яффе—Кампаначи (Jaffe-Campanacci syndrome). Редко неоссифицирующая фиброма может вызывать гипофосфатемический витамин-D-резистентный рахит [5].
Патология
Неоссифицирующая фиброма макроскопически представляет собой мясистое, волокнистое, желтое или коричнево-коричневое поражение с участками кровоизлияния [3].
Микроскопически поражение характеризуется высокой клеточностью, с наличием веретеновидных клеток, на фоне стромы, формируя так называемый «муаровый» узор. Встречаются пенистые гистиоцит и многоядерные гигантские клетки. Митотические фигуры и /или дисплазия не характерны для фиброксантомы [3]. Считается, что костные островки являются самоизлечившимися фиброксантомами.
Диагностика
Рентгенография /Компьютерная томография
Неоссифицирующая фиброма характеризуется дольчатой формой, обычно имеет склеротический ободок. Локализуются эксцентрично, в прилежащем к ростовой пластинке метафизе. С ростом пациента, смещается и отдаляется от ростовой пластинки. Не сочетается с периостальной реакцией, нарушением целостности кортикальной пластинки и не имеет мягкоткпнного компонента.
Магнитно-резонансная томография
МР картина разнообразная и зависит отдлительности заболевания и репаративной фазы, при которой получены изображения. В начале заболевания, поражение характеризуется высоким или промежуточным сигналом на Т2 взвешенных изображениях, окружённым по периферии низкоинтенсивным ободком, отражающем склеротическую границу. С началом оссификации сигнал становится низкоинтенсивным на всех последовательностях [2]. Контрастное усиление варьирует.
Сцинтиграфия
Данные сцинтиграфии зависят от фазы поражения. В целом они отрицательны; однако, во время процессов репарации присутсвуют умеренная гиперемия и умеренное поглащение. Если имеется выраженное поглощение или гиперемия, следует рассмотреть альтернативный диагноз или заподозрить перелом [3].
Лечение и прогноз
Неоссифицирующая фиброма относится к категории поражений «не трогай и оставь меня в покое«. В подавляющем большинстве случаев не требует биопсии и лечения. При вовлечении в процесс более половины диаметра кости, с целью профилактики патологического перелома, выполняется кюретаж с графитнгом/замещением кости [1].
Дифференциальный диагноз
- аневризмальная костная киста
- эксцетнтрический литический метафизарный дефект
- уровни жидкости при МР исследовании
- хондромиксоидная фиброма
- фиброзная дисплазия
- десмопластическая фиброма
Синонимы
- неоссифицирующая фиброма
- неоссифицированная фиброма кости
- фиброзный кортикальный дефект
- фиброксантома
- метафизарный фиброзный дефект
Источник
Fibrous Cortical Defect and Nonossifying Fibroma
eMedicine Specialties > Radiology > Musculoskeletal
Fibrous Cortical Defect and Nonossifying Fibroma
Author: Stacy E Smith, MD, Associate Professor of Radiology, Division of Musculoskeletal Imaging, University of Maryland School of Medicine
Contributor Information and Disclosures
Updated: Nov 28, 2007
* Print ThisPrint This
* Email ThisEmail This
* Overview
* Imaging
* Follow-up
* Multimedia
* References
* Keywords
Introduction
Background
The terms fibroxanthoma, nonossifying fibroma (NOF), fibrous cortical defect (FCD), and, less commonly, benign fibrous histiocytoma have all been used interchangeably in the radiology literature. NOF and FCD, however, are considered to be 2 distinct lesions with respect to size and natural history. Fibroxanthoma is the preferred term for the NOF lesion because it more accurately reflects the underlying pathologic findings. In the literature, FCD has a longer list of pseudonyms, including metaphyseal fibrous defect, metaphyseal supracondylar cortical defect, and developmental defect.
FCDs have been mislabeled or described as cortical avulsive irregularities, subperiosteal or periosteal desmoid, a variant of periostitis ossificans, and cortical desmoid. The cortical desmoid—or cortical avulsive injury, as it is currently known—is believed to be separate from the cortical defect, and it has been related to repetitive stress at the attachment of the extensor tendon fibers along the linea aspera of the distal femur.1
Fibroxanthoma and FCDs are nonaggressive fibrous lesions of bone that are distinguished from one another historically by their size and natural history. Both are considered to be developmental defects and to be nonaggressive. They were first described by Lichtenstein and Jaffe in 1942,2 and they typically occurred within the metaphysis of growing long tubular bones in children, most commonly about the knee. Controversy continues regarding the correct terminology and etiology of these lesions.
The distinction between FCD and fibroxanthoma is based on size and natural history. FCDs are asymptomatic, small (<3 cm), eccentrically located, metaphyseal cortical defects; most of these spontaneously disappear. However, some evolve and enlarge into fibroxanthomas. Conversely, fibroxanthomas (>3 cm) are larger, eccentric, intramedullary lesions that abut the cortex; they have a typical, superficial, scalloping pattern in the adjacent cortex.
While these lesions also can heal spontaneously (with reactive bone filling in the central lucent fibrous tissue component), they can also persist, with interval growth that continues into adulthood. Typically, fibroxanthomas are asymptomatic. However, the larger lesions may become symptomatic, with a risk of pathologic fracture. Steiner suggested that these 2 lesions are secondary to cellular proliferation due to aberrations in local development.3
(See also the eMedicine articles Fibrous Cortical Defect [Orthopedic Surgery] and Atypical Fibroxanthoma [Dermatology], as well as the article Less Common Cutaneous Malignancies, on Medscape.]
Anatomy
Approximately 90% of cases of both lesions involve the tubular long bones.5,6 Common sites include the femur (most commonly the distal femoral metaphysis [38%]), the proximal and distal tibia (43%), and the knee (55%); most lesions occur around the knee.7 The tibial diaphysis is involved in only 10% of cases. The fibula is affected in 8-10% of cases, as noted in one series at the Armed Forces Institute of Pathology (AFIP). Both fibroxanthoma and FCDs are uncommon in the upper extremity; however, of those reported in the literature, 8% were in the humerus, and both radial and ulnar lesions were rare. Less common sites include the innominate bone, clavicle, skull, scapula, mandible, and small bones of the hands and feet.
Typically, both lesions are metaphyseal and arise close to the physeal plate. The FCD arises within the cortex, whereas the fibroxanthoma arises eccentrically within the medullary cavity. Both lesions usually arise from the posterior wall of the tubular bone, and involvement of the medial rather than lateral osseous surface is characteristic. With healthy growth of the osseous skeleton, the lesions extend toward the shaft, and if they do not involute and disappear, they may extend into the diaphysis. An epiphyseal location is distinctly uncommon and has been reported only in unusual cases of multifocal lesions. Both lesions are more commonly solitary, and they can occur in similar locations.
Multifocal lesions in one or more bones can occur with FCDs; however, multifocal fibroxanthomas are less common and, if present, have other clinical manifestations (see Clinical Details). Moser et al described lesions in clusters in the same bone, at opposite ends of the same bone, and at opposite sides of the joints.8
Presentation
Typically, FCDs are asymptomatic and are detected only incidentally on radiographs obtained for reasons other than the evaluation of FCD. Fibroxanthomas also are characteristically asymptomatic; however, in larger lesions, mild pain may occur secondary to radiographically undetected microfractures that may eventually lead to painful and radiographically evident pathologic fractures.9 Although they are most commonly solitary lesions, multiple lesions have been described. Rare reports of multiple fibroxanthomas in patients with neurofibromatosis (5%) exist in the literature.
The presence of extraskeletal congenital anomalies (eg, café-au-lait spots, mental retardation, hypogonadism or cryptorchidism, ocular abnormality, cardiovascular malformations) in association with multiple nonossifying fibroxanthomas constitute the clinical and radiologic spectrum known as Jaffe-Campanacci syndrome, which was first reported in 1983.10,11 In one series, Moser et al also noted that the coexistent osteochondromas can be present.8
Preferred Examination
Plain radiographic findings are virtually diagnostic of both FCDs and NOFs; most of these lesions have a characteristic location and appearance. If a discrepancy in appearance or age or an atypical associated symptom is present, advanced imaging (usually computed tomography [CT] or magnetic resonance imaging [MRI]) can be performed.12,13,14,15
Differential Diagnoses
Chondromyxoid Fibroma
Fibrous Dysplasia
Osteoid Osteoma
Other Problems to Be Considered
Although the radiographic findings usually are pathognomonic, the differential diagnosis includes the following: chondromyxoid fibroma; fibrous dysplasia, particularly if lesions are multiple and polyostotic (in comparison, fibrous dysplasia has a more central and unilateral location and more of a ground-glass appearance); osteoid osteoma (typically has a central nidus); bone abscess; periosteal chondroma; chondromyxoid fibroma; avulsive cortical irregularity or periosteal desmoid (saucerlike radiolucent defect in the cortex with adjacent sclerosis and periostitis); and desmoplastic fibroma.
Reports of soft-tissue desmoid or desmoplastic fibromas of bone have been noted only when the fibrous tissue in these lesions is examined at biopsy. Although much less common, consider giant cell tumor and aneurysmal bone cysts in the differential diagnosis of a large lobulated fibroxanthoma at radiographic study. However, both of these lesions are clearly distinguished at CT or MRI. A herniation pit also has been described in the differential diagnosis of FCD.
The cortical avulsive injury that occurs in adolescents has been noted more frequently. It often was and still is confused with FCD. At histologic evaluation, cortical avulsive injury has a nonspecific fibrous appearance with intermixed spicules of bone and healthy osteoblasts. Later findings indicated that the histologic features of the cortical avulsive lesion (characteristically located at the insertion of the tendon at the posteromedial cortex of the distal femur) included those of healthy tendon and interspersed bone and cartilage; therefore, this lesion is separate from FCD and secondary to repetitive trauma rather than being a true developmental defect.
Radiography
Findings
The imaging features of fibroxanthomas are pathognomonic. Typically, a metadiaphyseal, eccentric, ovoid or round, intramedullary geographic radiolucency, with a sharply marginated sclerotic rim of reactive bone and a scalloped contour, is present. The medullary rim typically is thicker than the cortical rim. While they initially appear near the physeal plate, they eventually appear further down within the diaphysis, following a normal growth pattern. The epiphysis is never affected. Larger lesions can appear multiloculated, with dimensions as large as 4-7 cm, with erosion of the endosteal surface of the cortex.14,15,16,17
Since fibroxanthomas are thought to evolve from the FCD, the typical FCD appears similar but smaller, with the following defining features:
* They usually are round or oval geographic radiolucencies that measure 1-3 cm.
* They are located within the posteromedial aspect of the distal femoral cortex along the medial supracondylar ridge just proximal to the adductor tubercle.
* A sharply marginated rim of reactive bone is identified where the lesion impinges on the medullary cavity.
* No associated soft-tissue mass is present.
* FCDs are best visualized in the anteroposterior (AP) oblique projection of the femur, with the limb in 20-40 º external rotation.
While they typically are eccentric lesions within tubular bones, fibular lesions are an exception in that the entire diameter of the bone can be involved; this makes diagnosis slightly more difficult. Usually, fibroxanthomas are slow-growing lesions. Variations in size and density are secondary to interval growth and the natural resolution of the lesions; these processes include reactive bone formation, which can fill in and replace the central lucent defect over time.
This increase in sclerosis can be confusing to the observer and often is mistaken for fibrous dysplasia when it is present in the midst of the progressive changes. Initially, some of the lesions may be confused with neoplasms if one is not aware of the typical location and spectrum of their appearances over time. Knowledge of these characteristics is particularly important if periosteal reaction is present, since periosteal reaction occurs only with a pathologic fracture through the lesion.
Degree of Confidence
These nonaggressive fibrous lesions have a characteristic location and appearance and are rarely confused with other lesions if the observer is aware of the spectrum of appearances over time. The degree of confidence is virtually certain in most cases; further imaging is required only if atypical symptoms or associated injuries are present.
False Positives/Negatives
Cortical avulsive injury to the distal posteromedial femur often has been confused with FCD. Usually, the former lesion has more cortical irregularity and is located at the direct insertion of the gastrocnemius muscle. They are more common in young athletes. These 2 may be part of a spectrum of the same type of lesion but, for now, are considered separately.
Computed Tomography
Findings
Advanced imaging usually is not required unless an atypical appearance or symptom is present. The characteristic lesion is eccentrically located, intramedullary, well marginated, and sclerotic, with a central lucency. Heterogeneous lucency and reactive sclerosis is identified at later stages in the case of the involuting fibroxanthoma. The central fibrous component has a nonspecific soft-tissue attenuation value; older lesions have a high attenuation value secondary to the reactive bone component.
CT images are useful because they can clearly depict the cross-sectional extent of bone involvement and the degree of cortical thinning, features that can help in determining the risk of pathologic fracture.
The literature states that a tubular bone with a fibroxanthoma has a high risk for fracture if the lesion involves more than 50% of the width or if it extends more than 33 mm. If a fracture has occurred, a mild periosteal reaction may be present with subtle soft-tissue swelling; otherwise, no soft-tissue component is seen with fibroxanthomas, and the margins are very well demarcated.
With FCDs, the subtle apparent thickening of the cortical margin is noted with only subtle central cortical lucency because these lesions are very small in early disease. CT may help elucidate the irregular avulsive injury that is often confused with this lesion. Early differentiation between stress injuries caused by the adductor magnus muscle and the medial head of the gastrocnemius muscle, as well as clarification of the characteristic cortical defect, is possible with CT. When radiographic findings are not diagnostic, CT findings may obviate biopsy.
Degree of Confidence
Both lesions are fairly characteristic, and advanced imaging rarely is performed. The degree of confidence is 99%.
False Positives/Negatives
False-positive findings may include very small cortical avulsive irregularities (see Findings). A small cortical osteoid osteoma may be confused as an FCD if the imaging sections are too thin and the nidus is not elucidated. However, clinical pain occurs with osteoid osteomas, which should not be confused with FCDs.
Magnetic Resonance Imaging
Findings
Usually, both fibroxanthoma and FCDs are noted incidentally on images obtained for reasons other than evaluation of these lesions. Kransdorf et al described their characteristic low signal intensity on both T1- and T2-weighted spin-echo MRIs.13 This finding is similar to that of other nonossified lesions that they reviewed. Low signal intensity on T2-weighted images was thought to represent hemosiderin deposits or large amounts of collagen, which are consistent with the fibrous tissue content.
A peripheral hypointense rim represents the marginal sclerosis depicted on radiographs and the peripheral reactive sclerosis present at histologic evaluation. Bright areas can appear with sufficient cellularity. In a study by Jee et al, internal septa were noted in 95% of cases; these were correlated with subtle trabeculae depicted on the radiographs.12
Usually, MRI is not indicated in FCDs. However, study findings have shown that this intracortical lesion typically has low signal intensity on T1-weighted images and has increasing signal intensity on proton density– and T2-weighted images, which are consistent with their heterogeneous fibrous histologic characteristics. A rim of lower signal intensity represents the sclerotic border that abuts the medullary and cortical borders.
Degree of Confidence
Because MRI is not commonly used in the evaluation of these lesions, data are limited. The degree of confidence with MRI alone is approximately 95%.
False Positives/Negatives
Other fibrous lesions can have the same signal intensity changes as those of fibroxanthoma and FCDs. However, the location and lack of pain should be helpful.
Ultrasonography
Findings
Typically, ultrasonography is not used to evaluate these lesions.
Nuclear Imaging
Findings
Minimal-to-mild accumulation of bone-seeking pharmaceutical agents (eg, technetium-99m [99m Tc]) occurs and is indicative of a benign process. The intensity of the uptake is much less than that of active bone lesions. In a child or adolescent, a typical eccentric region of agent uptake located a short distance from the physis of a tubular bone is diagnostic for fibroxanthoma in the appropriate setting. FCDs do not have uptake on bone scintigrams obtained with99m Tc. In children, this finding can be masked by the proximity of the lesion to the distal femoral epiphyseal plate, which itself has marked tracer uptake.1,18,19
Degree of Confidence
Data are limited.
False Positives/Negatives
Cortical avulsive irregularities have increased tracer uptake in a location similar to that expected for a FCD. However, the former lesion has obvious uptake, unlike the usual pattern of no uptake in FCDs. Early osteosarcoma, particularly in the periosteal variant, can have99m Tc uptake within the distal posterior femur. Radiographic correlation helps in distinguishing between the aggressive lesion and benign FCD.
Multimedia
| Media file 1: Anteroposterior radiograph of the distal femur shows a solitary corticate lucent lesion within the posteromedial distal femoral cortex; this finding is consistent with a fibrous cortical defect. |
| Media file 2: Oblique (45°) radiograph of the distal femur best depicts the fibrous cortical defect. No soft-tissue mass or periosteal reaction is present. |
| Media file 3: Anteroposterior image of the distal femur in an 8-year-old boy. Pain in the distal femur led to imaging. Cortical irregularity is present at the distal medial femoral metaphyseal cortex, which suggests cortical avulsive injury rather than fibrous cortical defect. |
| Media file 4: Coronal proton density–weighted MRI of the distal femur shows a fibrous cortical defect with a low signal intensity peripheral rim and its intracortical nature and subtle, central, intermediate signal intensity. |
| Media file 5: Coronal inversion-recovery MRI of the distal femur shows a fibrous cortical defect with a low signal intensity border and a central area with heterogeneous high signal intensity. No edema or cortical irregularity is present. |
| Media file 6: Anteroposterior radiograph of the distal tibia shows a solitary, small, well-defined lucent lesion in the lateral distal tibial metadiaphysis that abuts the cortex. This finding is consistent with a benign fibrous cortical defect or nonossifying fibroma. Note the lack of multiple lobulations in this early lesion. |
| Media file 7: Anteroposterior radiograph of the distal tibia shows a lobulated well-circumscribed nonossifying fibroma that is eccentrically located within the distal tibia metadiaphysis. Peripheral sclerotic border with a central lucency is typical of this lesion. |
| Media file 8: Anteroposterior radiograph of the distal tibia and fibula shows an expansile corticate lytic nonossifying fibroma within the distal fibular metaphysis with prominent expansion in the small tubular bones. A second nonossifying fibroma within the distal lateral tibial metaphysis in this patient with multiple nonossifying fibromas is noted. No clinical symptoms were present in this patient, and Jaffe-Campanacci syndrome could not be confirmed. |
| Media file 9: Anteroposterior radiograph of the distal tibia and fibula obtained later in same patient as in Image 7 demonstrates increased sclerosis and thickening of the peripheral rim of both lesions and increased heterogeneous central opacity; this finding is consistent with the natural growth pattern of these fibrous lesions. |

Источник
Что важно знать о кортикальном дефекте и фиброме кости у ребенка
- Фиброзный дефект кортикального слоя и неоссифицированная фиброма — наиболее частые поражения костей.
- Возрастной пик — 7-8 лет
- Частота 30% у детей и подростков
- Мальчики поражаются в 2 раза чаще, 3 чем девочки
- Обычно возникает до закрытия § зон роста
- Пенетрация кортикального слоя надкостницей
- Предрасположенность к развитию в длинных трубчатых костях
- При кортикальном дефекте поражение ограничено кортикальным слоем
- Неоссифицироеанная фиброма распространяется на костный мозг
- Гистология: веретеновидные клетки и гистиоциты, многоядерные гигантские клетки, сходные с остеокластами, лимфоциты, плазматические клетки
- Предрасположенность к поражению дистальных медиальных отделов малоберцовой кости, проксимальных отделов большеберцовой кости и малоберцовой кости, проксимальных отделов плеча.
Какой метод диагностики фибромы кости у детей выбрать: МРТ, КТ, рентген, УЗИ
Что покажут снимки рентгена кости при фиброме
- Кистозное поражение кости
- Обычно возникает как эксцентрическое поражение метафизов
- Легкий краевой склероз, иногда напоминающий морскую раковину
- Овальная форма
- Продольная ось опухоли параллельна продольной оси кости
- Истончение кортикального слоя
- Первоначально возникает в проксимальных закрытых зонах роста
- Типичные признаки злокачественного поражения отсутствуют
- Физиологический рост кости увеличивает расстояние между поражением и зоной роста, поражение становится более склерозированным (оссифицированная фиброма).
Неоссифицироеанная фиброма. Рентгенография колена в двух проекциях. Классический рентгенографический вид неоссифицированной фибромы в проксимальном заднемедиальном метафизе большеберцовой кости
Что покажет УЗИ кости при дефекте кортикального слоя
- Четко ограниченный дефект кости
- Заполнен гипоэхогенным материалом
- Допплеровский режим выявляет выраженную васкуляризацию внутри поражения
- В динамике эхогенность поражения увеличивается, а размеры уменьшаются.
В каких случаях ребенку проводят МРТ конечностей при фиброме костей
- Не требуется для подтверждения диагноза
- Обычно является случайной находкой
- Определяется изоинтенсивной по отношению к мышцам на Т1-взвешенных изображениях
- Гиперинтенсивное поражение на Т2-взве- шенных изображениях
- Т1- и Т2-взвешенные изображения визуализируют гипоинтенсивное кольцо краевого склероза
- Легкое контрастное усиление, особенно в краевой области
- Отсутствие периостальной реакции.
МРТ, неусиленное Т1 -взвешенное изображение. Неоссифицироеанная фиброма дистального бокового метафиза большеберцовой кости.
Клинические проявления
Типичные симптомы:
- Бессимптомное течение
- Обычно обнаруживается случайно
- Крупные поражения могут приводить к патологическим переломам.
Тактика лечения
- Выскабливание и имплантация решетчатого трансплантата показаны, если поражение занимает более 50% поперечного сечения полости костного мозга.
Течение и прогноз
- Большинство поражений спонтанно исчезают путем окостенения в течение 2-4 лет
- Может наблюдаться дальнейший рост
- Поражения не рецидивируют после хирургического удаления.
Осложнения
- патологические переломы.
Какие заболевания имеют симптомы, схожие с фиброзом кости у детей
Доброкачественная фиброзная гистиоцитома
— обычно возникает в возрасте до 25 лет;
— может вызывать боли;
— может рецидивировать после кюретажа;
— рентгенологически не различимы.
Периостальный десмоид
— первично возникает в возрасте 12-20 лет;
— предрасположенность к поражению задней части медиальной лодыжки малоберцовой кости;
— сходен с фиброзным кортикальным дефектом;
— может проявлять признаки злокачественного процес-
— обычно спонтанно исчезает;
— биопсия противопоказана.
Фиброзная дисплазия
— поражение одной или нескольких костей;
— предрасположенность к поражению бедра, болыпеберцевой кости и ребер;
— образуется от центра кости;
— везикулярная форма;
— возникает при таких состояниях, как синдром Мак-Кьюна-Олбрайта.
Советы и ошибки
- Заживление неоссифицированной фибромы можно ошибочно принять за остеосклеротический злокачественный процесс кости
- МРТ и КТ не показаны для оценки фиброзного кортикального дефекта
- Биопсия фиброзного кортикального дефекта противопоказана.
Источник
Автор: Oleg Kruglov
Неоссифицирующая фиброма – это наиболее распространённое неопухолевое фиброзное поражение костей. По своей природе это более крупный вид фиброзного кортикального дефекта (< 3 см); оба состояния отражают термин фиброксантома или метафизарный фиброзный дефект.
Эпидемиология
Неоссифицирующая фиброма очень часто встречается у детей и подростков и является наиболее частыми фиброзным поражением костей в этой возрастной группе, с пиком выявляемости 10-15 лет [4]. Распространенность составлеят до 30-40% среди здоровых детей. У мальчиков встречается в два раза чаще чем у девочек [6]. Обычно не встречается после 30 лет, поскольку самостоятельно спонтанно излечивается, постепенно замещаясь костной тканью.

Клиническая картина
Большинство неоссифицирующих фибром бессимптомны. Крупные поражения могут быть болезненными и, ослабляя кость, являться предрасполагающим фактором для возникновения патологического перелома. Множественные неоссифицирующие фибромы сочетаются с нейрофиброматозом I типа, фиброзной дисплазией и синдромом Яффе—Кампаначи (Jaffe-Campanacci syndrome). Редко неоссифицирующая фиброма может вызывать гипофосфатемический витамин-D-резистентный рахит [5].
Патология
Неоссифицирующая фиброма макроскопически представляет собой мясистое, волокнистое, желтое или коричнево-коричневое поражение с участками кровоизлияния [3].
Микроскопически поражение характеризуется высокой клеточностью, с наличием веретеновидных клеток, на фоне стромы, формируя так называемый «муаровый» узор. Встречаются пенистые гистиоцит и многоядерные гигантские клетки. Митотические фигуры и /или дисплазия не характерны для фиброксантомы [3]. Считается, что костные островки являются самоизлечившимися фиброксантомами.
Диагностика
Рентгенография /Компьютерная томография
Неоссифицирующая фиброма характеризуется дольчатой формой, обычно имеет склеротический ободок. Локализуются эксцентрично, в прилежащем к ростовой пластинке метафизе. С ростом пациента, смещается и отдаляется от ростовой пластинки. Не сочетается с периостальной реакцией, нарушением целостности кортикальной пластинки и не имеет мягкоткпнного компонента.
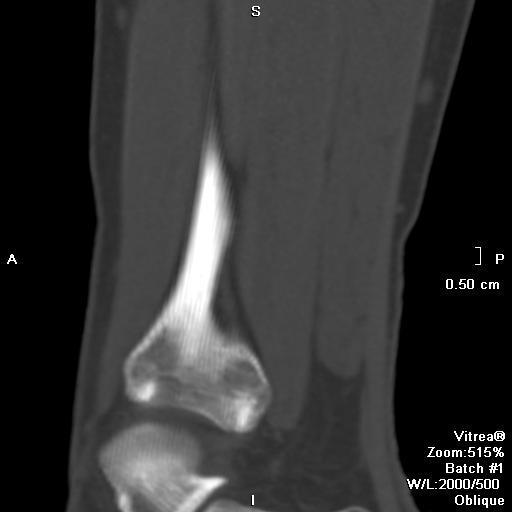
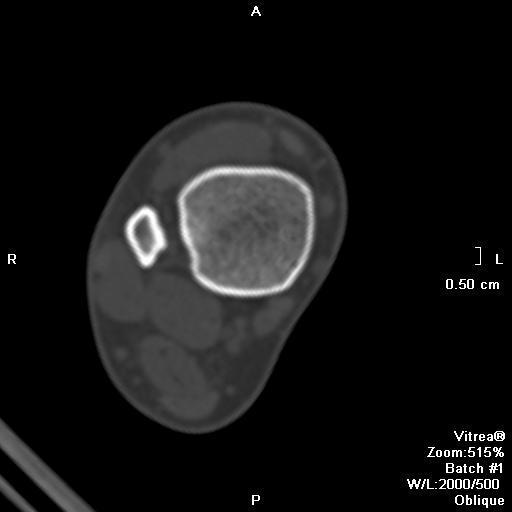
Магнитно-резонансная томография
МР картина разнообразная и зависит отдлительности заболевания и репаративной фазы, при которой получены изображения. В начале заболевания, поражение характеризуется высоким или промежуточным сигналом на Т2 взвешенных изображениях, окружённым по периферии низкоинтенсивным ободком, отражающем склеротическую границу. С началом оссификации сигнал становится низкоинтенсивным на всех последовательностях [2]. Контрастное усиление варьирует.
Сцинтиграфия
Данные сцинтиграфии зависят от фазы поражения. В целом они отрицательны; однако, во время процессов репарации присутсвуют умеренная гиперемия и умеренное поглащение. Если имеется выраженное поглощение или гиперемия, следует рассмотреть альтернативный диагноз или заподозрить перелом [3].
Лечение и прогноз
Неоссифицирующая фиброма относится к категории поражений “не трогай и оставь меня в покое”. В подавляющем большинстве случаев не требует биопсии и лечения. При вовлечении в процесс более половины диаметра кости, с целью профилактики патологического перелома, выполняется кюретаж с графитнгом/замещением кости [1].
Дифференциальный диагноз
- фиброзный кортикальный дефект
- аневризмальная костная киста
- эксцетнтрический литический метафизарный дефект
- уровни жидкости при МР исследовании
- хондромиксоидная фиброма
- фиброзная дисплазия
- десмопластическая фиброма
Синонимы
- неоссифицирующая фиброма
- неоссифицированная фиброма кости
- фиброзный кортикальный дефект
- фиброксантома
- метафизарный фиброзный дефект
Использованные источники:
- Jee WH, Choe BY, Kang HS et-al. Nonossifying fibroma: characteristics at MR imaging with pathologic correlation. Radiology. 1998;209 (1): 197-202.
- Stacy GS, Dixon LB. Pitfalls in MR image interpretation prompting referrals to an orthopedic oncology clinic. Radiographics. 27 (3): 805-26.
- Betsy M, Kupersmith LM, Springfield DS. Metaphyseal fibrous defects. J Am Acad Orthop Surg. 12 (2): 89-95.
- Hod N, Levi Y, Fire G et-al. Scintigraphic characteristics of non-ossifying fibroma in military recruits undergoing bone scintigraphy for suspected stress fractures and lower limb pains. Nucl Med Commun. 2007;28 (1): 25-33.
- François S, Lefort G, Poli-Merol ML et-al. Vitamin-resistant rickets cured by removal of a bone tumor. Review of the literature. Rev Chir Orthop Reparatrice Appar Mot. 1998;83 (4): 387-92.
- Grove J, Robbins C. Nonossifying fibroma: a literature review and case report.
- A.Prof Frank Gaillard et al. Non-ossifying fibroma. Radiopaedia.
Источник
