Фокальная кортикальная дисплазия на мрт

Фокальная кортикальная дисплазия — это заболевание из гетерогенной группы аномалий развития коры головного мозга, характеризующееся нарушением пролиферации нейронов и нарушением архитектоники коры. Является одной из наиболее частых причин эпилепсии, может сочетаться с склерозом гиппокампов и кортикальными глионейрональными опухолями.
Клиническая картина
Фокальная кортикальная дисплазия является наиболее частой причиной рефрактерной эпилепсии.
Классификация
С момента первого описания фокальной кортикальной дисплазии Тейлором в 1971 г. Было разработано много различных классификации данной патологии [5].
Наиболее распространенными классификациями, используемыми до недавнего времени, были гистопатологическая классификация Palmini [6] предложенная в 2004 году и генетическая / морфологическая классификация Барковича [2] предложенная в 2005 году.
Наиболее актуальной и широко распространенной в настоящее время считается классификация предложенная Blumcke в 2011 году.
К сожалению, как и в случае многих других классификаций, в разных системах существует дублирование сущностей, а одна и та же терминология может использоваться с разными значениями. Таким образом, необходимо явно указывать, используемую классификацию (напр., «IIB тип по Blumcke»).
Диагностика
Магнитно-резонансная томография
МРТ является модальностью выбора у пациентов с подозрением на фокальную кортикальныю дисплазию. У различных типов фокальной кортикальной дисплазии существет много схожих черт, а отдельные типы при МРТ могут не иметь выявляемых изменений.
Основные черты фокальной кортикальной дисплазии включают [4]:
- утолщение коры
- размытость границ серого и белого вещества с аномальной архитектоникой субкортикального слоя
- гиперинтенсивный МР сигнал от белого вещества на T2/FLAIR взвешенных изображениях с или без признаков трансмантийной дисплазии
- гиперинтенсивный МР сигнал от серого вещества на T2/FLAIR взвешенных изображениях
- изменение структуры борозд и извилин
- долевая гипоплазия или атрофия
При каждом из типов фокальной кортикальной дисплазии эти признаки выражены в разной степени. Нижеприведенные типы относятся к классификации фокальной кортикальной дисплазии Blumcke (2011).
I тип
- локализация
- Ia тип: локализация обычно ограничена височной долей [4]
- при сочетании с атрофией гиппокампов данный тип сейчас относится к IIIa типу по классификации Blumcke
- Ib тип: чаще встречается за пределами височной доли
- Ia тип: локализация обычно ограничена височной долей [4]
- структура
- размытость границ серого и белого вещества (менее выражена, чем при II типе ФКД)
- выраженная “сегментарная” или долевая атрофия / гипоплазия с локальной потерей объема белого вещества
- МР сигнал
- белое вещество
- промежуточно повышенный МР сигнала на T2/FLAIR взвешенных изображениях
- сниженный МР сигнал на T1 взвешенных изображениях
- белое вещество
II тип
- локализация
- часто встречается в лобных долях
- менее часто, по сравнению с ФКД I типа, в височных долях
- структура
- изменение структуры борозд и извилин
- выраженная размытость границ серого и белого вещества
- утолщение коры
- МР сигнал
- белое вещество
- промежуточно повышенный МР сигнал на T2/FLAIR взвешенных изображениях, обычно более интенсивный, чем сигнал от прилежащей коры
- сниженный МР сигнал на T1 взвешенных изображениях
- локально измененненный сигнал может может распространяться за пределы коры по направлению к желудочкам (трансмантийный признак): что не характерно для I типа
- серое вещество
- несколько повышенный МР сигнала на T2 взвешенных изображениях
- кора остается гипоинтенсивной, по отношению к повышеному сигналу от белого вещества на Т2 взвешенных изображениях [4]
- более выраженный чем при I типе
- несколько повышенный МР сигнала на T2 взвешенных изображениях
- белое вещество
III тип
Фокальная кортикальная дисплазия III типа характеризуется наличием ряда сочетанных нарушений нарушений (напр, IIIa — сочетается с атрофией гиппокампов, IIIb — сочетается с глионейрональными опухолями (напр, ДНЭО), IIIc — сочетается с сосудистыми мальформациями; IIId — сочетается с инсультом раннего детского возраста).
Источник

Фокальная корковая дисплазия — аномалия структуры коры головного мозга, затрагивающая её ограниченный участок. Клинически проявляется фокальными двигательными эпиприступами с потерей сознания, но небольшой продолжительностью. Диагностируется неврологом или эпилептологом по данным ЭЭГ, специально проведённого МР-сканирования, субдуральной электрокортикографии, ПЭТ головного мозга. Как правило, эпилепсия при корковой дисплазии устойчива к проводимой противоэпилептической терапии. Альтернативным методом лечения выступает нейрохирургическая резекция участка дисплазии.
Общие сведения
Фокальная корковая дисплазия (ФКД) — возникшее в период внутриутробного развития локальное нарушение в строении мозговой коры. Является самым частым этиофактором развития эпилепсии у детей. По данным международного исследования ILAE (2005 г.) ФКД была диагностирована у 31% детей с эпилепсией. Отличительными особенностями эпилептических пароксизмов при ФКД являются: устойчивость к проводимой противоэпилептической терапии, агрессивное течение с развитием у детей задержки психического развития и эпилептической энцефалопатии, эффективность нейрохирургических способов лечения.
Локальные диспластические изменения коры располагаются преимущественно в височных и лобных долях. Они слабо заметны на макроскопическом уровне, что затрудняет диагностику ФКД даже при помощи таких современных методов нейровизуализации как МРТ. Проблемы диагностики ФКД особо актуальны в практической неврологии и педиатрии, поскольку её выявление как причины эпилептических пароксизмов имеет решающее значение для выбора эффективной лечебной тактики в отношении резистентных форм эпилепсии.
Фокальная корковая дисплазия
Причины фокальной корковой дисплазии
ФКД обусловлена нарушением окончательных этапов развития церебральной коры (кортикогенеза) во внутриутробном периоде. В результате нарушений миграции и дифференцировки клеток коры образуется участок с аномальными нейронами, патологической утолщенностью, уплощенностью извилин или изменённой архитектоникой (появлением клеток, типичных для одного слоя, в другом слое коры). Формирование фокальной корковой дисплазии происходит незадолго до родов — за 4-6 недель до окончания периода внутриутробного развития. Более тяжёлые формы пороков мозговой коры (например, полимикрогирия, гемимегалэнцефалия) связаны с нарушениями конца 2-го начала 3-его триместра беременности.
Нельзя исключить генетическую природу ведущего к ФКД сбоя в кортикогенезе. Так, у многих пациентов обнаружены изменения в гене TSC1, которые также наблюдаются при туберозном склерозе. В настоящее время проводятся международные исследования по поиску генетического субстрата корковых дисплазий.
Классификация фокальной корковой дисплазии
До недавнего времени выделяли 2 основных типа ФКД. В 2011 г. была разработана новая классификация, в которую включён 3-й тип, ассоциированный с другим основным поражением церебральных структур. Согласно этой классификации выделяют:
ФКД I типа — локальное нарушение архитектоники коры: радиальное (IA), тангенциальное (IB) или смешанное (IC). Выявляется у 1,7% обследованных практически здоровых людей.
ФКД II типа — очаговое нарушение цитоархитектоники с наличием аномальных нейронов (IIA) и так называемых баллонных клеток (IIB). Как правило, дисплазия затрагивает лобные доли.
ФКД III типа — вторичное нарушение корковой архитектоники, обусловленное другой патологией: мезиальным темпоральным склерозом (IIIA), глиальной опухолью (IIIB), мальформацией сосудов головного мозга (IIIC) или другими нарушениями (IIID) — энцефалитом Расмуссена, нейроинфекцией, посттравматическими или постишемическими изменениями и пр.
Симптомы фокальной корковой дисплазии
Ведущим клиническим проявлением ФКД выступает фокальная эпилепсия. Как правило, она манифестирует в детском возрасте. Эпилептические пароксизмы отличаются своей кратковременностью — длятся не более минуты. Среди них преобладают сложные (с расстройством сознания) фокальные моторные приступы, зачастую с автоматизмами в начальном периоде пароксизма. Спутанность сознания в постприступный период выражена незначительно. Характерны двигательные феномены и внезапные падения. Вторичная генерализация эпиприступов происходит заметно быстрее, чем при височной эпилепсии.
Возраст дебюта эпилепсии и сопутствующая клиническая симптоматика зависят от типа, выраженности и расположения очага корковой дисплазии. Ранняя манифестация аномалии обычно сопровождается задержкой психического развития ребёнка и когнитивными нарушениями.
ФКД I типа имеет менее тяжёлое течение и не всегда проявляется эпиприступами. У ряда пациентов она приводит к затруднению в познавательной деятельности и проблемам в обучении. ФКД II типа сопровождается тяжёлыми парциальными и вторично генерализованными эпиприступами. У многих пациентов наблюдается эпилептический статус. Клиника и течение ФКД III типа зависит от характера основной патологии.
Диагностика фокальной корковой дисплазии
Основной метод диагностики ФКД — магнитно-резонансная томография. Она должна выполняться по специальному протоколу с толщиной срезов 1-2 мм. Только такое тщательное сканирование способно выявить минимальные структурные изменения мозговой коры. В МРТ диагностике корковой дисплазии имеет значение опыт и квалификация рентгенолога. Поэтому при необходимости результаты исследования следует показать более опытному в этом вопросе специалисту.
К МРТ признакам ФКД относятся: локальная гипоплазия или утолщение коры, «смазывание» перехода между белым и серым веществом, изменённый ход извилин, повышенный МР-сигнал на ограниченном участке коры при исследовании в режимах Т2 и FLAIR. Каждый тип ФКД имеет свои особенности МРТ-картины.
В обязательно порядке пациентам с ФКД проводится электроэнцефалография. В большинстве случаев она выявляет очаговую эпилептическую активность мозга не только в момент приступа, но и в межприступный период. Во время приступа отмечается повышенная возбудимость и активация зон коры, прилежащих в визуализируемому на МРТ очагу дисплазии. Это связано с наличием аномальных клеток и за пределами основного участка корковой дисплазии, который является лишь «верхушкой айсберга».
Выявление зоны начала эпилептического приступа возможно при помощи ПЭТ, совмещённой с МРТ-изображением. При этом радиофармпрепарат должен быть введён пациенту после первого же пароксизмального разряда. Такое исследование особенно ценно при МРТ-негативных случаях ФКД и при несовпадении очага, визуализируемого на МРТ, с данными ЭЭГ. Для более точного определения расположения эпилептогенного очага проводится инвазивная электрокортикография с установкой субдуральных электродов, требующая краниотомии.
Лечение фокальной корковой дисплазии
Терапию начинают с подбора эффективного противосудорожного препарата и его дозы. Пациента совместно курируют эпилептолог и невролог. Возможно применение карбамазепина, препаратов вальпроевой к-ты, диазепама, леветирацетама, топирамата и др. антиконвульсантов. Однако зачастую эпилепсия при ФКД оказывается резистентной к противосудорожной терапии. В таких случаях ставится вопрос о хирургическом лечении и проводится консультация нейрохирурга.
Поскольку диспластические изменения носят фокальный характер, то хирургическое удаление патологического очага является эффективным способом лечения ФКД. В начале нейрохирургического вмешательства проводится электростимуляция и индивидуальная интраоперационная кортикография с составлением карты функционально важных участков коры, что позволяет избежать их травмирования в ходе операции. Многие нейрохирурги настаивают на целесообразности как можно более радикального удаления диспластического очага для достижения наилучших результатов лечения. Сложность заключается в широком распространении зоны точечно расположенных патологически изменённых клеток вокруг основного очага и невозможности их полного удаления. Распространённые и билатеральные эпилептогенные поражения являются противопоказанием к хирургическому лечению.
В зависимости от локализации и распространённости очага применяется один из 3 видов оперативных вмешательств: селективная резекция эпилептогенной зоны, стандартизированная резекция головного мозга (лобэктомия), тэйлорированная резекция — «выкраивание» зоны дисплазии, определённой в ходе кортикографии. При ФКД III типа зачастую требуется удаление и дисплазии, и основного очага поражения (опухоли, участка склероза, сосудистой мальформации и т. п.).
Прогноз при фокальной корковой дисплазии
Прогноз зависит от типа ФКД, своевременности проведённого лечения, радикальности удаления участка корковой дисплазии. Консервативная терапия, как правило, не даёт желаемого результата. Длительное течение эпилепсии в детском возрасте чревато нарушением нервно-психического развития с исходом в олигофрению.
Хирургическое лечение наиболее эффективно при единичном хорошо локализуемом очаге. По некоторым данным полное отсутствие пароксизмов или их значительное урежение наблюдается у 60% прооперированных пациентов. Однако спустя 10 лет приступы отсутствуют только у 32%. По всей видимости, рецидив эпилепсии в таких случаях связан с неполным удалением эпилептогенных элементов.
Стойкие послеоперационные неврологические расстройства отмечаются в 2% случаев, при распространённых поражениях — в 6%. Риск их развития повышен при проведении лобэктомии и вмешательствах вблизи функционально значимых участков коры.
Источник
Ситников Андрей Ростиславович
Фокальные корковые дисплазии (ФКД), являющиеся структурными аномалиями коры головного мозга, выявляются у 12 — 50 % пациентов с фармакорезистентными симптоматическими эпилепсиями. Согласно данным программы хирургического лечения детской эпилепсии центра UCLA (США), гистологические данные, полученные в результате более 500 операций, выполненных с 1986 г. по поводу фармакорезистентной эпилепсии, выявили, что ФКД были причиной эпилепсии более чем у 80% детей до 3 лет.
Уже на ранних этапах изучения корковых дисгенезий считалось, что ФКД представляют собой дефект нейрональной миграции, так как исследователями выявлялось наличие в гистологической структуре ФКД повреждение перивентрикулярной нейроглиальной дифференцировки вместе с гигантскими и дизморфичными нейронами.
Современные исследования указывают на задержку дегенерации клеток нервного валика и нервной пластинки вместе с усиленной пролиферацией кортикальных нейронов. Большинство клеток нервного валика дегенерируют за 4 – 6 недель до рождения плода, что совпадает по времени с повышением дифференциации коры и белого вещества. В дальнейшем, при нормальном гистогенезе, перивентрикулярные глиальные радиальные клетки прикрепляются к хвостовым отросткам корковых пирамидных нейронов и мигрируют в направлении коры, где трансформируются в протоплазматические астроциты. Это объясняет, почему баллонные клетки корковых дисплазий обладают морфологическими и иммуно-гистохимическими характеристиками клеток радиальной глии. Исследователи группы UCLA предполагают, что патогенез ФКД, таким образом, представляет собой отсутствие или нарушение поздних фаз кортикогенеза. При этом сроки нарушения кортикогенеза коррелируют со степенью тяжести дисгенезий. Нарушения, возникающие в поздней втором или раннем третьем триместре беременности ведут к развитию крайне тяжелых форм, таких как гемимегалэнцефалия, в то время как нарушения дифференциации и миграции нейронов на сроках беременности, близких к родам, ведут к формированию кортикальных дисплазий.
В настоящее время используется распространенная классификация ФКД, предложенная Palmini A. в 2004 году. Эта классификация выделяет 2 типа ФКД на основании наличия или отсутствия дизморфичных нейронов или баллонных клеток. При первом типе ФКД нет ни баллонных клеток, ни дизморфичных нейронов. При типе IA выявляются изолированные цитоархитектурные аномалии, обычно ламинарные или столбчатые. При типе IB также обнаруживают цитоархитектонические аномалии, однако, с наличием небольшого количества гигантских клеток или незрелых нейронов. Необходимо отметить, что при ФКД первого типа отсутствуют абнормальные клетки.
В тканях ФКД типа IIA выявляются дизморфичные нейроны, но отсутствуют баллонные клетки, а при ФКД типа II B обнаруживаются и дизморфия нейронов и баллонные клетки.
Существует некоторая корреляция между нейропатологическими типами ФКД, их клинической картиной и радиологическими находками. ФКД первого типа обычно клинически себя не проявляют и могут быть выявлены у 1,7 % здоровых людей. При магнитной резонансной томографии ФКД первого типа могут проявляться в виде локального утолщения коры, снижения дифференцировки серого и белого вещества, гиперинтенсивного сигнала от серого и субкортикального белого вещества на T2-взвешенных изображениях, гипоинтенсивного сигнала от субкортикального белого вещества на T1-взвешенных изображениях. ФКД второго типа чаще проявляются симптоматической эпилепсией. МРТ – признаки ФКД второго типа могут быть представлены в виде локальных зон утолщения коры, нечеткости перехода коры в белое вещество мозга, повышении сигнала на T2-взвешенных изображениях, или расширения коры с сигналом повышенной интенсивности от поверхности желудочков мозга. Однако различные находки на МРТ, ассоциированные с ФКД первого или второго типа не являются достаточным основанием для постановки диагноза в виду своей неспецифичности и всегда требуют гистологического подтверждения. Принципиальное значение имеет правильное проведение МРТ исследования. В нашей клинике разработан протокол МРТ исследования для пациентов с эпилепсией, который позволяет диагностировать любые морфологические изменения коры головного мозга, которые могут послужить причиной заболевания.
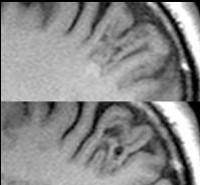
МРТ пациента с ФКД. Дисплазия указана стрелкой.
История хирургического лечения пациентов с эпилепсией и ФКД начинается с момента первого сообщения Taylor D. C. и соавторов в 1971 году, о хирургическом лечении 10 пациентов, 6 из которых продемонстрировали полное прекращение судорог после хирургии, после чего ФКД стали наиболее часто выявляемой причиной фармакорезистентных эпилепсий.
В нашем центре накоплен большой опыт хирургического лечения пациентов с симптоматическими эпилепсиями, вызванными фокальными корковыми дисплазиями. В плане прехирургической подготовки применяется МРТ высокого разрешения, функциональная МРТ для определения локализации функционально значимых зон и инвазивная кортикография для обеспечения максимально экономной и вместе с тем, эффективной хирургической резекции.
Как показал наш опыт, с применением разработанных протоколов нейровизуализации и электрофизиологического мониторинга, дисплазии могут быть идентифицированы более точно, что позволяет проводить экономные резекции с одновременным повышением частоты благоприятных результатов хирургии.
Источник
