Гуморальные факторы врожденного иммунитета белки теплового шока
Система
комплемента — это многокомпонентная
полиферментная самособирающаяся система
сывороточных белков, которые в норме
находятся в неактивном состоянии. При
появлении во внутренней среде микробных
продуктов запускается процесс, который
называют активацией комплемента.
Активация протекает по типу каскадной
реакции, когда каждый предшествующий
компонент системы активирует последующий.
В процессе самосборки системы образуются
активные продукты распада белков,
которые выполняют три важнейшие функции:
вызывают перфорацию мембран и лизис
клеток, обеспечивают опсонизацию
микроорганизмов для их дальнейшего
фагоцитоза и инициируют развитие
сосудистых реакций воспаления.
В
систему комплемента входит 9 основных
белков (обозначаемых как С1, С2-С9), а также
субкомпоненты — продукты расщепления
этих белков (Clg, С3в, С3а и т.д.), ингибиторы.
Белки
теплового шока (англ.HSP,
Heatshockproteins) —
это класс функционально сходных
белков, экспрессиякоторых
усиливается при повышении температуры
или при другихстрессирующихклетку
условиях. Повышение экспрессии генов,
кодирующих белки теплового шока,
регулируется на этапетранскрипции.
Чрезвычайное усиление экспрессии генов,
кодирующих белки теплового шока является
частью клеточного ответа на тепловой
шок и вызывается в основном фактором
теплового шока (HSFангл.heatshockfactor).Белки
теплового шока обнаружены в клетках
практически всех живых организмов,
от бактерийдочеловека.
Цитокины
Под
термином “цитокины” объединяются так
называемые ростовые факторы, которые
регулируют пролиферацию, дифференцировку
и функцию клеток крови, в том числе и
клеток иммунной системы. Это обширный
класс биохимических веществ, продуцируемый
большинством свободных клеток крови,
для общения друг с другом, через
поверхностные рецепторы на их мембранах.
Цитокины оказывают аутокринное и
паракринное воздействие.
Цитокины
можно разделить на несколько “семейств”:
интерлейкины, интерфероны,
опухольнекротизирующие факторы,
трансформирующие факторы роста, хемокины,
собственно ростовые факторы и др
Семейство
интерферонов.
Интерференция — это явление, когда ткани,
инфицированные одним вирусом, становятся
устойчивыми к заражению другим вирусом.
Было установлено, что такая резистентность
связана с продукцией зараженными
клетками особого белка, который и был
назван интерфероном.
В
настоящее время интерфероны хорошо
изучены. Они представляют собой семейство
гликопротеидов с молекулярной массой
от 15 000 до 70 000. В зависимости от источника
получения эти белки делят на интерфероны
I и II типов.
I тип
включает ИФН α и β, которые продуцируются
инфицированным вирусом клетками: ИФН-α
— лейкоцитами, ИФН-β — фибробластами. В
последние годы описаны три новых
интерферона: ИФН-τ/ε
(трофобластный ИФН), ИФН-λ и ИФН-К. В
противовирусной защите участвуют ИФН-α
и β.
Механизм
действия ИФН-α и β не связан с прямым
влиянием на вирусы. Он обусловлен
активацией в клетке ряда генов, блокирующих
репродукцию вируса. Ключевое звено —
индукция синтеза протеинкиназы R, которая
нарушает трансляцию вирусной мРНК и
запускает апоптоз зараженных клеток
через Вс1-2 и каспазазависимые реакции.
Другой механизм — это активация латентной
РНК-эндонуклеазы, которая вызывает
деструкцию вирусной нуклеиновой кислоты.
II тип
включает интерферон γ. Он продуцируется
Т-лимфоцитами и естественными киллерами
после антигенной стимуляции.
Эйкозаноиды
Эйкозаноиды
— метаболиты арахидоновой кислоты,
которая, в свою очередь освобождается
из мембранных фосфолипидов в ходе
липолиза под действием фосфолипаз. Одни
эйкозаноиды являются продуктами
циклооксигеназного пути: простагландины,
простациклин и тромбоксан, другие —
продуктами липоксигеназного пути:
лейкотриены.
Эйкозаноиды
принадлежат к классу аутокринных или
паракринных факторов. Они усиливают
или ослабляют действие других агонистов,
т.е. их относят к третьим посредникам,
к короткоживущим интермедиатам.
Простагландины
Поскольку
фосфолипиды всех клеточных мембран
содержат арахидоновую кислоту, то и все
клетки организма потенциально могут
быть источником простагландинов, и они
могут проявлять активность в самых
разных системах. Действие ПГ проявляется
чаще в тех гормоночувствительных
клетках, где вторым посредником служит
цАМФ: влияют на уровень цАМФ путем
изменения активности аденилатциклазы.
Следует подчеркнуть многофункциональность
биологических эффектов ПГ — ов, причём
простагландины групп Е и Г оказывают
противоположное действие. Основные
эффекты простагландинов
Процесс | Ткань | Эффект | |
Сокращение или | Легкие; Кровеносные сосуды | Расширение Сокращение Вазодилятация | |
Стероидогенез | Кора надпочечников | Стимуляция | |
Секреция и биосинтез | Щитовидная железа | Имитация эффекта ТТГ | |
Транспорт солей и | Почка | Повышение клиренса | |
Свертывание крови | Тромбоциты | Торможение или | |
Секреция кислоты | Слизистая желудка | Торможение | |
Липолиз | Адипоциты | Торможение | |
Простациклин
и тромбоксан обладают прямо противоположным
действием на два принципиально важных
процесса: простациклин расслабляет
гладкую мускулатуру сосудистой стенки
и тормозит агрегацию тромбоцитов;
тромбоксан, наоборот, сокращает гладкую
мускулатуру сосудов и способствует
агрегации тромбоцитов. Одним из основных
достижений в изучении простагландинов
является установление факта, что они —
важнейший компонент развития
воспалительного процесса.
Лейкотриены
Эйкозаноиды,
биосинтез которых идет по липоксигеназному
пути из арахидоновой кислоты. Три
лейкотриена: ЛТС4, ЛТД4 и
ЛТЕ4 в
совокупности являются МРВ-А ( медленно
реагирующим веществом, А-анафилаксии).
Они секретируются тучными клетками,
принимающими участие в реакциях
гиперчувствительности. Эффект компонентов
МРВ-А в 4000 раз сильнее, чем гистамина в
отношении стимуляции гладкой мускулатуры
трахеи и бронхов. Эти компоненты действуют
и на гладкую мускулатуру ЖКТ, но не столь
сильно. Они также действуют и на гладкую
мускулатуру артерий. Как и гистамин,
компоненты МРВ-А увеличивают проницаемость
сосудов.[13]
С -реактивный
белок (СРБ)
Очень
чувствительный элемент крови, быстрее
других реагирующий на повреждение
тканей. Наличие реактивного белка в
сыворотке крови — признак воспалительного
процесса, травмы, проникновения в
организм чужеродных микроорганизмов
— бактерий, паразитов, грибов. С — реактивный
белок стимулирует защитные реакции,
активирует иммунитет.
Содержание
СРБ в сыворотке крови — до 0,5 мг/л считается
нормой. Уже через 4-6 часов после того,
как в организм проникает инфекция,
развивается воспалительный процесс,
который может сопровождаться опухолями,
уровень СРБ начинает быстро расти. Чем
острее воспалительный процесс, активнее
заболевание, тем выше СРБ в сыворотке
крови. Когда заболевание в хронической
форме переходит в фазу, то содержание
СРБ в крови практически не обнаруживается.
Как наступает обострение, СРБ снова
начинает расти.
Пептиды
малой плотности
Пептиды
малой плотности (ПМП) — относятся к новому
классу регуляторных молекул, являющиеся
катионными белками, открытыми в середине
80-х годов R.Lehrer и В.Н. Кокряковым.
ПМП
обладают широким спектром прямой
противомикробной активацией, в частности
подавляют рост грамположительных и
грамотрицательных бактерий, грибов,
некоторых вирусов. В настоящее время
известны два больших класса ПМП человека:
дефензины и кателецидины. Они действуют
как эндогенные антибиотики и участвуют
в передаче сигналов клеткам, вовлечения
в процесс иммунной защиты. В основном
эти белки синтезируются эпителиальными
клетками покровных тканей и активированы.
Недавно получены данные о том, что
кателицидин LL-37 обладает прямым действием
на вирус осповакцины.[7,13]
Антимикробные
пептиды – Лизоцим.
Содержится
в сыворотке, крови, слюне, слезах и других
тканевых жидкостей человека. По
биологической природе — это полипептид,
по функциям фермент. Лизоцим действует
энзиматически на клеточную стенку
бактерий, расщепляя находящиеся в её
составе пептидогликана и мурамовой
кислоту.[4,11]
Пропердин
Пропердин
или фактор Р-белок, содержащийся в
сыворотке крови. Система пропердина
состоит из самого фактора Р и 3-х
дополнительных белков (А,В,0).
Все
они принимают участие в активации
комплемента — в расщеплении С3 компонента,
который в свою очередь обладает
выраженными антимикробными свойствами,
стимулятором фагоцитоза. Все эти
субстанции имеются в организме и не
нужно времени на их образование.[4]
Цитокины
Под
термином “цитокины” объединяются так
называемые ростовые факторы, которые
регулируют пролиферацию, дифференцировку
и функцию клеток крови, в том числе и
клеток иммунной системы. Это обширный
класс биохимических веществ, продуцируемый
большинством свободных клеток крови,
для общения друг с другом, через
поверхностные рецепторы на их мембранах.
Цитокины оказывают аутокринное и
паракринное воздействие.
Соседние файлы в предмете Иммунология
- #
- #
Источник
Система комплемента — это многокомпонентная полиферментная самособирающаяся система сывороточных белков, которые в норме находятся в неактивном состоянии. При появлении во внутренней среде микробных продуктов запускается процесс, который называют активацией комплемента. Активация протекает по типу каскадной реакции, когда каждый предшествующий компонент системы активирует последующий. В процессе самосборки системы образуются активные продукты распада белков, которые выполняют три важнейшие функции: вызывают перфорацию мембран и лизис клеток, обеспечивают опсонизацию микроорганизмов для их дальнейшего фагоцитоза и инициируют развитие сосудистых реакций воспаления.
В систему комплемента входит 9 основных белков (обозначаемых как С1, С2-С9), а также субкомпоненты — продукты расщепления этих белков (Clg, С3в, С3а и т.д.), ингибиторы.
Белки теплового шока (англ. HSP, Heat shock proteins) — это класс функционально сходных белков, экспрессия которых усиливается при повышении температуры или при других стрессирующих клетку условиях. Повышение экспрессии генов, кодирующих белки теплового шока, регулируется на этапе транскрипции. Чрезвычайное усиление экспрессии генов, кодирующих белки теплового шока является частью клеточного ответа на тепловой шок и вызывается в основном фактором теплового шока (HSF англ. heat shock factor).Белки теплового шока обнаружены в клетках практически всех живых организмов, от бактерий до человека.
Цитокины
Под термином “цитокины” объединяются так называемые ростовые факторы, которые регулируют пролиферацию, дифференцировку и функцию клеток крови, в том числе и клеток иммунной системы. Это обширный класс биохимических веществ, продуцируемый большинством свободных клеток крови, для общения друг с другом, через поверхностные рецепторы на их мембранах. Цитокины оказывают аутокринное и паракринное воздействие. Цитокины можно разделить на несколько “семейств”: интерлейкины, интерфероны, опухольнекротизирующие факторы, трансформирующие факторы роста, хемокины, собственно ростовые факторы и др
Семейство интерферонов. Интерференция — это явление, когда ткани, инфицированные одним вирусом, становятся устойчивыми к заражению другим вирусом. Было установлено, что такая резистентность связана с продукцией зараженными клетками особого белка, который и был назван интерфероном.
В настоящее время интерфероны хорошо изучены. Они представляют собой семейство гликопротеидов с молекулярной массой от 15 000 до 70 000. В зависимости от источника получения эти белки делят на интерфероны I и II типов.
I тип включает ИФН α и β, которые продуцируются инфицированным вирусом клетками: ИФН-α — лейкоцитами, ИФН-β — фибробластами. В последние годы описаны три новых интерферона: ИФН-τ/ε (трофобластный ИФН), ИФН-λ и ИФН-К. В противовирусной защите участвуют ИФН-α и β.
Механизм действия ИФН-α и β не связан с прямым влиянием на вирусы. Он обусловлен активацией в клетке ряда генов, блокирующих репродукцию вируса. Ключевое звено — индукция синтеза протеинкиназы R, которая нарушает трансляцию вирусной мРНК и запускает апоптоз зараженных клеток через Вс1-2 и каспазазависимые реакции. Другой механизм — это активация латентной РНК-эндонуклеазы, которая вызывает деструкцию вирусной нуклеиновой кислоты.
II тип включает интерферон γ. Он продуцируется Т-лимфоцитами и естественными киллерами после антигенной стимуляции.
Эйкозаноиды
Эйкозаноиды — метаболиты арахидоновой кислоты, которая, в свою очередь освобождается из мембранных фосфолипидов в ходе липолиза под действием фосфолипаз. Одни эйкозаноиды являются продуктами циклооксигеназного пути: простагландины, простациклин и тромбоксан, другие — продуктами липоксигеназного пути: лейкотриены.
Эйкозаноиды принадлежат к классу аутокринных или паракринных факторов. Они усиливают или ослабляют действие других агонистов, т.е. их относят к третьим посредникам, к короткоживущим интермедиатам.
Простагландины
Поскольку фосфолипиды всех клеточных мембран содержат арахидоновую кислоту, то и все клетки организма потенциально могут быть источником простагландинов, и они могут проявлять активность в самых разных системах. Действие ПГ проявляется чаще в тех гормоночувствительных клетках, где вторым посредником служит цАМФ: влияют на уровень цАМФ путем изменения активности аденилатциклазы. Следует подчеркнуть многофункциональность биологических эффектов ПГ — ов, причём простагландины групп Е и Г оказывают противоположное действие. Основные эффекты простагландинов
| Процесс | Ткань | Эффект | |
| Сокращение или расслабление гл. мускулатуры | Легкие; матка; ЖКТ; Кровеносные сосуды | Расширение бронхов Сокращение Вазодилятация | |
| Стероидогенез | Кора надпочечников | Стимуляция | |
| Секреция и биосинтез тириоидных гормонов | Щитовидная железа | Имитация эффекта ТТГ | |
| Транспорт солей и воды | Почка | Повышение клиренса своб. Воды | |
| Свертывание крови | Тромбоциты | Торможение или усиление агрегации | |
| Секреция кислоты | Слизистая желудка | Торможение | |
| Липолиз | Адипоциты | Торможение | |
Простациклин и тромбоксан обладают прямо противоположным действием на два принципиально важных процесса: простациклин расслабляет гладкую мускулатуру сосудистой стенки и тормозит агрегацию тромбоцитов; тромбоксан, наоборот, сокращает гладкую мускулатуру сосудов и способствует агрегации тромбоцитов. Одним из основных достижений в изучении простагландинов является установление факта, что они — важнейший компонент развития воспалительного процесса.
Лейкотриены
Эйкозаноиды, биосинтез которых идет по липоксигеназному пути из арахидоновой кислоты. Три лейкотриена: ЛТС4, ЛТД4 и ЛТЕ4 в совокупности являются МРВ-А ( медленно реагирующим веществом, А-анафилаксии). Они секретируются тучными клетками, принимающими участие в реакциях гиперчувствительности. Эффект компонентов МРВ-А в 4000 раз сильнее, чем гистамина в отношении стимуляции гладкой мускулатуры трахеи и бронхов. Эти компоненты действуют и на гладкую мускулатуру ЖКТ, но не столь сильно. Они также действуют и на гладкую мускулатуру артерий. Как и гистамин, компоненты МРВ-А увеличивают проницаемость сосудов.[13]
С -реактивный белок (СРБ)
Очень чувствительный элемент крови, быстрее других реагирующий на повреждение тканей. Наличие реактивного белка в сыворотке крови — признак воспалительного процесса, травмы, проникновения в организм чужеродных микроорганизмов — бактерий, паразитов, грибов. С — реактивный белок стимулирует защитные реакции, активирует иммунитет.
Содержание СРБ в сыворотке крови — до 0,5 мг/л считается нормой. Уже через 4-6 часов после того, как в организм проникает инфекция, развивается воспалительный процесс, который может сопровождаться опухолями, уровень СРБ начинает быстро расти. Чем острее воспалительный процесс, активнее заболевание, тем выше СРБ в сыворотке крови. Когда заболевание в хронической форме переходит в фазу, то содержание СРБ в крови практически не обнаруживается. Как наступает обострение, СРБ снова начинает расти.
Пептиды малой плотности
Пептиды малой плотности (ПМП) — относятся к новому классу регуляторных молекул, являющиеся катионными белками, открытыми в середине 80-х годов R.Lehrer и В.Н. Кокряковым.
ПМП обладают широким спектром прямой противомикробной активацией, в частности подавляют рост грамположительных и грамотрицательных бактерий, грибов, некоторых вирусов. В настоящее время известны два больших класса ПМП человека: дефензины и кателецидины. Они действуют как эндогенные антибиотики и участвуют в передаче сигналов клеткам, вовлечения в процесс иммунной защиты. В основном эти белки синтезируются эпителиальными клетками покровных тканей и активированы. Недавно получены данные о том, что кателицидин LL-37 обладает прямым действием на вирус осповакцины.[7,13]
Источник
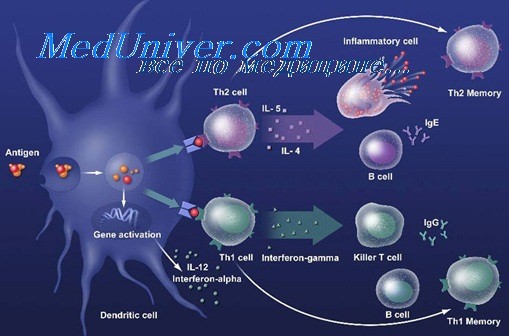
Белки теплового шока (HSPs). Эффекты врожденного иммунитета в ответ на HSPsБелки теплового шока (heat shok proteins HSPs) широко распространены в живой природе и являются одними из наиболее консервативных молекул биосферы. Основная функция HSPs — защита биологических систем от повреждающих стрессорных воздействий. В процессе эволюции эукариот некоторые HSPs приобрели функции, позволившие им интегрироваться в систему иммунитета. Белки теплового шока обеспечивают важные жизненные функции и представлены у всех живых организмов. Продукты генов, наименованные белками теплового шока или белками клеточного стресса, вырабатываемые в условиях гипертермии, изначально были идентифицированы как молекулы, вырабатываемые в ответ на присутствие в клетках белков с нарушенной конформацией. Затем было установлено, что HSPs играют роль шаперонов в нековалентной сборке и демонтаже других макромолекулярных структур, хотя сами не являются перманентными компонентами этих структур при выполнении своих биологических функций. Реакция белков теплового шока зафиксирована не только в условиях гипертермии, но также при оксидативном стрессе, ацидозе, ишемии, гипоксии-гипероксии, энергетическом истощении клеток и т п. В этих условиях HSPs высвобождаются из некротизированных клеток при разрушении ткани или лизисе инфицированных клеток. Благодаря особенности распознавания гидрофобных аминокислотных последовательностей на поверхности белков, как предупредительного сигнала о конформационной их нестабильности, HSPs способны осуществлять такие жизненно важные функции, как участие в обеспечении пространственной организации белковых молекул (фолдинге), их стабилизации, коррекции конформационных изменений (рефолдинге), транслокации белков через мембраны внутриклеточных органелл, предотвращении белковой агрегации и деградации нестабильных белков. Наряду с этим, HSPs проявляют антиапоптотическую активность. В совокупности, HSPs выполняют роль буферной системы, противодействующей стохастическим и потенциально дестабилизирующим факторам клеточного окружения. HSPs играют важную роль в индукции иммуного ответа, в особенности врожденного иммунитета: усиливают активность NK-клеток, созревание АПК и продукцию цитокинов. Пептидные фрагменты расщепляющихся белковых молекул перехватываются HSPs и, в конечном итоге, претерпевая процессинг в АПК, индуцируют реакции адаптивного иммунитета. Таким образом, через активацию АПК и участие в процессинге антигена белки теплового шока интегрируют реакции врожденного и приобретенного (адаптивного) иммунитета. Иммуностимулирующие свойства проявляют HSP про- и эукаритического происхождения. Способностью к индукции иммунного ответа обладают представители нескольких семейств HSP (кальретикулин, HSP10, HSP60, HSP70, HSP90, HSP100 и HSP170).
Шаперонная функция белков теплового шока осуществляется не только в процессе биогенеза других белков, но и при иммунном ответе на антигены. Изменение окружающей среды при инфицировании создает стрессорную ситуацию как для вторгшегося патогена, так и для клеток хозяина, что проявляется в обоюдной интенсификации синтеза и функциональной активности белков теплового шока. Молекулярные шапероны бактерий выступают в роли лигандов для рецепторов на поверхности клеток хозяина. HSPs могут быть распознаны TLR2, TLR4. Другие др96, HSP90 и HSP70, взаимодействуют с антигенпрезентирующими клетками через общий рецептор, CD91. HSP-шаперонные пептиды проникают в макрофаг/дендритные клетки через CD91, процессируются и презентируются вместе с молекулами МНС I и МНС II. Это вызывает активацию CD4 и CD8 Т-клеток. HSP-ДК взаимодействие через CD91 ведет к созреванию дендритных клеток и секреции ряда цитокинов. В результате взаимодействия рекомбинантного HSP 70 М tuberculosis с TLR-2 и TLR-4 in vitro запускается сигнальный каскад с вовлечением адапторных белков MyD88, TIRAP, TRIF и TRAM в эндотелиоцитах человека и в макрофагах мышей происходит активация фактора транскрипции NF-кВ. Представленный в эндоплазматическом ретикулуме эукариот, шаперон GRP94/gp96 через взаимодействие с TLR-2 и TLR-4 активирует дендритные клетки к инициации CD8′ Т-лимфоцитарного ответа. При этом усиливается экспрессия MICA/B молекул, взаимодействующих с NKG2D рецептором, представленным на поверхности CD8, но не СD4*Т-клеток. При взаимодействии TLR7 с HSP70, активно секретируемым, так и освобождаемым при некротической гибели клеток млекопитающих, усиливается фагоцитарная функция макрофагов. Данный эффект проявляется за несколько минут и выражается не только в стимуляции фагоцитоза, но также и функции представления антигена Т-клеткам через сигнальные пути, опосредуемые фосфоинозитид 3-киназой и р38 МАР-киназой. В осуществлении презентации антигена хелперным Т-клеткам принимают участие также зрелые В-лимфоциты, экспрессирующие TLR-2 и TLR-4. Они отвечают на LPS, пептидогликан, HSP60 повышением экспрессии МНС II и костимуляторных молекул. HSP 60 человека, но не GroEL E. coli или HSP65 М. tuberculosis индуцируют пролиферацию наивных В-клеток мышей и секрецию ими IL-6 и IL-10. На сегодняшний день многие рецепторы, распознающие паттерны известных PAMPs прокариотов, грибков, вирусов, простейших патогенов остаются еще не охарактеризованными. Существует взаимосвязь между фагоцитозом и экспрессией TLRs, поскольку активация сигналов через TLR усиливает фагоцитарные процессы, а фагоцитоз модулирует последовательность активации TLR. Является очевидным, что еще неопределенные молекулярные паттерны могут искажать или направлять адаптивный имунный ответ по Тh-2 типу Возможно, что отсутствие сигналов (например — PAMPs), подобно дефициту своих МНС I для NK-клеточной активации является стимулом для запуска иммунитета второго типа. Индукция сигналов через Toll-подобные рецепторы может обеспечивать не только защиту организма от различных инфекций. Нарушение функции проводимости данных сигналов приводит к развитию целого ряда патологических процессов в организме. Например, чрезмерная продукция провоспалительных цитокинов эндогенными лигандами может стать причиной развития хронического воспаления, аутоиммунных заболеваний, таких как болезнь Крона, диабет типа 1, атеросклероз. Изменение баланса в сторону провоспалительных цитокинов, вероятно, обусловлено развитием локальных отеков и воспалительных реакций в ЦНС инициированных провоспалительными цитокинами (TNF-a или IL-1p). В формировании длительно сохраняющихся неврологических нарушений принимают участие несколько цитокинов, которые потенцируя продукцию и действие друг друга, дольше сохраняются в циркуляции. Постоянное присутствие цитокинов поддерживает хронический воспалительный процесс в ЦНС, сопровождающийся демиелинизацией, а в ряде случаев и гибелью нейронов. — Также рекомендуем «Сигналы Toll-подобных рецепторов. Роль молекулы MyD88» Оглавление темы «Врожденный иммунитет»:
|
Источник
