Иммунитет и рак поджелудочной железы
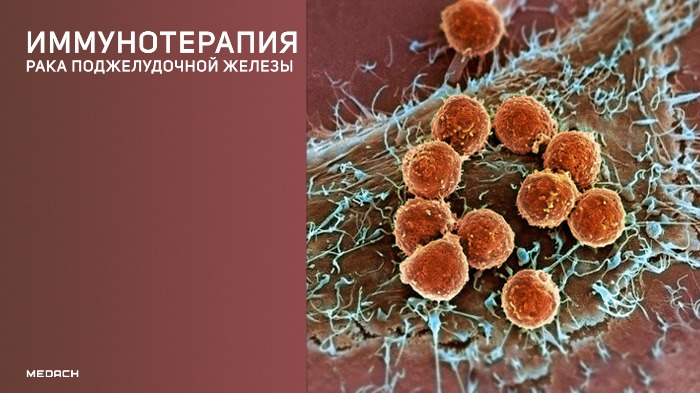
Клетки рака поджелудочной железы переваривают собственные белки, которые могут выдать их иммунной системе.
Иммунитет должен уничтожать не только вирусы с бактериями, но и злокачественные клетки. Но у злокачественных клеток есть разные уловки, которые позволяют им оставаться незаметными для иммунитета. Однако если иммунной системе, так сказать, открыть глаза, то она увидит опухоль и начнёт её истреблять. Суть иммунотерапии в том и заключается, чтобы активировать противораковые свойства иммунитета. Здесь используют разные подходы, и два иммунотерапевтических открытия даже удостоились недавно Нобелевской премии.
Т-лимфоциты, окружившие раковую клетку. (Фото: NICHD / Flickr.com)
‹
›
Но разные виды рака по-разному реагируют на иммунотерапию, и рак поджелудочной железы в этом смысле один из самых стойких. Он не реагирует как раз на «нобелевские « методы терапии, основанные на том, что у иммунитета в прямом смысле отключают тормоза.
У иммунной системы есть предохранители, клетки и молекулы, которые следят, чтобы защитная реакция была по делу и адекватна угрозе – чтобы иммунитет не впадал в агрессию без повода и чтобы иммунная активность утихала по мере исчезновения опасности. В число таких предохранителей входят белки PD-1 и CTLA-4, сидящие на поверхности Т-лимфоцитов, которые обычно уничтожают больные клетки, в том числе и раковые.
PD-1 и CTLA-4 успокаивают Т-лимфоциты, то есть если PD-1 и CTLA-4 активны, Т-лимфоциты никого не убивают. Раковые клетки как раз поддерживают PD-1 и CTLA-4 во включённом состоянии, так что иммунитет опухоль игнорирует. Но если отключить PD-1 и CTLA-4 – иными словами, сорвать лимфоцитам тормоза – то иммунная система начнёт охотиться на раковые клетки.
Но и Т-лимфоциты с сорванными тормозами всё равно почему-то не трогают клетки рака поджелудочной железы. Тут может быть несколько причин. Во-первых, активность иммунных клеток зависит не только от этих двух белков. И в самой раковой опухоли могут быть какие-то другие клетки, которые усыпляют бдительность Т-лимфоцитов, используя какие-то другие клеточно-молекулярные механизмы. Во-вторых, собственно у раковых клеток могут быть особенности, из-за которых лимфоциты просто не могут их обнаружить.
Почему иммунные клетки начинают атаковать раковые? Потому что иммунные клетки чувствуют на поверхности раковых клеток особые молекулы, которые выдают раковые клетки с головой. Но особые раковые молекулы не появляются на поверхности клеток просто так. На днях мы писали о белках главного комплекса гистосовместимости (MHC), или человеческих лейкоцитарных антигенах (HLA), которые служат чем-то вроде клеточного паспорта: они сидят на клеточной мембране и держат на себе обломки разных клеточных белков.
Иммунные клетки проверяют, что держат на себе белки MHC: если они держат обломки обычных клеточных белков, то клетка здорова и трогать её не надо; если же они держат обломки вирусных или бактериальных молекул, то клетка инфицирована и её нужно уничтожить. И если белки MHC держат обломки других белков, которые присущи раковым клеткам, то такую клетку тоже нужно уничтожить.
Говорят, что белки MHC занимаются презентацией антигенов – молекул, на которые иммунная система может отреагировать. И если в генах MHC случается мутация, то они уже не могут показывать иммунным клеткам разные антигены, или показывают их плохо. Некоторые раковые клетки спасаются от иммунитета как раз благодаря тому, что в генах MHC у них мутированы.
Но рак поджелудочной железы в этом смысле особенный: мутации в генах MHC у него встречаются не более чем в 1% случаев, и одновременно в клетках рака поджелудочной в более чем 60% случаев уровень MHC ниже должного, или же MHC вовсе отсутствуют (что особенно заметно у метастазных клеток).
Исследователи из Нью-Йоркского университета пишут в Nature, что клетки рака поджелудочной избавляются от белков MHC с помощью важного клеточного процесса под названием аутофагия. С помощью аутофагии клетка переваривает ставшие ненужными белки и целые органеллы, чтобы из их запчастей снова сделать что-нибудь полезное (кстати, за расшифровку механизма аутофагии тоже дали Нобелевскую премию несколько лет назад). То, что нужно переварить, расщепить, разобрать на части, метится специальной меткой, после чего помеченный мусор упаковывается в мембранный пузырёк – аутофагосому; потом аутофагосома сливается с другим мембранным пузырьком – лизосомой, которой содержатся расщепляющие ферменты.
И вот оказалось, что у клеток рака поджелудочной железы мало белков MHC на поверхности – зато много белков MHC в аутофагосомах, «самопереваривательных пузырьках». Удалось также найти белок-рецептор, который отправляет MHC-белки на расщепление. Аутофагию можно подавить либо генетической инженерией, либо некоторыми веществами (например, хлорохином, который сейчас бурно обсуждают как одно из средств против коронавируса SARS-CoV-2).
Если у подопытных мышей с раком поджелудочной аутофагию каким-то образом подавляли, то у мышей активировались Т-лимфоциты, задача которых была в истреблении раковых клеток – эти Т-лимфоциты массово приходили в опухоль, а если мышам ещё и давали иммунотерапевтические препараты, то болезнь у животных заметно отступала.
На самом деле, как пишет портал Nature, специалисты давно знали о том, что для рака поджелудочной железы аутофагия очень и очень важна; неясно было только, чем именно аутофагия так полезна именно раковым клеткам. Также сравнительно давно блокируют одну из стадий аутофагии; оба вещества, которые уже не одно десятилетие используют как средство от малярии, испытывали против злокачественных опухолей, но результаты тогда получались не слишком выдающиеся.
Возможно, что после новых данных интерес к противораковым свойствам хлорохина снова воскреснет, и рак поджелудочной железы можно будет успешно лечить иммунотерапевтическими методами, усиленными этим противомалярийным средством или же его аналогом.
Источник

Рак поджелудочной железы (РПЖЖ) — это одно из самых смертельных заболеваний среди солидных опухолей. Ежегодно регистрируется более 250000 смертей от рака поджелудочной железы. Он является восьмой по частоте причиной смерти от злокачественных новообразований у мужчин и женщин во всем мире, а заболеваемость РПЖЖ варьируется от 1 до 10 случаев на 100000 человек. Проблема рака поджелудочной железы актуальна в современной медицине, так как большинство пациентов с локальным или метастатическим РПЖЖ не являются кандидатами на лечебную резекцию из-за чрезвычайно неблагоприятного прогноза.
Несмотря на огромный прогресс в лечении других злокачественных опухолей благодаря прорыву в иммунотерапии рака, лечение рака поджелудочной железы развивалось медленно в течение последних двух десятилетий. Неэффективность иммунотерапии РПЖЖ объясняется несколькими факторами, в том числе слабой иммуногенностью опухоли (мутантные белки, экспрессируемые на поверхности опухолевых клеток РПЖЖ, обладают слабыми антигенными свойствами, по сравнению, к примеру, с антигенами меланомы или рака легкого), а также наличием иммуносупрессивных свойств как у самой опухоли, так и у ее микроокружения. Не последнюю роль в резистентности к терапии играет десмопластическая строма опухоли, состоящая из фибробластов, клеток поджелудочной железы, иммунных клеток, кровеносных сосудов и белков внеклеточного матрикса. Помимо уже упомянутых иммуносупрессивных свойств, она играет роль физического барьера, препятствующего доставке терапевтических агентов к опухолевым клеткам. Взаимодействие опухолевых клеток с микроокружением может приводить как к усилению роста опухоли и подавлению иммунного ответа на нее, так и к нарушению ее развития, что делает опухолевое микроокружение хорошей целью для терапевтического воздействия. Совокупностью этих факторов обосновывается неэффективность традиционной иммунотерапии. Это поднимает необходимость разработки и внедрения новых, улучшенных способов лечения РПЖЖ с помощью различных иммунологических методик, а также подготовки комбинированных схем терапии с применением различных препаратов или иных методов (например, лучевая терапия).
Устранение иммуносупрессивных свойств опухолей — это один из зарекомендовавших себя подходов в иммунотерапии рака. Ингибирование иммуносупрессивных молекул CTLA-4 и PD-1 — неплохой метод, который проявил себя в лечении таких видов рака как меланома, уротелиальная карцинома, рак почки, гепатоцеллюлярный рак и др. CTLA-4 (цитотоксический лимфоцитарный антиген 4) представляет собой ингибирующий рецептор, локализующийся на CD4+ и CD8+ лимфоцитах. Его экспрессия повышена в опухолях, и было показано, что блокада CTLA-4 вызывает противоопухолевый иммунный ответ. Препарат ипилимумаб — это человеческое моноклональное антитело, нацеленное на CTLA-4. Однако несмотря на его эффективность в терапии других опухолей, клинические испытания ипилимумаба в терапии РПЖЖ не показали эффективных результатов. Другой супрессивной молекулой является programming death 1 (PD-1, рецептор запрограммированной смерти 1). Он экспрессируется на эффекторных Т-лимфоцитах, B-лимфоцитах, NK-клетках и Treg. При связывании со своим лигандом PD-1L этот рецептор активирует ингибирование активации и пролиферации лимфоцитов. Терапия моноклональными антителами против PD-1 (препараты пембролизумаб и ниволумаб) также была эффективна при лечении солидных опухолей, таких как меланома, рак почки и урогенитальная карцинома. Также применяются моноклональные антитела против PD-1L (атезолизумаб). Однако клинические испытания на РПЖЖ не показали эффективности данных методов.
Другим подходом к лечению злокачественных новообразований является стимуляция собственного иммунитета организма пациента с помощью противоопухолевых вакцин. Такие вакцины предназначены для увеличения представления опухолевых антигенов и активации антигенспецифичных эффекторных Т-лимфоцитов и Т-клеток памяти. Выявлено несколько антигенов, которые экспрессируются в большинстве опухолей поджелудочной железы, как например карциноэмбриональный антиген (СЕА), муцин-1 (MUC-1) и белок, кодируемый мутированным геном KRAS. В настоящее время несколько вакцин были испытаны для терапии РПЖЖ. GVAX — это клеточная вакцина, в которой модифицированные клетки рака поджелудочной железы экспрессируют гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF). Фаза I клинических испытаний показала безопасность данной вакцины, однако эффект от терапии был неоднозначный. Несмотря на то, что не было выявлено улучшения однолетней и общей выживаемости в группах пациентов, получавших данную вакцину в сочетании с химиолучевой терапией, и пациентов, получавших только адъювантную лучевую терапию, подгруппа пациентов с длительной безрецидивной выживаемостью показала увеличение опухолеспецифичных CD8+ Т-лимфоцитов после вакцинации. Это демонстрирует, что данная методика может использоваться в отношении некоторой группы пациентов. Другой тип вакцин, на основе опухолевых пептидов, также был исследован. Вакцина на основе мутантного белка KRAS, который мутирует больше чем в 90 % случаев РПЖЖ, давала появление иммунного ответа у 58 % пациентов, причем медиана выживаемости среди таких пациентов была в два раза выше, чем у группы, не развивших иммунный ответ. Другая мультипептидная вакцина OCV-C01, содержащая фрагменты рецептора фактора роста эндотелия сосудов 1 и 2 (VEGFR1 и VEGFR2 соответственно), а также белка семейства кинезина (KIF20A), была исследована на пациентах с РПЖЖ. 58,6 % испытуемых показали развитие иммунного ответа на KIF20A, что сопровождалось значительным улучшением безрецидивной выживаемости. Данные результаты свидетельствуют о перспективности использования противоопухолевых вакцин и необходимости установления новых антигенных детерминант, более специфичных для РПЖЖ.
Хорошие результаты вакцин и важность иммуносупрессивных свойств микроокружения опухоли для успешной терапии дают обоснования для комбинирования данных методик в терапии РПЖЖ. Клиническое исследование комбинированной терапии ипилимумабом и вакциной GVAX показало эффективность данного подхода, по сравнению с монотерапией ипилимумабом, а также безопасность данного сочетания препаратов. Эффективной оказалась и комбинация GVAX с ингибиторами PD-1, которая демонстрировала значительное увеличение средней общей выживаемости по сравнению с монотерапией. В группе пациентов, получавших оба препарата, обнаруживалось увеличение CD8+ T-лимфоцитов, продуцирующих IFN-gamma. Было показано, что пациенты, получавшие GVAX за 2 недели до резекции опухоли, демонстрировали увеличение уровня PD-L1, что указывает на один из механизмов иммунорезистентности. Таким образом, комбинация вакцин и ингибиторов иммуносупрессивных молекул является обоснованной и перспективной схемой терапии, требующей дальнейших исследований.
Новым подходом к лечению РПЖЖ являются методики, воздействующие на определенный компоненты стромы рака поджелудочной железы, о роли которой в резистентности к терапии было упомянуто ранее. Мезенхимальная строма РПЖЖ содержит большое количество фибробластов, продуцирующих белок-α активирующий фибробласты (FAP-α). Высокая экспрессия этого белка коррелирует с худшим прогнозом заболевания. В эксперименте на мышах ликвидация клеток, экспрессирующих FAP-α, повышала эффективность противоопухолевых вакцин. Эффективными оказались и комбинации данной методики с анти-CTLA-4 и анти-PD-L1 препаратами. Другое исследование было направлено на блокаду рецептора колониестимулирующего фактора 1 (CSF1R), который экспрессируется на ассоциированных с опухолью М2-макрофагах и супрессорных миелоидных клетках (MDSC). Данные клетки обладают способностью блокировать цитотоксический иммунный ответ. Ингибирование CSF1R в сочетании с химиотерапией улучшает противоопухолевый иммунитет. В мышиной модели трансплантации РПЖЖ лечение ингибиторами CSF1R приводило к усилению инфильтрации опухоли Т-клетками, однако эти клетки демонстрировали повышенные уровни CTLA-4, а также наблюдалось усиление экспрессии PD-L1 в опухоле. Этот факт делает обоснованным сочетание ингибиторов CSF1R и анти-CTLA-4, анти-PD-L1 препаратов. IMC-CS4 является CSF1R-антителом, которое в настоящее время проходит клинические испытания в сочетании с GVAX и анти-PD1 терапией. Еще одна важная молекула, а точнее пара молекул, была исследована в качестве мишени для терапии РПЖЖ. Хемокин CXCL12 широко представлен в микроокружении опухоли, а его рецептор CXCR4 экспрессирован на опухолевых клетках. Показано, что CXCL12 способствует хемотаксису опухолевых клеток, что указывает на перекрестное клеточное взаимодействие между опухолевыми клетками и стромой. Это взаимодействие оказалось значимым для иммунорезистентности РПЖЖ, так как при обработке опухоли AMD3100 моноклональным антителом к CXCR4, регистрировалось снижение роста опухоли, зависимое от Т-лимфоцитов. Комбинация AMD3100 с анти-PD-L1 препаратом также оказалась эффективной. На данный момент AMD3100 находится в I фазе клинических испытаний в качестве терапии РПЖЖ под торговым названием Мозобил (Mozobil). Помимо ингибирующих агентов моноклональные антитела могут использоваться и как агонисты различных рецепторов. CD40 является молекулой, располагающейся на поверхности иммунных клеток. При связывании со своим лигандом CD40L (который экспрессирован на CD4+ Т-хелперных клетках) активирует антигенпредставляющие клетки. Было продемонстрировано, что усиление действия CD40 повышает эффективность противоопухолевых вакцин. Моноклональные антитела, активирующие CD40, приводили к регрессии опухоли в сочетании с химиотерапией в доклинических исследованиях. В клинических испытаниях I фазы терапия агонистом CD40 в сочетании с химиотерапией привела к иммунному противоопухолевому ответу в 19 % случаев у пациентов с неоперабельной формой РПЖЖ. В мышиных моделях, сочетание анти-PD-1 или анти-CTLA-4 препаратов с агонистами CD40 усиливало противоопухолевый иммунитет. 39 % мышей, получавших подобную схему терапии, демонстрировали длительную полную ремиссию и продолжительную выживаемость. Также терапия привела к уменьшению Treg и увеличению CD8+ Т-лимфоцитов в микроокружении опухоли. Важно, что в экспериментах на мышах сочетание CD40 агонистов с анти-PD-1 или анти-CTLA-4 препаратами показало улучшенную среднюю выживаемость по сравнению с комбинацией химиотерапии и CD40 агониста. На данный момент моноклональное антитело-агонист CD40 R07009789 проходит клинические испытания в комбинации с химиотерапией и ингибиторами супрессорных молекул.
Таким образом, рак поджелудочной железы является важной проблемой в современной медицине. Традиционные подходы иммунотерапии, такие как ингибиторы иммуносупрессивных молекул и противоопухолевые вакцины, малоэффективны в качестве монотерапии при РПЖЖ. В то же время, комбинации специальных препаратов, воздействующих на компоненты микроокружения опухоли с традиционной иммунотерапией и химиотерапией показали многообещающие результаты. Требуется дальнейшее всестороннее изучение данного злокачественного новообразования для разработки эффективных методов лечения, в том числе и иммунотерапии.
Источники:
- Torphy R. J., Zhu Y., Schulick R. D. Immunotherapy for pancreatic cancer: Barriers and breakthroughs //Annals of Gastroenterological Surgery. — 2018.
- Bhosale R. R. et al. Current Perspectives on Novel Drug Carrier Systems and Therapies for Management of Pancreatic Cancer: An Updated Inclusive Review // Critical Reviews™ in Therapeutic Drug Carrier Systems. — 2018. — Т. 35. — №. 3.
Источник
Лечение
Сегодня многие исследования сосредоточены на поиске наиболее оптимальной схемы лечения рака поджелудочной железы. Совершенствование методов хирургической и лучевой терапии сейчас стали главной целью, которая определит наилучшую комбинацию лечения людей на разных стадиях рака. Лечение зависит и от локализации опухоли и от стадии процесса. Хирургическое удаление опухоли и всех раковых клеток самая главная задача лечения. Если же этого достичь невозможно, все силы бросаются на замедление роста опухоли и предотвращение ее дальнейшей прогрессии.
Митоз
Хирургическое лечение
Операция по удалению злокачественной опухоли (чаще всего это операция Уиппла) довольно продолжительная и сложная, ее тяжело переносят как пациенты, так и хирурги. Часто она требует длительного послеоперационного ухода. Новейший подход сегодня – это проведение лапароскопической операции.
Радиотерапия
Некоторые исследования направлены на поиск новых подходов в радиотерапии. Среди них, например, интраоперационная радиотерапия, при которой опухоль облучают изолированной высокой дозой радиации во время операции, и протонная терапия, при которой используется специальный тип радиации, который меньше повреждает окружающие опухоль ткани.
Химиотерапия
Сейчас в клинических испытаниях тестируется большое количество новых комбинаций препаратов для химиотерапии. Проверяют влияет ли комбинация гемцитабина с другими препаратами на продолжительность жизни. Также тестируются и совершенно новые химиопрепараты, как в отдельности, так и в комбинации с уже проверенными.
Таргетная терапия
Таргетные препараты работают несколько по-другому принципу нежели чем стандартные химиопрепараты: они нацелены на определенную молекулу раковых клеток — мишень. Таргетная терапия может показать свою эффективность наряду с существующими препаратами или даже оказаться гораздо эффективнее последних. Как минимум уже сегодня ясно, что при таргетной терапии возникает меньше побочных эффектов.
Механизм таргетной терапии
Механизм таргетной терапии
Механизм таргетной терапии
Ингибиторы факторов роста
Множество типов клеток, включая клетки панкреатических опухолей, на своих мембранах имеют рецепторы, которые помогает им расти — рецепторы факторов роста. Например, рецептор эпидермального фактора роста (РЭФР). Сейчас исследуют несколько лекарственных препаратов, которые в качестве мишени используют этот рецептор. Он блокирует рецептор и злокачественная клетка уже не воспринимает стимулы для роста. Один из таких препаратов, известный как ерлотиниб, уже одобрен для использования наряду с гемцитабином.
Антиангиогенные факторы
Все опухоли зависят от новообразованных кровеносных сосудов, которые «подпитывают» их рост. Ученые разработали специальные антиангиогенные препараты, которые блокируют рост этих сосудов и тем самым заставляют опухоль «голодать».
Лекарства нацеленные на опухолевое окружение
При раке поджелудочной химиотерапия не всегда выход. Отчасти это благодаря свойствам самих раковых клеток. Другая причина в плотной соединительной ткани поддерживающей и питающей опухоль – строме, которая формирует что-то вроде барьера, защищающего раковые клетки от химиопрепаратов. В настоящее время исследователи тестируют лекарства, такие как PEGPH20, которые атакуют строму и помогают ее разрушить. Это добавит эффективности в лечение как химией, так и другими медикаментами.
Препараты, нацеленные на стволовые клетки опухоли
Одна из теорий касательно рака поджелудочной гласит, что этот вид рака так трудно лечится потому что не все клетки в опухоли однотипные. Возможно среди них есть небольшая группа так называемых, стволовых клеток, которая запускает опухолевый рост и устойчива к химии. Т.е. даже если другие клетки погибли, эти стволовые клетки дадут старт новой опухоли в том же месте. Препараты, которые предположительно нацелены на такого рода клетки, такие как BBI-608 и демцизумаб, тестируются в комбинации с химией, и первые результаты довольно многообещающие.
Иммунотерапия
При иммунотерапии либо стимулируют иммунную систему пациента либо вводят уже готовые компоненты иммунной системы, которые «обучены» атаковать раковые клетки.
Препараты, направленные на контрольные точки иммунной системы
В норме иммунная система защищает от самой себя нормальные здоровые клетки с помощью «контрольных точек» — молекул иммунной системы, которые нужно активировать (или инактивировать) чтобы запустить иммунный ответ. Опухолевые клетки находят способы использовать эти контрольные точки, чтобы «обмануть» иммунитет и «спрятаться» от иммунной системы, поэтому она опухоль не трогает. Новейшие препараты, направленные на контрольные точки оказались очень полезными в лечении некоторых типов опухолей. И некоторые из них сегодня тестируются в лечении рака поджелудочной.
Моноклональные антитела
Одна из форм иммунотерапии заключается во введении пациенту человеческих моноклональных антител. Эти белки иммунной системы фокусируются на определенных молекулах, например, эмбриональном опухолевом антигене, который обнаруживается на поверхности опухолевых клеток. К антителам крепятся токсины или радиоактивные атомы, которые доставляются прямо к опухолевым клеткам. Ученые надеются, что они будут повреждать только опухолевые клетки и не затронут нормальные. Пока что использование этих антител доступно только в рамках клинических исследований.
Вакцины от рака
Несколько типов противораковых вакцин для стимуляции иммунного ответа, направленного на опухоль, также все еще тестируются в клинических испытаниях. В отличии от вакцин против инфекционных заболеваний, таких как паротит или корь, эти вакцины созданы для лечения рака поджелудочной, а не его предотвращения. Основное преимущество этих вакцин в том, что у них очень мало побочных эффектов.
Еще по теме:
Спасибо за дочитывание!
Источник
