Иммунитет по типу антигенов
Внешние и внутренние факторы меняют клеточные циклы здорового человека. В результате образуются аномальные (чужеродные, или синтезированные не так, как свои собственные) молекулы и клетки. Специальные клетки крови и других тканей продуцируют и поддерживают достаточную концентрацию фиксированных на клетках и свободных молекул, которые распознают, связывают (преобразуют) и выводят из организма аномальные молекулы и клетки.
Перераспределение частиц и клеток, «иммунного надзора» во все ткани организма происходит через крово- и лимфоток, а также транспорт через гистогематические барьеры.
Иммунитет (от лат. immunis) дословно означает свободный от чего- либо. Организм здорового человека непрерывно освобождается от веществ и структур, в том числе болезнетворных, как попадающих в него извне, так и образующихся внутри организма.
Источниками внешних (экзогенных) веществ и структур являются компоненты пищи, химические примеси воздуха и капельки жидкости, микроорганизмы, попадающие на кожу, в легкие, ЖКТ. Эндогенными (возникающими в самом организме) веществами, нарушающими постоянство внутренней среды и выводимыми с помощью иммунных механизмов, являются аномальные (мутантные) клетки и их компоненты, появившиеся при делении клеток, внутриклеточном синтезе веществ, метаболиты (шлаки) и др.
Тело человека состоит примерно из 1012-1013генотипически похожих клеток. Если принять, что при делении клеток каждая миллионная клетка подвергается мутации, то в любой момент в организме человека есть примерно 10 млн. аномальных клеток.
Благодаря иммунитету организм опознает, связывает, разрушает и выводит вещества и структуры. Вещества, отличающиеся по происхождению от собственных структур, называют чужеродными.
Иммунитет — способность специальных клеток жидкостей организма опознавать, связывать и удалять (выводить) вещества и структуры, происходящие из клеток других организмов или потерявших сходство с клетками собственного тела.
Иммунитет поддерживает жизнедеятельность организма путем выведения изношенных клеток, белков (гемоглобин, др.), шлаков, возобновления специфических для организма белков, клеток, в том числе клеток крови определенной группы, сохранения чужеродного плода во время беременности, и др. Поэтому понятие иммунитет шире способности защищаться от инфекции. Хотя значение инфекции очевидно: около 50% здоровых людей является носителями болезнетворных микроорганизмов.
Таким образом, иммунитет поддерживает определенные (молекулярные) показатели гомеостаза и, значит, здоровья человека: динамическое равновесие количества удаляемых и восстанавливаемых клеток, тканей и жидкостей тела.
Эти показатели гомеостаза включают не только постоянство жидких сред организма, но и нормальную жизнедеятельность клеток, дифференцировку клеток, скорость образования клеточных клонов, продолжительность жизни клеток и др. Показатели гомеостаза, в том числе количество клеток каждого типа, как и размеры органов зависят от характера жизнедеятельности.
Раздражителями для органов иммунной системы являются антигены — сложные химические вещества, микроорганизмы, появляющиеся в результате деления аномальные клетки или их компоненты.
Эти антигенные воздействия вызывают ответы «органов» иммунной системы — костного мозга, тимуса, селезенки, пейеровых бляшек стенки кишечника, лимфоузлов, лимфатических сосудов и др. Степень активности органов иммунной системы, вызванная воздействием внутренних и внешних антигенов, описывается как состояние — иммунный статус человека, или иммунитет. Условно выделяют клеточные и гуморальные показатели степени активности иммунных органов.
Человек остается здоровым до тех пор, пока не нарушается динамическое равновесие между антигенным воздействием и активностью иммунной системы. Поэтому иммунная система — понятие не столько морфологическое, сколько функциональное.
Врожденный иммунитет — образованная во внутриутробной жизни способность клеток синтезировать мембранные рецепторы к антигенам других организмов, других тканей и некоторым микроорганизмам, а также синтезировать соответствующие антитела и выводить их в жидкости тела.
Приобретенный иммунитет — образованная во внеутробной жизни способность клеток синтезировать мембранные рецепторы к экзогенным антигенам. В общем приобретенный иммунитет менее устойчив, чем врожденный.
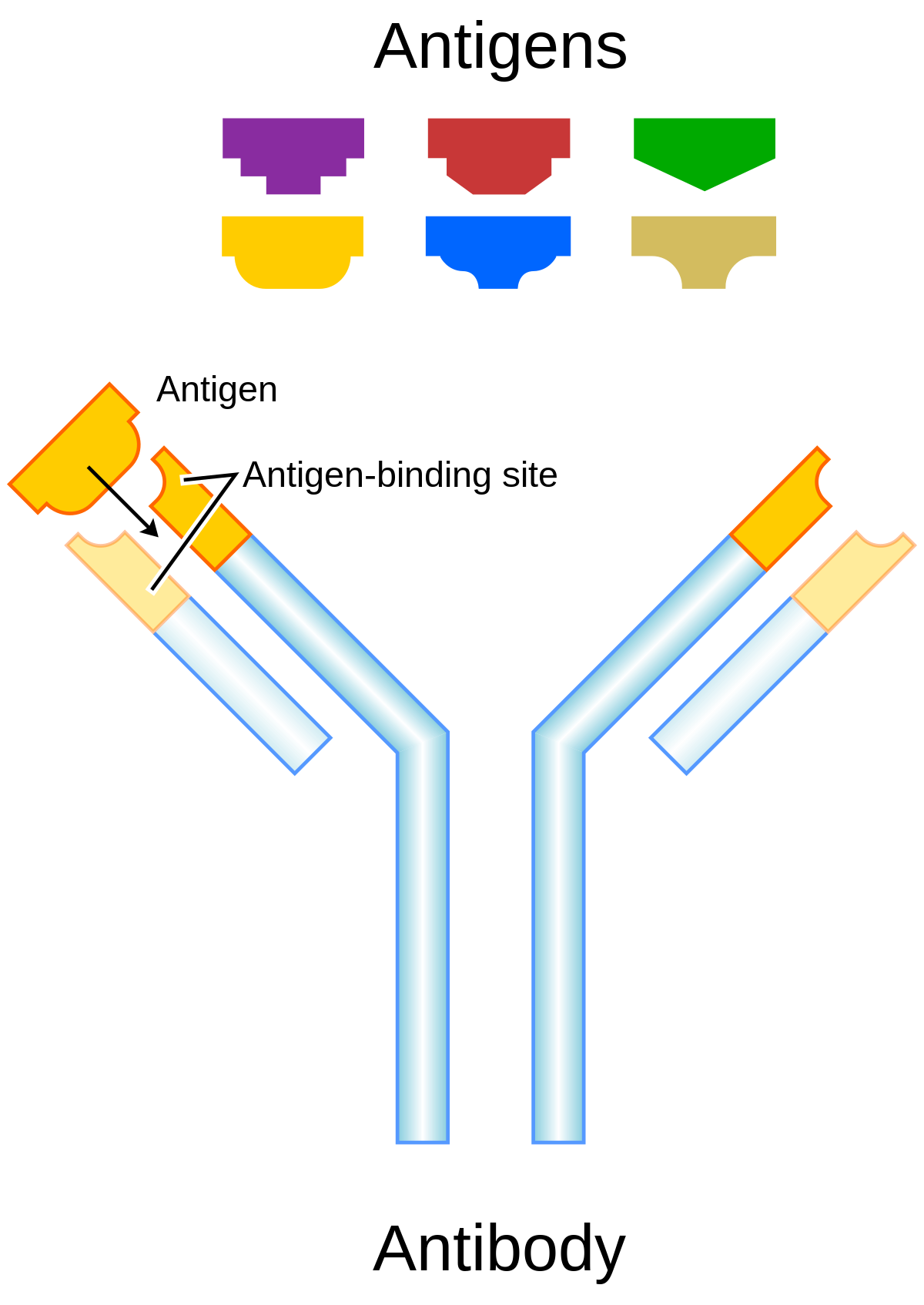
Антигены — это макромолекулярные соединения с жесткой структурой, вызывающие иммунный ответ организма
Макромолекулы, отличающиеся по происхождению и строению от основной массы меток организма и вызывающие иммунный ответ, называют антигенами (АГ). АГ поступают извне (пищевые, микробные, бытовые) или образуются внутри (эндогенные) организма. Антигенность вещества относительна: она зависит от способности клеток и находящихся в жидкостях тела веществ распознавать АГ. Антигенность молекул может усиливаться или ослабевать в случае соединения их с другими. Антигенны клетки плода по отношению к матери, сперма относительно слизистой влагалища, кровь одного человека относительно другого.
Иммунная система реагирует на химические вещества различно: легче связывает такие, к которым имеет специальные молекулы- рецепторы. Такие вещества называют антигенами. Другие вещества реагируют с иммунными соединениями и могут разрушать их.
Значит, антигены (греч, ага -против, gennao- создавать) — это воспринимаемые иммунной системой химические раздражители (адекватные), вызывающие иммунные реакции.
Антигенность, т.е. способность вызывать иммунный ответ, приобретается в ходе внутриутробного или внеутробного развития человека.
Главным свойством антигена является его чужеродность, т.е. особенности молекулы, образованные иным, непохожим на собственный, набором синтезирующих ферментов. Антигенная чужеродность проявляется в перестройке внутриклеточного синтеза. Для предотвращения этого антиген разрушается с помощью иммунной системы.
В отличие от химической реакции, взаимодействие антигена с антителом происходит не со всеми однотипными молекулами, а только с той их частью, которая имеет соответствующие детерминанте активные центры. Поэтому антигенность имеет свойство иммунной избирательности.
Аномальные клетки имеют на своих мембранах образованные с участием вируса антигены Т (англ.tumor — опухоль). Узнавание Т- антигенов таких клеток рецепторами (антителами) цитотоксических Т-лимфоцитов (Тц- тимус-зависимые цитотоксические лимфоциты) и связывание тех и других клеток приводит к разрушению и выведению из организма аномальных клеток.
Антигены групп крови представляют собой олигосахариды, связанные с белками поверхности мембран клеток крови. В настоящее время известно более 160 различных антигенов, образующих свыше 20 групп крови. Наиболее распространена АВНО (О) система групповой принадлежности крови. Антигены данной системы объединены в 3 вида: 1) гликофосфолипиды и гликопротеины на поверхности эритроцитов и других клеток, 2) олигосахариды молока и мочи и 3) олигосахариды, связанные с муцинами, секретируемыми желудочно-кишечным, мочевыделительным и дыхательным трактами.
Антигенными свойствами обладают клетки и жидкости плода по отношению к матери. Иммунный ответ здоровой беременной женщины не развивается вследствие специфического его подавления.
Резкое повышение чувствительности иммунной системы проявляется, в частности, в виде аллергической реакции. Антигены, чувствительность к которым значительно усилена и которые вызывают аллергическую реакцию, названы аллергенами (греч. allos — иной. ergen — действие).
Пищевые аллергены вызывают усиленный иммунный ответ не столько благодаря своей природе (наиболее часто аллергическую реакцию вызывают лактоглобулин коровьего молока, казеин, белки крабов, раков и др.), сколько снижением иммунных свойств кишечной стенки.
По источнику антигены делят на эндогенные и экзогенные. Эндогенными антигенами являются аномальные клетки и их компоненты, а также эмбрион для матери. Экзогенными антигенами являются попадающие на поверхность и слизистые оболочки, а также в ЖКТ белковые и полисахаридные вещества пищи, пыли, жидкости, воздуха, а также микроорганизмов.
Пищевые и другие экзогенные антигены изменяют иммунный статус человека. Так, круглые черви — аскариды, трихинеллы, др., попадающие в пищеварительный канал, подавляют иммунитет. Амебы, токсоплазма, giardia, др., попадая в пищеварительный канал, могут как подавлять, так и усиливать иммунный ответ.
Имеют свою флору и наружные половые органы. Несовместимость антигенных свойств, обусловленных различием микрофлоры половых органов супругов, может быть причиной бесплодного брака (10-25% бесплодия). Бытовые аллергены входят в состав пыли (нитраты, смолы, лаки, биологические частицы, др.), косметических средств, покрытий мебели, стен, красок для одежды, обуви и т.д.
Источник
Антиген (англ. antigen[1] от antibody-generator — «производитель антител») — любое вещество, которое организм рассматривает как чужеродное или потенциально опасное и против которого организм обычно начинает вырабатывать собственные антитела (иммунный ответ). Обычно в качестве антигенов выступают белки, однако простые вещества, даже металлы, также могут становиться антигенами в сочетании с собственными белками организма и их модификациями (гаптены)[2]
С точки зрения биохимии, антиген — любая молекула, специфично связывающаяся с антителом. По отношению к организму антигены могут быть как внешнего, так и внутреннего происхождения. Хотя все антигены могут связываться с антителами, не все они могут вызвать массовую выработку этих антител организмом, то есть иммунный ответ. Антиген, способный вызывать иммунный ответ организма, называют иммуногеном[3].
Антигены, как правило, являются белками или полисахаридами и представляют собой части бактериальных клеток, вирусов и других микроорганизмов. Липиды и нуклеиновые кислоты, как правило, проявляют иммуногенные свойства только в комплексе с белками. Простые вещества, даже металлы, также могут вызывать выработку специфичных антител, если они находятся в комплексе c белком-носителем. Такие вещества называют гаптенами.
К антигенам немикробного происхождения относятся пыльца, яичный белок и белки трансплантатов тканей и органов, а также поверхностные белки клеток крови при гемотрансфузии.
Аллергены — это антигены, вызывающие аллергические реакции.
Вещество оказывается в роли антигена, когда объединяется в комплекс с белками главного комплекса гистосовместимости (англ. MHC) внутри антигенпрезентирующих клеток, и располагается на их поверхности для презентации в качестве антигена другим имунным клеткам. В зависимости от предъявляемого антигена и от типа молекулы комплекса гистосовместимости, активируются разные виды клеток иммунной системы[3]. В частности, могут дифференцироваться B-лимфоциты, способные производить специализированные антитела для распознавания именно этого антигена, чтоб организм мог впредь распознавать этот антиген и в свободном виде.
Классификация[править | править код]
В зависимости от происхождения, антигены классифицируют на экзогенные, эндогенные и аутоантигены.
Экзогенные антигены[править | править код]
Экзогенные антигены попадают в организм из окружающей среды, путём вдыхания, проглатывания или инъекции. Такие антигены попадают в антигенпредставляющие клетки путём фагоцитоза или пиноцитоза и затем процессируются на фрагменты. Антиген-представляющие клетки затем на своей поверхности презентируют фрагменты Т-хелперам (CD4+) через молекулы главного комплекса гистосовместимости второго типа (MHC II).
Эндогенные антигены[править | править код]
Эндогенные антигены образуются клетками организма в ходе естественного метаболизма или в результате вирусной или внутриклеточной бактериальной инфекции. Фрагменты далее презентируются на поверхности клетки в комплексе с белками главного комплекса гистосовместимости первого типа MHC I. В случае, если презентированные антигены распознаются цитотоксическими лимфоцитами (CTL, CD8+), Т-клетки секретируют различные токсины, которые вызывают апоптоз или лизис инфицированной клетки. Для того, чтобы цитотоксические лимфоциты не убивали здоровые клетки, аутореактивные Т-лимфоциты исключаются из репертуара в ходе отбора по толерантности.
Аутоантигены[править | править код]
Аутоантигены — как правило, нормальные белки или белковые комплексы (а также комплексы белков с ДНК или РНК), которые распознаются иммунной системой у пациентов с аутоиммунными заболеваниями. Такие антигены в норме не должны узнаваться иммунной системой, но, ввиду генетических факторов или условий окружающей среды, иммунологическая толерантность к таким антигенам у таких пациентов может быть утеряна.
Т-зависимые и Т-независимые антигены[править | править код]
По способности вызывать продукцию антител В-клетками без дополнительной стимуляции со стороны Т-клеток, антигены делят на Т-зависимые и Т-независимые[4]. Т-зависимые антигены не способны сами вызывать продукцию антител без помощи со стороны Т-клеток. Эти антигены не содержат большого количества повторяющихся эпитопов, к ним относятся белки. После того как В-клетка узнаёт Т-зависимый антиген с помощью уникального B-клеточного рецептора, она перемещается в герминативный центр лимфоидного фолликула. Здесь при участии Т-лимфоцитов происходит активная пролиферация активированной клетки, соматический гипермутагенез её генов, кодирующих вариабельные участки иммуноглобулинов, и последующая селекция[5].
Т-независимые антигены могут активировать В-клетки без помощи Т-клеток. Антигены этого типа характеризуются многократным повторением антигенной детерминанты в их структуре, к ним относятся полисахариды. По способности Т-независимых антигенов активировать В-клетки, специфичные к другим антигенам (поликлональная активация), их делят на I (вызывают поликлональную активацию) и II тип (не вызывают поликлональную активацию). В-клетки, активированные Т-независимыми антигенами, перемещаются в краевые зоны лимфоидных фолликулов, где они пролиферируют без участия Т-клеток. Также они могут подвергаться соматическому мутагенезу, но, в отличие от Т-зависимой активации, это не обязательно[5].
Под действием Т-зависимых и Т-независимых антигенов активированные В-клетки в обоих случаях дифференцируются в плазматические клетки и В-клетки памяти[5].
Антигены опухолей[править | править код]
Опухолевые антигены, или неоантигены — антигены, презентируюющиеся молекулами MHC I или MHC II на поверхности опухолевых клеток. Такие антигены могут быть презентированы опухолевыми клетками, и никогда — нормальными клетками. В таком случае они называются опухоль-специфичными антигенами (tumor-specific antigen, TSA) и, в общем случае, являются следствием опухоль-специфичной мутации. Более распространенными являются антигены, которые презентируются и на поверхности здоровых, и на поверхности опухолевых клеток, их называют опухоль-ассоциированными антигенами (tumor-associated antigen, TAA). Цитотоксические Т-лимфоциты, которые распознают такие антигены, могут уничтожить такие клетки до того, как они начнут пролиферировать или метастазировать.
Нативные антигены[править | править код]
Нативный антиген это антиген, который не был еще процессирован антигенпредставляющей клеткой на малые части. Т-лимфоциты не могут связываться с нативными антигенами и поэтому требуют процессинг АПК, в то время как В-клетки могут быть активированы непроцессированными антигенами.
См. также[править | править код]
- Эпитоп
Примечания[править | править код]
Ссылки[править | править код]
- Протокол выделения антител
- Иммунология
Источник
клеточным или гуморальным. Клеточный иммунитет обеспечивают иммунокомпетентные Т-лимфоциты, которые образуются из стволовых клеток, мигрирующих из красного костного мозга, в тимуса. Попадая в кровь, Т-лимфоциты создают большую часть лимфоцитов самой крови (до 80%), а также оседают в периферических органах иммуногенеза (прежде всего в лимфатических узлах и селезенке), образуя в них тимус-зависимые зоны, которые становятся активными точками пролиферации (размножения) Т-лимфоцитов вне тимуса. Дифференциация Т-лимфоцитов происходит в трех направлениях. Первая группа дочерних клеток способна при встрече с «чужим» белком-антигеном (возбудителем болезни, или собственным мутантом) вступать с ним в реакцию и уничтожать его. Такие лимфоциты называются Т-киллераш («убийцами») и характеризуются тем, что способны собственными силами, без предварительной иммунизации и без подключения антител и защитного комплемента плазмы крови (толкование этих понятий см. далее), осуществлять лизис (уничтожение путем растворения клеточных мембран и н Связывание белков) клеток-мишеней (носителей антигенов). Таким образом, Т-киллеры является отдельной ветвью дифференциации стволовых клеток (хотя их развитие, как будет описано далее, регулируемый Г-хелперов) и предназначены создавать как бы первичный барьер в противовирусном и противоопухолевый иммунитет организма.
Другие две популяции Т-лимфоцитов называются Т-хелперы и Т-супрессоры и осуществляют клеточный иммунный защиту через регуляцию уровня функционирования Т-лимфоцитов в системе гуморального иммунитета. Т-хелперы («помощники») в случае появления в организме антигенов способствуют быстрому размножению эффекторных клеток (исполнителей иммунной защиты). Различают два подтипа клеток хелперов: Т-хелперы-1, выделяющие специфические интерлейкины типа 1Л2 (гормоноподобные молекулы) и в-интерферон и связаны с клеточным иммунитетом (способствуют развитию Т-хелперов) Т-хелперы-2 выделяют интерлейкины типа ИЛ 4-1Л 5 и взаимодействуют преимущественно с Т-лимфоцитами гуморального иммунитета. Т-супрессоры способны регулировать активность В и Т-лимфоцитов в ответ на антигены.
Гуморальный иммунитет
Гуморальный иммунитет обеспечивают лимфоциты, которые дифференцируются из стволовых клеток мозга не в тимуса, а в других местах (в тонкой кишке, лимфатических узлах, глоточных миндалинах и т. д.) и называются В-лимфоцитами. Такие клетки составляют до 15% всех лейкоцитов. При первом контакте с антигеном чувствительны к нему Т-лимфоциты интенсивно размножаются. Некоторые из дочерних клеток дифференцируют в клетки иммунологической памяти и на уровне лимфоузлов в £-зонах превращаются в плазматические клетки, далее способны создавать гуморальные антитела. Способствуют этим процессам Т-хелперы. Антитела представляют собой большие протеиновые молекулы, имеющие специфическое родство к тому или иному антигену (на основе химической структуры соответствующего антигена) и называются иммуноглобулинов. Каждая молекула иммуноглобулина составлена из двух тяжелых и двух легких цепей связанных друг с другом дисульфидных связей и способных активизировать клеточные мембраны антигенов и присоединять к ним комплемент плазмы крови (содержит 11 протеинов, способных обеспечивать лизис или растворения клеточных мембран и свя Связывание белков клеток-антигенов). Комплемент плазмы крови имеет два пути активизации: классический (от иммуноглобулинов) и альтернативный (от эндотоксинов или ядовитых веществ и от лекарств). Выделяют 5 классов иммуноглобулинов (lg): G, A, M, D, E, различающихся по функциональным особенностям. Так, например, lg М привычно первым включается в иммунный ответ на антиген, активизирует комплемент и способствует поглощению этого антигена макрофагами или лизису клетки; lg А размещается в городах наиболее вероятного проникновения антигенов (лимфоузлах желудочно-кишечного тракта, в слезных, слюнных и потовых железах, в аденоидах, в молоке матери и т. д.) чем создает прочный защитный барьер, способствуя фагоцитозу антигенов; lg D способствует пролиферации (размножению) лимфоцитов при инфекциях, Т-лимфоциты «распознают» антигены при помощи включенных в мембрану гаммаглобулина, образующих антитело, связывая звена, конфигурация которых соответствует трехмерной структуре антигенных детерминированных групп (гаптенов или низкомолекулярных веществ, которые могут связываться с белками антитела, передючы им свойства белков антигена), как ключ соответствует замку (Г. Вильям, 2002; Г. Ульмер и др.., 1986). Активированные антигеном В-и Т-лимфоциты быстро размножаются, включаются в процессы защиты организма и массово погибают. В то же время не многие из активированных лимфоцитов превращаются в В-и Т-клетки памяти, которые имеют длительный срок жизни и при повторном инфицировании организма (сенсибилизации) В-и Т-клетки памяти «вспоминают» и распознают структуру антигенов и быстро превращаются в эффекторные (активные) клетки и стимулируют клетки плазмы лимфоузлов на изготовление соответствующих антител.
Повторные контакты с определенными антигенами могут иногда давать гиперергични реакции, сопровождающиеся повышенной проницательностью капилляров, усилением кровообращения, зудом, бронхоспазм и т. п.. Такие явления называются аллергическим реакциям.
Неспецифический иммунитет, обусловленный наличием в крови «естественных» антител, которые часто возникают при контакте организма с кишечной флорой. Насчитывают 9 веществ, которые вместе образуют защитный комплемент. Одни из таких веществ способны нейтрализовать вирусы (лизоцим), вторые (С-реактивный белок) подавляют жизнедеятельность микробов, третьи (интерферон) уничтожают вирусы и подавляют размножение собственных клеток в опухолях и др.. Неспецифический иммунитет обусловливают также специальные клетки-нейтрофилы и макрофаги, способные к фагоцитозу, т. е. к уничтожению (переваривания) чужеродных клеток.
Специфический и неспецифический иммунитет подразделяется на врожденный (передастся от матери), и приобретенный, который образуется после перенесенной болезни в процессе жизни.
Кроме этого существует возможность искусственной иммунизации организма, которая проводится либо в форме вакцинации (когда в организм вводят ослабленный возбудитель болезни и этим вызывают активизацию защитных сил что до образования соответствующих антител), либо в виде пассивной иммунизации, когда делают так называемое прививки против определенной болезни путем введение сыворотки (плазмы крови не содержащая фибриногена, или фактора ее свертывания, а зато имеет готовые антитела против определенного антигена). Такие прививки делают, например, против бешенства, после укусов ядовитых животных и так далее.
Как свидетельствует В. И. Бобрицкая (2004) у новорожденного ребенка в крови насчитывается до 20 тыс. всех форм лейкоцитов в 1 мм3 крови и в первые дни жизни их количество растет, даже, до 30 тыс. в 1 мм3, что связано с рассасыванием продуктов распада кровоизлияний в ткани ребенка, которые обычно происходят при рождении. Через 7-12 первых дней жизни количество лейкоцитов снижается до 10-12 тыс. в I мм3, что и сохраняется в течение первого года жизни ребенка. Далее количество лейкоцитов постепенно уменьшается и в 13-15 лет устанавливается на уровне взрослых (4-8 тыс. в 1 мм 3 крови). У детей первых лет жизни (до 7 лет) среди лейкоцитов преувеличивают лимфоциты и только в 5-6 лет их соотношение выравнивается. К тому же дети до 6-7 лет имеют большое количество незрелых нейтрофилов (юных, палочки — ядерных), что и обуславливает относительно низкие защитные силы организма детей младшего возраста против инфекционных заболеваний. Соотношение различных форм лейкоцитов в составе крови называется лейкоцитарной формулой. С возрастом у детей лейкоцитарная формула (табл. 9) значительно меняется: растет число нейтрофилах тогда как процент лимфоцитов и моноцитов уменьшается. В 16-17 лет лейкоцитарная формула принимает состав, характерный для взрослых.
Инвазия организма всегда приводит к возникновению воспаления. Острое воспаление обычно порождается реакциями антиген-антитело при которых активация комплемента плазмы крови начинается через несколько часов после иммунологических повреждений, достигает своей вершины через 24 часа, а угасает через 42-48 часов. Хроническое воспаление связано с влиянием антител на Т-лимфоцитарная систему, привычно проявляется через возрастная характеристика лейкоцитарной формулы
1-2 дня и достигает пика через 48-72 часа. В месте воспаления всегда повышается температура (связано с расширением сосудов); возникает припухлость (при остром воспалении обусловлено выходом в межклеточное пространство белков и фагоцитов, при хроническом воспалении — добавляется инфильтрация лимфоцитов и макрофагов); возникает боль (связано с повышением давления в тканях).
Болезни иммунной системы очень опасны для организма и зачастую приводят к летательным последствий, так как организм фактически становится незащищенным. Выделяют 4 основных групп таких болезней: первичная или вторичная иммунная недостаточность, нарушение функции; злокачественные заболевания, инфекции иммунной системы. Среди последних известным является вирус герпеса и угрожающе распространяясь в мире, в том числе и в Украине, вирус анти-HIV или anmiHTLV-lll/LAV, который вызывает синдром приобретенного иммуннодифицита (AIDS или СПИД). В основе клиники СПИД лежит вирусное повреждение Т-хелперных (Th) цепи лимфоцитарной системы, что ведет к значительному росту количества Т-супрессорах (Ts) и нарушение соотношения Th / Ts, которое становится 2:1 вместо 1:2, следствием чего является полное прекращение продукции антител и организм погибает от любой инфекции.
Источник
