Иммунитет при раке пищевода

 На фоне успеха современной медицины в лечении различных злокачественных образований, рак пищевода остается своеобразной цитаделью, сопротивление которой не удается сломить.
На фоне успеха современной медицины в лечении различных злокачественных образований, рак пищевода остается своеобразной цитаделью, сопротивление которой не удается сломить.
Это связано с рядом причин:
- Прежде всего это раковая опухоль внутренней локализации. Диагностика рака пищевода, на ранних стадиях затруднена, а это значит что 60-70% диагностированных имеют уже запущенную форму — 3 либо 4 стадию.
- Следующей проблемой является нахождение опухоли, при раке пищевода, она находится вблизи жизненно важных органов, что затрудняет оперативное вмешательство и лучевую, химиотерапии.
- Рак пищевода, это удел как правило пациентов пожилого возраста, и здесь наряду с опухолью имеется букет сопутствующих заболеваний. Которые зачастую делают невозможным проведение специального лечения.
Как следствие, радикальное лечение возможно лишь у двух пациентов из трех с диагнозом раковая опухоль грудного отдела пищевода. Врачи называют рак пищевода — «неблагодарной опухолью», ведь лечение крайне затруднено, а результаты очень малозначительны.
По статистическим данным выживаемость после радикальной терапии у онкобольных раком пищевода, по истечению двух лет, составляет 56%, выше этого срока (более 5 лет), показатели снижаются до 25%.
В случаях использования неоадъювантной терапии рака пищевода, при использовании лучевой и химиотерапий, хотя и улучшаются результаты непосредственные, но не приводят к изменению отдаленных результатов.
Иммунотерапия рака пищевода
На фоне вышеперечисленных методов лечения, иммунотерапия считается наиболее перспективной. Использование ряда иммуноактивных веществ класса «фактор переноса»(трансфер фактор) дают очень высокие показатели.
Что такое трансфер фактор? — Определение данное профессором Амадс, данное им в журнале «Аллергология» №2 2005г., это концевая часть парадомера растворимого, одноклеточного, антигенсвязочного белка. Трансфер факторы это молекулы иммунизированного донора, способные перенести гиперчувствительность замедленного типа, и другие проявления специфического клеточного иммунитета, не иммунному реципиенту, способные контролировать деятельность Т-лимфоцитов и NK — натуральных киллеров.
Применение Трансфер Факторов при раке пищевода
Применение ТФ при иммунореабилитации значительно улучшает результаты лечения при различных видах рака, в т.ч. рак пищевода. По наблюдениям препараты ТФ, при диагнозе рак пищевода, демонстрируют ярко выраженное лечебное действие, которое сопоставимо с химиолучевой терапией. Отсутствие побочных эффектов и широкий спектр действия выделяют ТФ из ряда других иммунных препаратов. Имеющиеся аналоги имеют целый ряд побочных действий, при котором происходит критическое повреждение внутренних органов и ряда систем организма
Использование ТФ в режиме моно терапии, при диагнозе рак пищевода, приводит к регрессии опухоли. Сочетание иммунотерапии с использованием ТФ и лучевой терапии к стойкой регресии опухоли пищевода.
Настоятельно рекомендуется сочетать ТФ с существующими методами лечения, а не в моно терапии.
Дополнительное действие ТФ при раке пищевода
Как уже говорилось выше, рак пищевода зачастую дополнен сопутствующими заболеваниям, в силу возрастной категории пациентов. По заключению Российского Онкологического Научного Центра им.Блохина, у онкобольных с выраженным иммунодефицитом, применение ТФ значительно повышает иммунный статус. Немаловажно то что ТФ, помимо противоопухолевого действия, повышает не специфическую резистентность, оказывает анти стрессорный, анти склеротический, антиоксидантный и мембраностабилизирующие эффекты. Восстанавливает нарушенные функции различных систем организма, у возрастных больных с диагнозом рак пищевода. Также Тф имеет адаптогенные и радио протекторные свойства, т.е. повышает сопротивление организма вредному действию лучевого лечения и помогает максимально быстро восстановится после проведения процедур.
Выводы о применении ТФ при диагнозе рак пищевода
После достижения на фоне приема ТФ регрессии опухоли рака пищевода и нормализации общего состояния у больных (инкурабельных) которым ранее было запрещено специальное лечение, необходимо вновь обследоваться на предмет проведения специального лечения. Подобная тактика может дать дополнительный шанс на полное выздоровление.
Дополнительным достоинством сочетания химиолучевой терапии с препаратами ТФ, при диагнозе рак пищевода, является перспектива излечения пациентов без опасных последствий применения операции по удалению части пищевода и безвозвратного повреждения множества систем и органов, что в конечном итоге значительно повысит качество жизни.
Отзывы о применении Трансфер Факторов при онкологии (раке пищевода)
Документально зарегистрированный результат применения ТФ при раке пищевода(из практики онколога Пинаева С.К.)
Житель Дальнегорска в возрасте 75 лет, в августе 2010г. получил диагноз: рак нижней трети пищевода стадия 1. Были проведены рентгенография, компьютерная томография, фиброизофагоскопия, гистологические исследования показали: умеренно дифференцированный плоскоклеточный неороговевающий рак с изъязвлениями. Поставлены и сопутствующие диагнозы: атеросклеротический кардиосклероз, артериальная гипертензия 2-й степени (риск 3-й степени) и недостаточность кровообращения 1-й степени.
Больному было назначено лечение, согласно принятым стандартам, проведено лучевое лечение в два этапа. Одновременно с лучевой терапией больной принимал Трансфер Фактор Эдванс и Трансфер Фактор Плюс, по 9 капсул каждого препарата в день на протяжении 6 месяцев. При контрольном обследовании, после начала лечения, через 2 месяца, в ноябре 2010, опухоль необнаружена и констатирована полная регрессия рака пищевода. Больной находится под регулярным наблюдением онколога и вот спустя 3 года, по данным на декабрь 2013г., у пациента стойкая ремиссия.
Статья подготовлена по материалам доклада онколога Пинаева С.К. «Терапия рака пищевода»
Применение Трансфер Факторов в терапии и профилактике рака пищевода Пинаев С. К.
Источник
ФАКТОРЫ ЛОКАЛЬНОГО ИММУНИТЕТА ПРИ РАКЕ ПИЩЕВОДА РАЗНОЙ СТЕПЕНИ ДИФФЕРЕНЦИРОВКИ
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Кит О.И.
1
Максимов А.Ю.
1
Колесников Е.Н.
1
Трифанов В.С.
1
Златник Е.Ю.
1
Новикова И.А.
1
Селютина О.Н.
1
Закора Г.И.
1
Базаев А.Л.
1
1 ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России
Проведено исследование некоторых субпопуляций лимфоцитов, присутствующих в тканях опухоли при раке пищевода, особенности их распределения при хирургическом лечении в опухолевом очаге, по линии резекции пищевода и в перифокальной зоне между линией резекции и видимой границей опухоли. Исследование проведено у больных с опухолями разной степени дифференцировки от G1 до G3. В изученных препаратах опухолей пищевода найдено максимальное количество CD3+CD4+ Т-лимфоцитов и T regs по сравнению с остальными образцами тканей. Выявлены некоторые гендерные различия, а также различия в зависимости от степени дифференцировки: в высокодифференцированных опухолях уровни CD3+ и CD3+CD4+ клеток были выше, чем в низкодифференцированных, но уровень T regs повышен в образцах всех опухолей вне зависимости от степени дифференцировки.
рак пищевода
степень дифференцировки
лимфоциты
1. Бережная Н.М., Чехун В.Ф. Иммунология злокачественного роста. – Киев. «Наукова Думка», –2005. –792 с.
2. Златник Е.Ю., Бахтин А.В., Кочуев С.С., Новикова И.А., Селютина О.Н., Непомнящая Е.М., Пржедецкий Ю.В., Позднякова В.В., Захарова Н.А. Факторы локального клеточного иммунитета при меланоме кожи // Современные проблемы науки и образования. – 2015. — № 5. URL: https://www.science-education.ru/128-21801.
3. Кит О.И., Геворкян Ю.А., Солдаткина Н.В., Ильченко С.А., Златник Е.Ю., Новикова И.А., Непомнящая Е.М. Факторы локального иммунитета у больных раком желудка при применении химиотерапии с озонированными средами // Современные проблемы науки и образования. – 2013. – № 5. URL: https://www.science-education.ru/111-9893.
4. Кит О.И., Шапошников А.В., Златник Е.Ю., Никипелова Е.А., Новикова И.А. Местный клеточный иммунитет при аденокарциноме и полипах толстой кишки // Сибирское медицинское обозрение. – 2012. – № 4 (76). – С. 11-16.
5. Селькова М.С., Селютин А.В., Сельков С.А. Особенности содержания Т-регуляторных лимфоцитов и NК-клеток у пациентов с хроническим гепатитом С. // Инфекции и иммунитет. — 2012. — Т.2. №4. — С. 715-722.
6. El-Serag HB, Hollier JM, Gravitt P, Alsarraj A, Younes M. Human papillomavirus and the risk of Barrett’s esophagus [published online ahead of print August 14, 2012]. Dis Esophagus. doi: 10.1111/j. 1442-2050.2012.01392.x.
7. Ferlay J, Shin HR, Bray F. et al. Estimates of world wide burden of cancer in 2008: GLOBOCAN 2008 // J. Cancer. – 2010. – Vol.127. – P.28932917.
8. Jemal A.,Bray F.,Center M.M.et al. Global cancer statistics // CA Cancer J. Clin. 2011. Vol. 61 (2). P. 69–90
9. Xu W. • Liu Z. • Bao Q. • Qian Z. Viruses, Other Pathogenic Microorganisms and Esophageal Cancer // Gastrointest Tumors. – 2015. — Vol. 2, No. 1, Р. 2-13 (DOI:10.1159/000380897)
10. Zandberg D. P., Bhargava R., Badin S., Cullen K. J. The role of human papillomavirus in nongenital cancers. A Cancer Journal for Clinicians. 2013, vol. 63, no.1, p. 57–81. (DOI: 10.3322/caac.21167).
Рак пищевода занимает 8-е место в структуре злокачественных новообразований в мире [8]. В настоящее время в мире ежегодно регистрируется около 480 тысяч новых случаев этого заболевания, при этом смертность: 400 тысяч смертей от рака пищевода каждый год [7].
Прогноз онкологических заболеваний, как и возможность применения иммунотерапии в комплексном лечении, не в последнюю очередь зависит от состояния локального иммунитета [1]. При диагностическом гистологическом исследовании опухолей пищевода в них нередко отмечается лимфоцитарная инфильтрация, однако, ее роль в течении и прогнозе заболевания остается дискуссионной. Происхождение ее также неясно, так как пищевод, в отличие от желудка, толстого кишечника, бронхов, не содержит MALT или BALT. В последнее время в литературе встречаются сообщения об ассоциации рака пищевода с присутствием некоторых вирусов, прежде всего, ВПЧ, что отчасти может объяснять лимфоцитарную инфильтрацию [6, 9, 10].
Целью данной работы является изучение клеточных факторов локального иммунитета при раке пищевода с различными характеристиками опухолей и организма-опухоленосителя.
Материалы и методы
Объектом изучения были фрагменты ткани опухоли и перитуморальной области 25 пациентов, прооперированных по поводу рака пищевода (6 женщин и 19 мужчин в возрасте от 40 до 77 лет), оперированных в отделении абдоминальной онкологии №1 Ростовского научно-исследовательского онкологического института за период с 2014 по 2015 годы. Все случаи заболевания были первичными, неоадъювантного лечения не проводилось. Преимущественное поражение верхнегрудного отдела пищевода выявлено у 1 больного, среднегрудного – у 12 больных, нижнегрудного – у 11 больных, у одного больного выявлено поражение абдоминального отдела пищевода. Распределение больных по распространенности опухолевого процесса представлено в таблице 1.
Таблица 1
Распределение пациентов по стадиям опухолевого процесса
Стадия | IA | IB | IIA | IIB | IIIA | IIIB | IIIC |
Количество больных | 2 | 4 | 6 | 2 | 7 | 1 | 3 |
% | 8 | 16 | 24 | 8 | 28 | 4 | 12 |
После предварительной подготовки всем больным по показаниям было выполнено оперативное вмешательство на органах брюшной полости и грудной клетки. Выбор объема операции определялся локализацией и размерами опухоли; распространенностью – стадией опухолевого процесса; наличием отдаленных метастазов; морфологическими характеристиками новообразования; возрастом и общем состоянием больных.
В зависимости от локализации и формы роста опухоли и объема поражения были выполнены следующие объемы операций: 24 больным с локализацией рака в среднегрудном, нижнегрудном и абдоминальном отделах пищевода выполнено оперативное вмешательство в объеме – субтотальная резекция пищевода, проксимальная резекция желудка с одномоментной внутриплевральной пластикой пищевода желудком. Одному больному с диагнозом рак верхнегрудного отдела пищевода выполнена экстирпация пищевода с формированием эзофаго и гастростомии (операция типа Добромыслова-Торека). Всем больным (25) стандартно выполняли двухзональную лимфадиссекцию.
При гистологическом исследовании был выявлен плоскоклеточный рак у 7 больных без ороговения, у 18 с ороговением. У 8 больных определялась низкодифференцированная степень дифференцировки опухоли, у 12 – умереннодиффернцированная, у 5 – высокодифференцированная.
Исследование факторов локального клеточного иммунитета проводили не позднее, чем через час после хирургического лечения на свежем послеоперационном материале. Фрагменты опухолевой ткани, перитуморальной зоны (ПЗ, визуально неизмененной ткани, прилежащей к опухоли) и линии резекции (ЛР, ткани, удаленной от опухоли на расстояние 2-4 см дистально и проксимально, гомогенизировали с помощью дезагрегирующего устройства BD Medimachine. В гомогенатах тканей определяли популяционный и субпопуляционный состав лимфоцитов на проточном цитометре FACSCantoII (BD) с панелью антител T-, B-, NK (CD45, CD3, CD4, CD8, CD19, CD16/56), включая Т-клетки с TCR- рецептором αß и γδ; рассчитывали уровни NKT (CD3+CD16/56+), DN (CD3+CD4-CD8-); дополнительно оценивали количественное содержание Т-регуляторных (T-regs) клеток (CD4+CD25+CD127dim). Несмотря на то, что наиболее распространенным методом определения последних является подсчет клеток с фенотипом CD4+CD25brightFoxP3+, в литературе есть данные о приемлемости для этой цели фенотипа CD4+CD25+CD127dim [5].
Результаты выражали в процентах от общего количества лимфоцитов, для TCRαß TCRγδ – в процентах от CD3+, а для T-regs в процентах от CD3+CD4+ клеток. Статистическую обработку данных выполняли с помощью параметрических и непараметрических методов (t-критерий Стьюдента, критерий Уилкоксона, метод непрямых разностей).
Результаты
Проводили сравнение полученных показателей: в опухоли, ПЗ и ЛР; в зависимости от пола больных; в зависимости от степени дифференцировки опухоли.
Результаты представлены в таблицы 2, 3 и на рисунке 1.
Таблица 2
Характеристика факторов локального клеточного иммунитета у больных раком пищевода
Субпопуляции лимфоцитов, % | Образцы тканей (n=25) | ||
Опухоль | Перитуморальная зона | Линия резекции | |
CD3+ | 76,5±2,7 | 66,5±5,1 | 60,6±5,7 |
CD3+CD4+ | 47,8±6,06* ** | 29,1±5,76 | 23,6±4,26 |
CD3+CD8+ | 27,3±4,3 | 26,5±3,1 | 26,4±4,7 |
TCRαß | 92,3±2,43 | 89,4±3,45 | 88,0±2,22 |
TCRγδ | 7,05±2,38 | 9,36±3,0 | 10,4±2,2 |
CD16+/56+ | 8,0±2,9 | 8,4±2,8 | 13,1±3,0 |
CD19+ | 10,1±1,4 | 8,0±2,1 | 8,7±2,0 |
T regs (CD4+ СD25+CD127dim) | 19,1±2,8* ** | 8,1±2,0 | 3,8±1,1 |
Примечание. * — статистически достоверные отличия от ткани ЛР; ** — статистически достоверные отличия от ткани ПЗ (р<0,05)
Как видно из таблицы 2, обнаружен ряд статистически достоверных различий по содержанию исследованных субпопуляций лимфоцитов в тканях опухоли и немалигнизированных образцах (ПЗ и ЛР). Так, в опухолевой ткани выше, чем в ткани ЛР, оказалось содержание CD3+CD4+ и T regs, также имеющих рецептор CD4, которые могут рассматриваться по иммунофенотипу как часть общей Т-хелперно-индукторной субпопуляции. Среди Т-лимфоцитов преобладают Т-клетки с фенотипом TCRαß, как в крови, но не в ткани толстой кишки, где их соотношение обратное. Уровни остальных исследованных субпопуляций не имеют статистически значимых различий между образцами тканей.
Некоторые гендерные различия исследованных характеристик представлены в таблице 3.
Таблица 3
Сравнительная характеристика факторов локального иммунитета у мужчин и женщин, больных раком пищевода
Показатели, % | Образцы тканей | |||||
Опухоль | ПЗ | ЛР | ||||
мужчины | женщины | мужчины | женщины | мужчины | женщины | |
CD3+ | 77,6±6,1 | 84,8±3,9* | 61,8±7,5 | 70,3±14,5 | 60,2±7,4 | 60,2±12,4 |
Продолжение таблицы 3 | ||||||
CD3+CD4+ | 37,0±3,9* ** *** | 52,5±5,5* *** | 24,4±3,6 | 34,4±10,2 | 20,5±3,4 | 27,5±6,7 |
CD3+CD8+ | 29,7±4,1 | 23,9±2,4 | 28,1±4,6 | 25,6±7,8 | 28,0±5,7 | 24,3±5,6 |
CD19+ | 8,4±3,4 | 12,2±3,6 | 11,5±4,2 | 7,9±3,1 | 10,7±3,5 | 7,8±3,1 |
CD16/56+ | 10,1±3,7 | 4,0±0,9* | 10,9±3,4 | 5,1±2,1* | 13,2±3,8 | 14,1±6,3 |
NKT (CD3+CD16/56+) | 5,4±1,1 | 4,7±1,9 | 6,1±1,9 | 5,9±1,9 | 6,7±1,4 | 6,2±2,7 |
DN CD3+CD4-CD8- | 10,5±2,1 | 8,1±3,4 | 8,7±1,4 | 6,9±3,1 | 11,0±3,6 | 9,8±4,9 |
T regs (CD4+ CD25+CD127dim) | 21,0±2,7* ** | 18,3±3,6* | 5,1±0,7 | 11,2±6,1 | 4,3±0,9 | 3,2±1,8 |
Примечания: * — статистически достоверные отличия от ткани ЛР; ** — статистически достоверные отличия от ткани ПЗ; *** — статистически достоверные различия в зависимости от пола больных
У женщин выявлены различия по уровням CD3+ клеток, которые были выше в опухоли по сравнению с тканью ЛР, и NК-клеток, которые, напротив, были ниже, чем в ЛР. Обнаружено также более высокое содержание CD3+CD4+ лимфоцитов в опухолевой ткани у женщин по сравнению с мужчинами.
Сравнительная характеристика содержания лимфоцитов исследованных субпопуляций в опухолях различной степени дифференцировки представлена на рисунке 1. Несмотря на выраженную индивидуальную вариабельность полученных данных, удалось выявить ряд статистически достоверных различий.
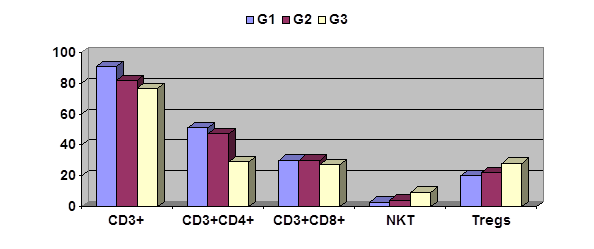
Рисунок 1. Содержание лимфоцитов некоторых субпопуляций в ткани опухолей с различной степенью дифференцировки (%).
Как видно из рисунка 1, в высокодифференцированных опухолях (G1) содержится статистически достоверно больше зрелых Т-лимфоцитов (CD3+), а также CD3+CD4+ клеток, чем в низкодифференцированных (G3); умеренно-дифференцированные опухоли (G2) занимают промежуточное положение. Описанная разница особенно демонстративна для CD3+CD4+ клеток, составляя 51,0±2,7% для G1, 46,9±5,8% для G2 и 25,8±6,8% для G3; последний показатель статистически значимо ниже двух первых (р<0,05). Следует отметить, что соответствующие данные по проценту T regs в опухолевой ткани не имели столь выраженных различий (рисунок 1), то есть их уровень высок вне зависимости от степени дифференцировки опухоли. Напротив, уровни NКТ-лимфоцитов были статистически достоверно выше в низкодифференцированных опухолях G3 (9,3±2,1% против 4,1±1,1% при опухолях G2 и 2,8±0,7% в высокодифференцированных опухолях G1; р<0,05). Содержание CD3+CD8+ и В-клеток в опухолях с различной степенью дифференцировки не различаются.
Заключение
Итак, удалось обнаружить некоторые различия показателей локального клеточного иммунитета в тканевых образцах больных раком пищевода. Опухоль отличается от прилежащих к ней немалигнизированных тканей более высоким содержанием хелперно-индукторных и Т-регуляторных лимфоцитов. Отмечены некоторые гендерные различия, свидетельствующие о том, что у женщин в локальные иммунные реакции более интенсивно вовлечено адаптивное звено клеточного иммунитета, а у мужчин – врожденное, связанное с NК-клетками. Однако, учитывая малочисленную группу больных женского пола, эти наблюдения можно рассматривать как предварительные. Установленные различия субпопуляционного состава лимфоцитов в опухолях с различной степенью дифференцировки позволяют предположить более выраженное нарушение Т-хелперно-индукторной субпопуляции при, по-видимому, компенсаторном повышении лимфоцитов минорной субпопуляции NКТ в образцах ткани низкодифференцированного рака. В целом, полученные данные соответствуют полученным нами ранее на других локализациях [2, 3, 4], что предполагает общность механизмов взаимодействия опухоли и иммунной системы организма опухоленосителя при различных злокачественных новообразованиях. Возможно, CD3+CD4+ клетки, мигрируют из крови через опухолевые сосуды с повышенной проницаемостью и адгезивными свойствами эндотелия, при этом происходит отбор минорной субпопуляции T regs, обладающих проонкогенными и иммуносупрессивными свойствами, для заселения опухолевой ткани.
Рецензенты:
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии Ростовского государственного медицинского университета, г. Ростов-на-Дону;
Николаева Н.В., д.м.н., ассистент кафедры онкологии Ростовского государственного медицинского университета, г. Ростов-на-Дону.
Библиографическая ссылка
Кит О.И., Максимов А.Ю., Колесников Е.Н., Трифанов В.С., Златник Е.Ю., Новикова И.А., Селютина О.Н., Закора Г.И., Базаев А.Л. ФАКТОРЫ ЛОКАЛЬНОГО ИММУНИТЕТА ПРИ РАКЕ ПИЩЕВОДА РАЗНОЙ СТЕПЕНИ ДИФФЕРЕНЦИРОВКИ // Современные проблемы науки и образования. – 2015. – № 6.;
URL: https://science-education.ru/ru/article/view?id=23527 (дата обращения: 11.07.2020).

Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
