Какие препараты убивают иммунитет
 Обычно когда речь идёт об иммунной системе, чаще приходиться читать и слышать о препаратах «повышающих иммунитет». Это достаточно модная тема, хотя и достаточно спорная. Пожалуй, единственное, о чём можно говорить, в контексте «повышения иммунитета», это его укреплении.
Обычно когда речь идёт об иммунной системе, чаще приходиться читать и слышать о препаратах «повышающих иммунитет». Это достаточно модная тема, хотя и достаточно спорная. Пожалуй, единственное, о чём можно говорить, в контексте «повышения иммунитета», это его укреплении.
В данном случае, избегая различных спекуляций, единственной группой средств являются витаминные комплексы грамотно подобранные специалистами. Особенно это касается детей. Витамины для детей являются наиболее безопасными и эффективными средствами для нормализации работы всего организма, в том числе и иммунной системы.
А вот о том, что иммунная система может подвергаться негативному действию ряда лекарственных средств, с развитием снижения защитных реакций организма, информации значительно меньше.
Вместе с тем, нередко, препараты снижающие иммунитет, являются необходимыми и полностью обоснованными, в отличие от средств направленных на его повышение.
Дело в том, что иммунная система очень сложно устроена и у некоторых людей может быть очень сильно выражены иммунные реакции. Это чаще даже опасней, чем умеренная иммуносупрессия, так как может привести к аутоиммунным заболеваниям или тяжёлым аллергическим состояниям. Поэтому у пациентов с гиперреактивными иммунными состояниями единственными средствами лечения являются иммунодепрессанты и цитостатики. Это, так называемые специфические средства иммунной супрессии. Наиболее эффективными иммунодепрессантами являются глюкокортикоидные средства, которые подавляют активность клеточного и гуморального иммунитета и позволяют помочь пациентам страдающих аутоиммунными заболеваниями, иммунозависимыми дерматозами и тяжёлыми формами аллергий, включая бронхиальную астму.
Препараты, понижающие иммунные реакции, необходимы и в трансплантологии. Так как после пересадки возникает реакция «трансплантат против хозяина» и возможно отторжение пересаженного органа или тканей. Назначение иммуносупреессантов позволяет избежать этого и добиться успеха в операциях обеспечивающих жизнь человека.
Однако необходимо понимать, что эти препараты назначаются исключительно по жизненным показаниям, а спектр их применения строго регламентирован. Это обусловлено тем, что препараты, понижающие иммунитет, являются специфическими химическими веществами, оказывающими угнетающее воздействие на различные компоненты иммунной системы, что, в свою очередь, неизбежно ведёт к подавлению реакций и различным патологическим процессам и состояниям. Так, при снижении защитных функций, многократно возрастает вероятность инфекционно-вирусными заболеваниями, а подчас и онкопатологиями. В связи с этим, при развитии вирусной или бактериальной инфекции на фоне длительного приёма препаратов иммуносупрессивного действия требуется назначение антибиотиков, сульфаниламидов или противогрибковых средств, что может ещё больше усугубить иммунный дефицит. Дело в том, антибиотики, сульфаниламиды и антимикотики, сами по себе обладают дополнительным механизмом, угнетающим иммунные реакции. Таким образом, присоединение их к терапии должно быть обосновано, а их назначение сопряжено с инфекционными осложнениями, угрожающими жизни больного.
Препараты из группы антибиотиков, сульфаниламидов и антимикотиков, относятся к группе препаратов, которые имеют побочное свойство подавлять защитные иммунные реакции, однако это не является основным фармакологическим действием данных средств. Поэтому не стоит сильно переживать за иммунную систему, если эти препараты назначаются для лечения бактериальных инфекций. Они обычно назначаются короткими курсами и не оказывают значительного негативного действия на иммунную систему, которая быстро восстанавливается после окончания терапии.
Материал подготовил:
Коллектив авторов компании ООО «Ферон»
Источник
Иммунодепресса́нты (иммуносупрессивные препараты, иммуносупрессоры) — это класс лекарственных препаратов, применяемых для обеспечения искусственной иммуносупрессии (искусственного угнетения иммунитета).
Применение[править | править код]
Искусственная иммуносупрессия как метод лечения применяется прежде всего при трансплантации органов и тканей, таких, как почки, сердце, печень, лёгкие, костный мозг.
Кроме того, искусственная иммуносупрессия (но менее глубокая) применяется при лечении аутоиммунных заболеваний и заболеваний, предположительно (но пока недоказанно) имеющих аутоиммунную природу.
Виды препаратов[править | править код]
Класс иммуносупрессивных препаратов неоднороден и содержит препараты с различными механизмами действия и различным профилем побочных эффектов. Различается и профиль иммуносупрессивного эффекта: некоторые препараты более или менее равномерно подавляют все виды иммунитета, другие имеют особую избирательность по отношению к трансплантационному иммунитету и аутоиммунитету, при сравнительно меньшем влиянии на антибактериальный, противовирусный и противоопухолевый иммунитет. Примерами таких, относительно селективных, иммуносупрессоров являются тимодепрессин, циклоспорин А и такролимус. Различаются иммуносупрессивные препараты и по преимущественному влиянию на клеточный либо гуморальный иммунитет.
Стоит отметить, что сама успешная аллотрансплантация органов и тканей, резкое снижение процента отторжения трансплантатов и длительная выживаемость больных с трансплантатами стали возможными только после открытия и внедрения в широкую практику трансплантологии циклоспорина А. До его появления не существовало удовлетворительных методов иммуносупрессии, позволявших обеспечить необходимую степень подавления трансплантационного иммунитета без тяжёлых, угрожающих жизни больного побочных эффектов и глубокого снижения противоинфекционного иммунитета.
Следующим этапом развития теории и практики иммуносупрессивной терапии в трансплантологии стало внедрение протоколов комбинированной — трёх- или четырёхкомпонентной иммуносупрессии при пересадке органов. Стандартная трёхкомпонентная иммуносупрессия на сегодняшний день состоит из комбинации циклоспорина А, глюкокортикоида и цитостатика (метотрексата или азатиоприна, или микофенолат мофетила). У больных с высоким риском отторжения трансплантата (высокая степень негомологичности трансплантата, предшествующие неудачные трансплантации и др.) обычно применяют четырёхкомпонентную иммуносупрессию, включающую также анти-лимфоцитарный или анти-тимоцитарный глобулин. Больным, не переносящим один или более компонентов стандартной схемы иммуносупрессии или подверженным высокому риску инфекционных осложнений либо злокачественных опухолей, назначают двухкомпонентную иммуносупрессию или, реже, монотерапию.
Новый прорыв в трансплантологии связан с появлением нового цитостатика флударабина фосфата (Флудары), обладающего сильной селективной цитостатической активностью в отношении лимфоцитов, и c разработкой метода кратковременной (несколько суток) высокодозной пульс-терапии глюкокортикоидами с использованием метилпреднизолона в дозах, в 100 раз превышающих физиологические. Сочетанное применение флударабина фосфата и сверхвысоких доз метилпреднизолона позволило в считанные дни и даже часы купировать остро возникающие на фоне стандартной иммуносупрессивной терапии реакции отторжения трансплантатов, что было очень трудным делом до появления Флудары и высокодозных глюкокортикоидов.
Ссылки[править | править код]
- Фармакологическая группа — Иммунодепрессанты // RLSNET, Только для медицинских специалистов
Источник
Лекарства подавляющие иммунитет (иммунодепрессанты)
Как профилактика отторжения трансплантата, так и лечение аутоиммунных заболеваний требуют подавления иммунных реакций. Однако иммунная супрессия влечет за собой ослабление защитных сил против инфекционных возбудителей и повышение риска развития опухоли в отдаленный период.
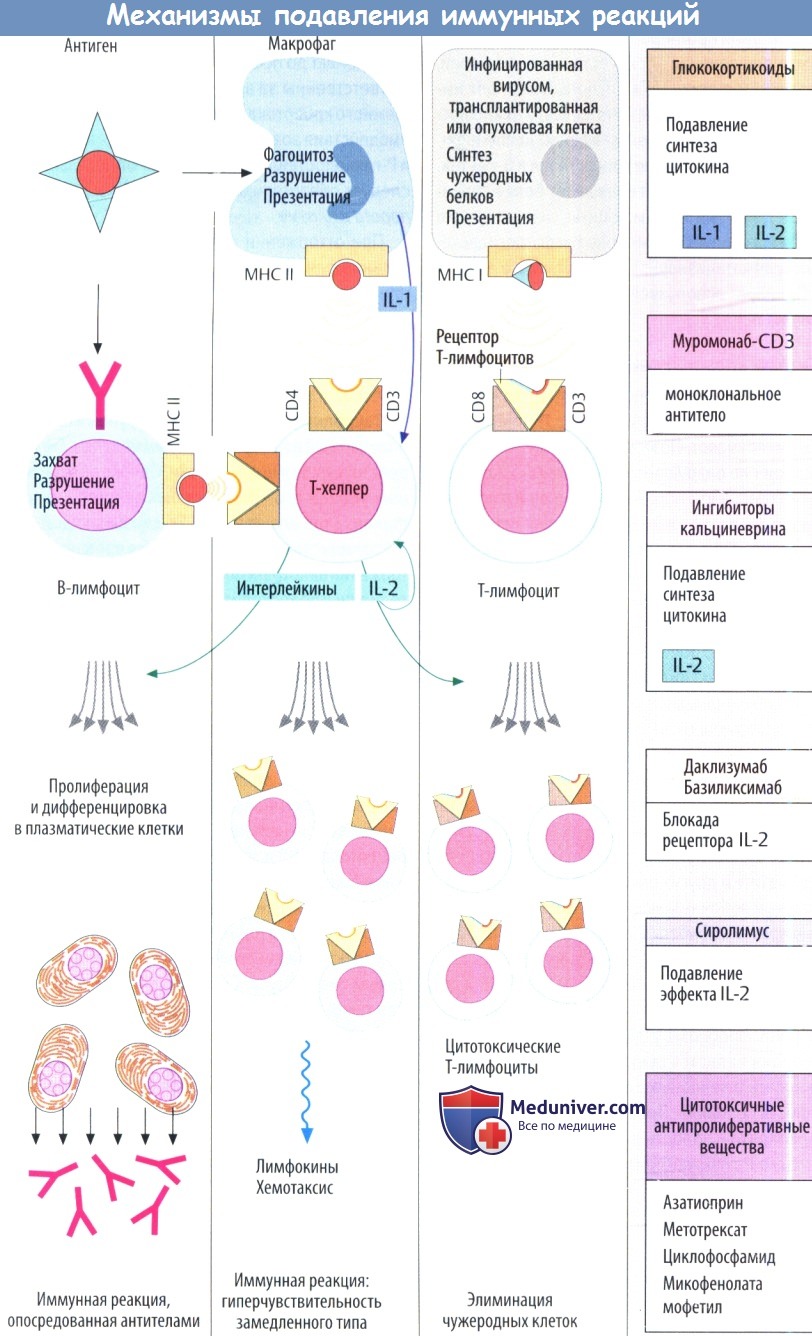
Специфический иммунный ответ начинается со связывания антигена лимфоцитами, несущими рецепторы с соответствующим антигенсвязываю-щим участком. В-лимфоциты распознают структуры поверхностного антигена с помощью мембранных рецепторов, которые похожи на образованные впоследствии антитела. Т-лимфоцитам (и интактным В-клеткам) требуется антиген на поверхности макрофагов или других клеток в сочетании с главным комплексом гистосовместимости (МНС); последний обеспечивает распознавание антигенных структур посредством рецепторов Т-клеток. Т-хелперы несут комплексы CD3 и CD4, цитотоксические Т-клетки — комплекс CD8.
Белки CD участвуют в связывании МНС. Активация Т-клеток также увеличивается при контакте с другими мембранными белками: CD80/86 в случае клетки, несущий антиген, и CD28 на лимфоците. Существует собственный физиологический прерывающий механизм при высвобождении активированными лимфоцитами С028-подобных инертных молекул во внеклеточное пространство; они «покрывают» комплекс CD80/86 и предупреждают контакт с ним и активацию лимфоцитов. Кроме того, распознавание антигена и стимуляция цитокинами играют важную роль в активации лимфоцитов.
Интерлейкин-1 образуется макрофагами, а другие интерлейкины (IL), в т. ч. IL-2, образуются Т-хелперами. При пролиферации антигенспецифических лимфоцитов запускается иммунная защита. I.
I. Воздействие на распознавание антигена. Муромонаб CD3 — моноклональное антитело, направленное против CD3 мышей, которое блокирует распознавание антигена Т-лимфоцитами (используется при отторжении трансплантата).
Глатирамера ацетат состоит из пептидов различной длины, полимеризованных в случайной последовательности из аминокислот глутамина, лизина, аланина и тирозина. Его используют при лечении рассеянного склероза наряду с IFN-β. Данное заболевание является результатом аутоагрессии Т-лимфоцитов направленной против олигодендроцитов, которые образуют миелиновые оболочки аксонов ЦНС.
Причинный антиген, очевидно, является основным миелиновым белком. Глатирамер имеет сходство с последним. Блокируя рецепторы антигена, он нарушает распознавание антигена лимфоцитами.
Абатацепт — слитный белок, состоящий из инертной молекулы лимфоцита CD28 и Fc-фрагмента антитела. Он имитирует физиологическое торможение в результате антигенной стимуляции Т-клеток и применяется при ревматоидном артрите.
II. Подавление продукции цитокина и его действия. Глюкокортикоиды модулируют экспрессию множества генов. В частности, за счет этого эффект; ингибируется продукция IL-1 и IL-2, что объясняет супрессию зависимых от Т-клеток иммунных ответов. Кроме того, глюкокортикоиды нарушают образование воспалительных цитокинов и сигнальных молекул в других мишенях. Глюкокортикоиды используются при пересадке органов, аутоиммунных и аллергических заболеваниях. Системное применение несет в себе риск ятрогенного синдрома Кушинга.
Циклоспорин и родственные соединения ингибируют продукцию цитокинов, в частности IL-2. В отличие от глюкокортикоидов его применение не сопровождается множеством сопутствующих метаболических эффектов.
Анакинра — рекомбинантная форма эндогенного антагониста рецепторов IL-1, применяется при ревматоидном артрите.
Даклизумаб и базиликсимаб являются моноклональными антителами против рецепторов IL-2. Они состоят из Fab-фрагмента мышей и Fc-фрагмента человека. Их используют для подавления реакций отторжения трансплантата.
III. Нарушение метаболизма клетки в результате подавления пролиферации. В дозах ниже, чем требуюгся для лечения злокачественных опухолей, некоторые цитостатики также используются для иммуносупрессии (азатиоприн, метотрексат и циклофосфамид). Антипролиферативный эффект неспецифичен для лимфоцитов и касается как Т-, так и В-клеток.
Микофенолата мофетил оказывает более специфическое действие на лимфоциты, чем на другие клетки. Он ингибирует инозинмонофосфатдегидроге-назу, которая катализирует синтез пуринов в лимфоцитах. Препарат используется при острых реакциях отторжения ткани.
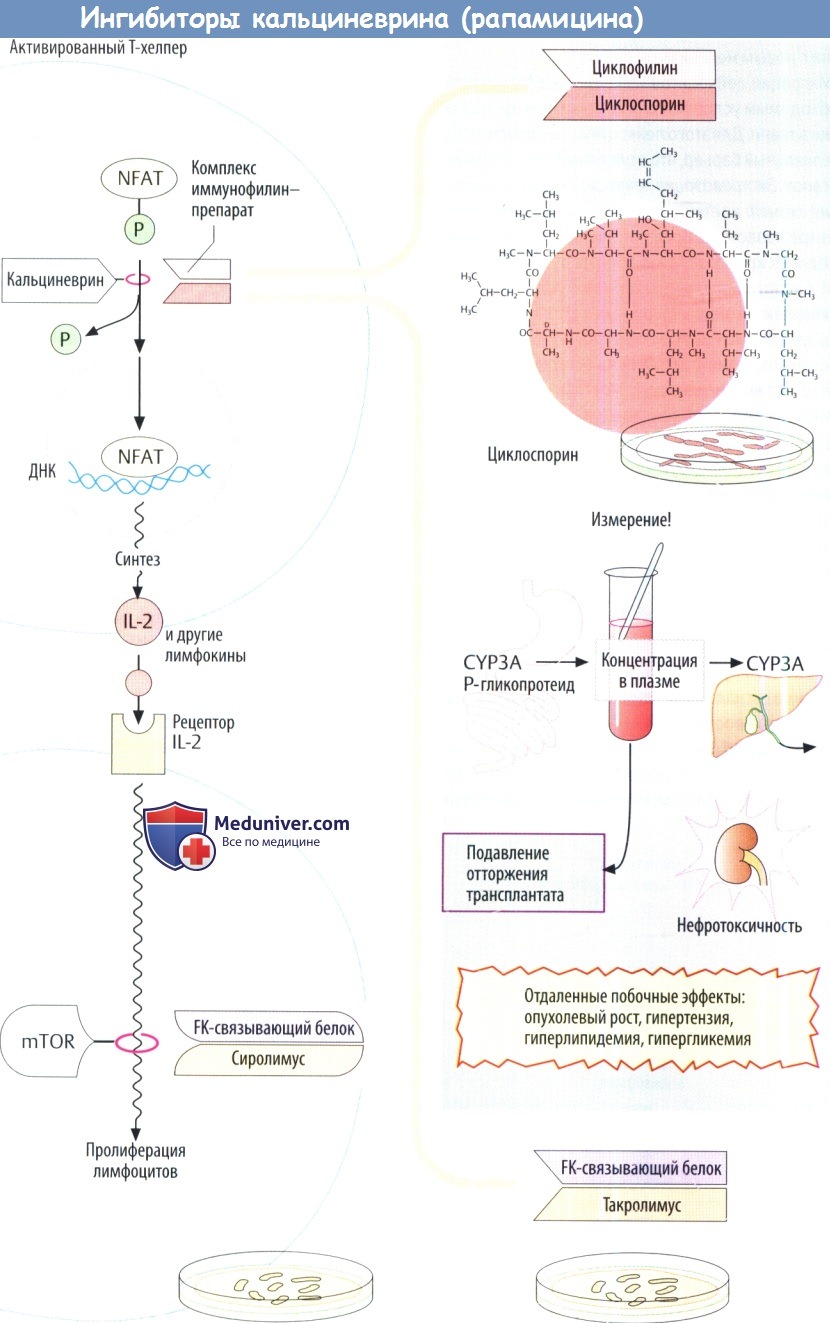
IV. Ингибиторы кальциневрина (сиролимус). Циклоспорин имеет грибковое происхождение. Он является пептидом, состоящим из 11 отчасти атипичных аминокислот. Поэтому при введении внутрь циклоспорин не разрушается желудочно-кишечными протеазами. В клетках Т-хелперов он ингибирует продукцию IL-2 за счет изменения уровня регуляции транскрипции. Обычно ядерный фактор активированных Т-клеток (NFAT) стимулирует экспрессию IL-2. Это требует дефосфорилирования предшественника, фосфорилированного NFAT, с помощью фосфатазы кальциневрина, что обеспечивает поступление NFAT в клеточные ядра из цитозоля.
Циклоспорин связывается с белком циклофилином внутренней среды клетки, а образующийся комплекс ингибирует кальциневрин и, следовательно, продукцию IL-2.
Достижения в современной трансплантологии связаны в основном с введением в практику циклоспорина. В настоящее время он также используется при некоторых аутоиммунных заболеваниях, атопическом дерматите и других расстройствах.
Основным побочным эффектом циклоспорина является нефротоксичность. Поэтому его дозу необходимо титровать таким образом, чтобы уровень препарата в крови не был слишком высоким (риск повреждения почек) и не слишком низким (реакция отторжения). Проблема усложняется еще и тем, что циклоспорин является веществом, которое трудно использовать в лечебных целях. Пероральная био-доступность неполная. Происходит обратный транспорт препарата в полость кишечника посредством выносящего Р-гликопротеидного насоса в дополнение к метаболизму цигохромоксидазами подгрупп 3А.
Печеночные изоферменты CYP3A4 способствует выведению до поступления в системный кровоток и ответственны за выведение циклоспорина из системного кровотока. Различные лекарственные взаимодействия возникают в результате влияния CYP3, и Р-гликопротеида. При подборе оптимальной дозы следует обязательно контролировать уровень препарата в плазме.
При отторжении трансплантата требуется длительное лечение препаратами, вызывающими супрессию. Длительная иммуносупрессия несет в себе повышенный риск развития злокачественных опухолей. Факторами риска сердечно-сосудистых заболеваний могут быть нежелательные реакции — критический и важный момент в отдаленном прогнозе
Такролимус — антибиотик из группы макролидов получаемый из Streptomyces tsukubaensis. По сути oн действует, как и циклоспорин. Однако на молекулярном уровне его «рецептором» является не циклофилин, а так называемый FK-связывающий белок. Такролимус тоже используется для профилактики отторжения аллотрансплантата. По проницаемости эпителия он превосходит циклоспорин, что позволяет применять его местно при атопическом дерматите
Сиролимус (рапамицин) — еще один макролид, продуцируемый Streptomyces hydroscopicus. Иммуносупрессивное действие не связано с ингибированием кальциневрина. Он образует комплекс с FK белком, вызывая особые конформационные изменения, а комплекс далее ингибирует фосфатазу mTOP (мишени рапамицина млекопитающих). Последний управляет сигнальным путем, который начинается рецептором IL-2 и заканчивается активацией митоза в лимфоцитах. Следовательно, сиролимус ингибирует пролиферацию лимфоцитов. Препарат одобрен для профилактики отторжения трансплантата.
Структура и действие эверолимуса аналогичны таковым сиролимуса. Сиролимус также используется для покрытия стентов, которые установлены в атеросклеротических коронарных артериях для сохранения просвета сосудов после баллонной дилатации. Сиролимус предназначен для остановки процессов пролиферации в сосудистой стенке, которая может привести к сужению просвета. Темсиролимус используется при лечении почечноклеточного рака.
V. Ингибиторы миграции лейкоцитов. Натализумаб и эфализумаб — блокаторы интегрина с новым механизмом действия.
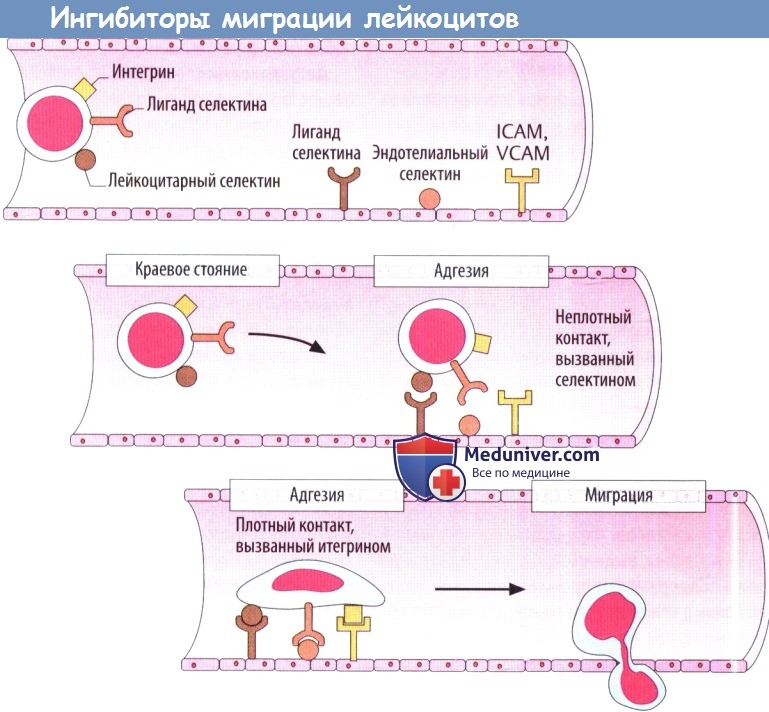
Миграция лейкоцитов из кровотока является необходимым условием для переноса иммунной реакции в ткани. Для этого лейкоциты преодолевают эндотелиальный барьер, что осуществляется в несколько этапов. Экстравазация лейкоцитов в месте повреждения тканей: клетки крови обычно располагаются в центре кровотока. Воспалительная вазодилатация замедляет кровоток, а лейкоциты лучше контактируют с эндотелиальными клетками. Адгезия: между лейкоцитами и эндотелиальными клетками образуются адгезивные мостики.
В первую очередь селектины с некоторыми углеводными остатками контактируют со смежными клетками. Мостики нестабильные, но открываются повторно, что замедляет движение лейкоцитов к эндотелию. Стабильная адгезия с остановкой лейкоцитов обусловлена интегринами в лейкоцитах и белками адгезии в эндотелии (ICAM — внутриклеточная молекула адгезии; VCAM — сосудистая клеточная молекула адгезии). Эндотелиальные клетки в воспаленной области связывают большее количество белков адгезии на мембране. Лейкоциты движутся между контактами эндотелиальных клеток, затем проходятсквозьокружающиебазальные мембраны и мигрируют в ткань, притягиваемые хемотаксическими сигнальными веществами, которые продуцируются при воспалений.
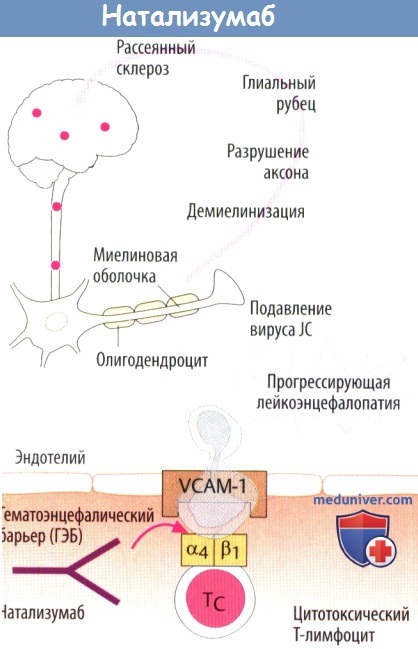
Натализумаб — человеческие антитела против α4-субъединицы интегринов. Интегрины являются гетеродимерными белками, состоящими из субъединиц α и β. Существуют разные изоформы. Связывание натализумаба блокирует миграцию Т-лимфоцитов в ЦНС. Это можно использовать при лечении рассеянного склероза. При данном аутоиммунном заболевании цитотоксические Т-лимфоциты атакуют олигодендроциты, которые продуцируют миелин в ЦНС. Редкой, но очень опасной нежелательной реакцией является прогрессирующая мультифокальная лейкоэнцефалопатия.
Она возникает в результате растормаживания вируса JC (от инициалов пациента у которого впервые выделен вирус). Данный вирус широко распространен, но обычно контролируется иммунной системой. Натализумаб является резервным препаратом, и его нельзя вводить вместе с другими иммуносупрессивными средствами против рассеянного склероза (IFN-β, глатирамера ацетат).
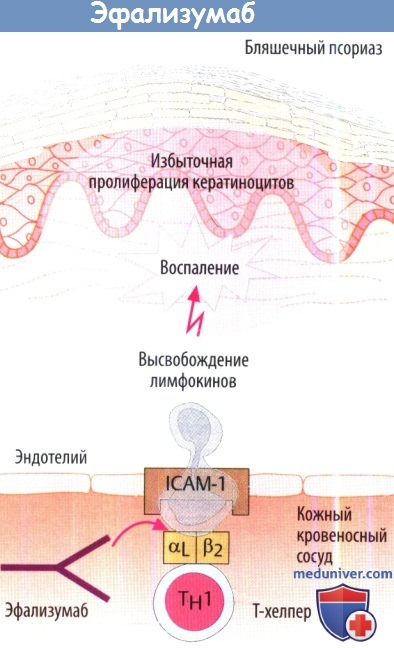
Эфализумаб используют при умеренной и тяжелой формах бляшечного псориаза. Известно, что данное заболевание аутоиммунное. Эфализума действует против а-субъединицы (αL, также известной как CD11) интегрина (LFA-1) Т-хелперов. Это останавливает миграцию лимфоцитов из сосудистого русла. Кроме того, блокируется контакт с клетками пораженной области кожи (клетки, несущие антиген кератиноциты). Побочные эффекты: выраженные гриппоподобные симптомы, повышение числа лимфоцитов. Из-за случаев прогрессирующей мультифокальной лейкоэнцефалопатии, о которых сообщалось у некоторых пациентов после лечения эфализумабом, данный препарат в настоящее время не используется в США и ЕС.

— Также рекомендуем «Лекарства для лечения отравлений — антидоты»
Оглавление темы «Фармакология лекарств»:
- Лекарства для выведения глист — противоглистные
- Лекарства для лечения малярии
- Лекарства для лечения тропических инфекций
- Лекарства для лечения опухоли — цитостатики
- Цитостатики влияющие на сигнальные пути клеточной пролиферации
- Целенаправленные цитостатики для лечения опухоли
- Механизмы развития устойчивости опухоли к химиотерапии
- Лекарства подавляющие иммунитет (иммунодепрессанты)
- Лекарства для лечения отравлений — антидоты
- Лекарства галлюциногены — психомиметики
Источник
