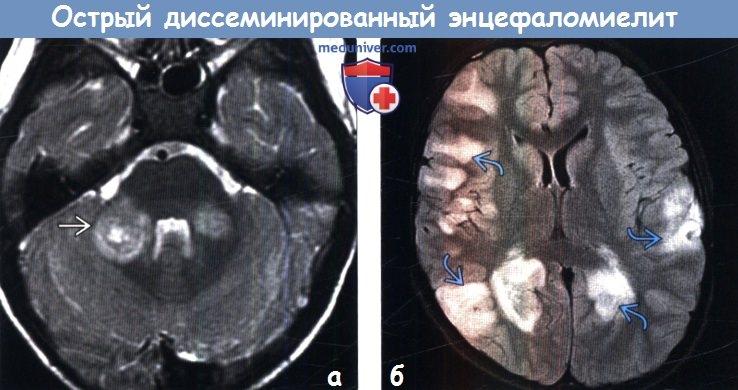
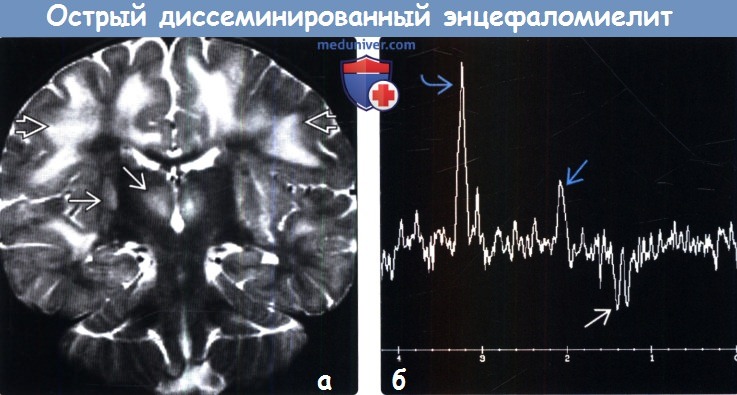
Картина мрт при рассеянном энцефаломиелите
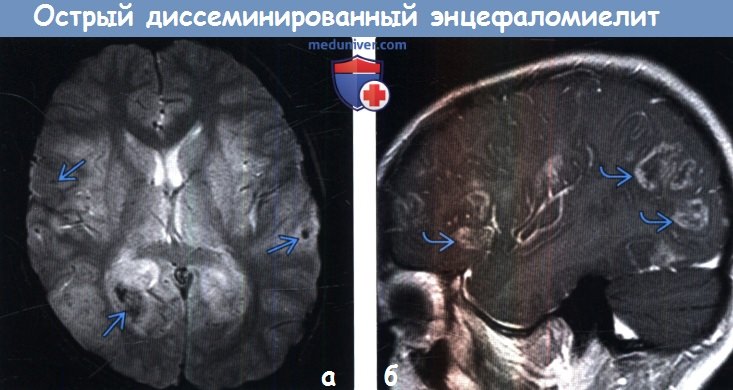
Диагностика острого диссеминированного энцефаломиелита по КТ, МРТа) Терминология: б) Визуализация: 1. Общие характеристики острого диссеминированного энцефаломиелита (ОДЭМ): 2. КТ признаки острого диссеминированного энцефаломиелита (ОДЭМ):
3. МРТ признаки острого диссеминированного энцефаломиелита (ОДЭМ): 4. Рекомендации по визуализации:
в) Дифференциальная диагностика острого диссеминированного энцефаломиелита (ОДЭМ): 1. Рассеянный склероз (PC): 2. Аутоиммунный васкулит: 3. Острая гипертензивная энцефалопатия, СЗЭО: 4. Возрастные изменения головного мозга с гиперинтенсивными поражениями БВ: 5. Болезнь Фабри: 6. Болезнь Бехчета:
г) Патология: 1. Общие характеристики острого диссеминированного энцефаломиелита (ОДЭМ): 2. Макроскопические и хирургические особенности: 3. Микроскопия: д) Клиническая картина: 1. Проявления острого диссеминированного энцефаломиелита (ОДЭМ): 2. Демография: 3. Течение и прогноз: 4. Лечение острого диссеминированного энцефаломиелита (ОДЭМ): д) Диагностическая памятка. Советы по интерпретации изображений: е) Список литературы:
— Также рекомендуем «Острый геморрагический лейкоэнцефалит (ОГЛЭ) на МРТ» Редактор: Искандер Милевски. Дата публикации: 19.4.2019 |
Источник
Острый рассеянный энцефаломиелит (ОРЭМ) – это острое, как правило, однофазное аутоиммунно обусловленное (на антигены миелина) демиелинизирующее заболевание нервной системы, характеризующийся наличием общемозговых и очаговых симптомов в результате иммунизации или инфекций (в 70% случаев дебюту ОРЭМ предшествуют перенесенные инфекционные заболевания либо вакцинации, в остальных случаях патологический процесс развивается независимо от каких-либо факторов и его причина остается неизвестной — идиопатическая форма ОРЭМ). Имеются сообщения о повторных случаях заболевания ОРЭМ — «рецидивирующий, возвратный или мультифазный ОРЭМ» (см. далее).
Несмотря на достаточно четкую временную связь ОРЭМ с перенесенной инфекцией или иммунизацией, установлено, что он не является результатом прямого вирусного повреждения нервной ткани. Указанные причины являются триггерным фактором в запуске аутоиммунного процесса. Предполагаемыми механизмами развития аутоиммунной реакции при ОРЭМ являются: [1] молекулярная мимикрия (перекрестный иммунный ответ на антигены вируса и составляющие миелина), [2] неспецифическая активация аутореактивных клеток под воздействием суперантигена, [3] повреждение (инфицирование) олигодендро-глиальных клеток с нарушением ресинтеза миелина и [4] повреждения эндотелия сосудов с нарушением гемато-энцефалического барьера.
читать (на laesus-de-liro.livejournal.com) статью: Нейроглия [читать] и статью: Нейроглия и глиоз [читать]
В качестве провоцирующего агента ОРЭМ могут выступать предшествующие инфекции, вызванные вирусами кори, эпидемического паротита, краснухи, ветряной оспы, простого герпеса, гриппа А и В, Эпштейна-Барр, группы Коксаки, цитомегаловируса, а также, вероятно, вирусами гепатита С и ВИЧ; вакцинации от ветряной оспы, бешенства, кори, краснухи, полиомиелита, японского энцефалита, гепатита В, гриппа, столбняка, коклюша, дифтерии. В последнее время высказываются предположения о том, что в качестве этиологического фактора ОРЭМ могут выступать и некоторые бактериальные инфекции (b-гемолитический стрептококк группы А, легионелла, лептоспира, риккетсия, микоплазма, боррелия). Наиболее часто предшествуют ОРЭМ в детском возрасте корь (1 : 1000), ветряная оспа (1 : 10 000) и краснуха (1 : 20 000). В некоторых случаях ОРЭМ может развиваться после перенесенного острого респираторного заболевания неясной этиологии.
Считается, что заболеванию подвержены дети младше 10 лет, а средний возраст начала заболевания у детей составляет приблизительно 8 лет. Зарегистрированы даже случаи начала ОРЭМ в младенческом возрасте (3 месяца). В зрелом и пожилом возрасте ОРЭМ встречается реже, средний возраст этой категории пациентов составляет 33,9 и 62,3 года соответственно.
Морфологической основой заболевания являются аутоиммунное воспаление в пространствах Вирхова–Робена, а также выраженная диффузная демиелинизация, вследствие чего вовлекается преимущественно подкорковое белое вещество головного мозга, при этом возможно наличие очагов и в сером веществе: базальные ганглии, таламус, гипоталамус, кора больших полушарий (см. далее).
читать статью: Пространства Вирхова-Робина (на laesus-de-liro.livejournal.com) [читать]
Клиническая картина ОРЭМ характеризуется ярким, «богатым» на симптомы (см. далее) и быстро развивающимся дебютом заболевания. В начале болезни симптомы развиваются остро в течение 4 — 7 дней. Нередко начало заболевания знаменуется лихорадкой и недомоганием, что в купе с остальными симптомами отличает его от рассеянного склероза (РС). Отличительной чертой ОРЭМ и даже обязательным условием для постановки этого диагноза как у детей, так и у взрослых является наличие в клинической картине заболевания признаков энцефалопатии или общемозгового синдрома. Клинически синдром энцефалопатии включает в себя жалобы на головные боли, тошноту, возможно рвоту. Ключевым моментом в синдроме энцефалопатии являются поведенческие нарушения и нарушения сознания. При этом возможны психические нарушения вплоть до развития бреда и галлюцинаций; такие проявления считаются более характерным для пожилых пациентов. Зарегистрированы случаи дебюта ОРЭМ с острого психоза, корсаковского синдрома, депрессии и конверсионных изменений. Специфичность клинической картине ОРЭМ придает наличие нарушения сознания, которое может варьировать от сонливости и оглушенности до развития комы различной степени выраженности. У 10 — 35% больных ОРЭМ развиваются эпилептические припадки.
Следует выделить тот момент, что ОРЭМ у взрослых чаще развивается без лихорадки и выраженного общемозгового синдрома, который в большинстве случаев протекает легко или умеренно.
Клинически дебют ОРЭМ характеризуется полисимптомностью неврологических проявлений, что отражает одномоментное многоочаговое поражение ЦНС. Одновременно могут возникнуть поражения со стороны черепных нервов и двигательной сферы, которые также могут сочетаться с чувствительными и тазовыми нарушениями. При поражении пирамидного тракта развиваются геми-, тетрапарезы. В случае формирования очага демиелинизации в спинном мозге возможно развитие вялых парапарезов с тазовыми нарушениями различной степени выраженности. В патологический процесс при ОРЭМ могут вовлекаться различные черепные нервы. Наиболее ярким является двустороннее вовлечение II пары черепных нервов с развитием двустороннего оптического неврита. При ОРЭМ описаны поражения VII пары черепных нервов с формированием периферической невропатии лицевого нерва; III и VI пары — с жалобами на двоение, каудальной группы нервов — с развитием бульбарного синдрома. Поражение стволовых структур при ОРЭМ может проявиться в виде дыхательных нарушений, что нередко требует применения интенсивной терапии для поддержания витальных функций. При ОРЭМ выявляются проводниковые нарушения чувствительности, обусловленные очагами демиелинизации в спинном мозге. Развитие очагов демиелинизации в мозжечке и стволе более характерна для детей с ОРЭМ, хотя некоторые авторы утверждают, что мозжечковая симптоматика чаще выявляется у взрослых пациентов. Изменения в когнитивной сфере описываются у 69% пациентов с ОРЭМ и к ним относятся развитие лобного синдрома, мутизма и различных форм афазии (чаще моторной). Возникновения афазии у пациентов с ОРЭМ связывают с поражением проводящих путей, идущих к коре речевого центра. Особенностью ОРЭМ у взрослых является вовлечение в патологический процесс периферической нервной системы (ПНС). Процессы демиелинизации в ПНС носят чаще субклинический характер и касаются в основном спинномозговых корешков. Проявляются они клинически в виде корешковых болей и чувствительных нарушений в зоне иннервации корешков.
Отличительные особенности ОРЭМ у детей и взрослых:
Обратите внимание! В типичных случаях ОРЭМ клинически проявляется тяжелой энцефалопатией с выраженными общемозговыми и очаговыми симптомами. Нарушение сознания, психомоторное возбуждение, эпилептические припадки, головная боль и головокружение, тошнота, иногда менингеальные симптомы указывают на выраженный воспалительный процесс с отеком мозга и ориентируют в большей степени на ОРЭМ, требуя также дифференциальной диагностики с острыми сосудистыми и инфекционными поражениями.
Единой классификации ОРЭМ не существует, однако выделяют его особые варианты: [1] острый геморрагический лейкоэнцефалит; [2] острый поперечный миелит; [3] неврит зрительного нерва; [4] оптикомиелит; [5] церебеллит; [6] стволовой энцефалит.
Согласно последним исследованиям и метаанализу большой группы пациентов с ОРЭМ, выделяют три варианта течения ОРЭМ: [1] монофазное, [2] возвратное и [3] мультифазное. ОРЭМ с монофазным течением характеризуется одним эпизодом неврологического нарушения с последующим разрешением заболевания. Для возвратного РЭМ характерным является появление или нарастание тех же симптомов, которые были во время дебюта заболевания через 3 месяца после начала первой атаки или после 30 дней после последней дозы кортикостероидов. Мультифазный РЭМ представляет собой развитие последующего обострения ОРЭМ с новыми жалобами и симптомами через 3 месяца после первой атаки заболевания или после 30 дней после последней дозы кортикостероидов. Считается, что случаи мультифазного ОРЭМ коррелируют с более старшим возрастом начала заболевания.
Эти «хронические» варианты ОРЭМ (возвратный и мультифазный), как и огран ченные формы (миелиты или стволовые энцефалиты) с волнообразным течением в ряде случаев требуют длительного динамического наблюдения с проведением МРТ для исключения такого необычного начала РС.
Прогноз при ОРЭМ в большинстве случаев благоприятный. У 70 — 90% пациентов наблюдается монофазное течение, и у 70 — 90% этих больных симптомы полностью регрессируют в течение 6 месяцев от начала заболевания, что объясняется процессами ремиелинизации. Возможны исходы с остаточным неврологическим дефицитом, вплоть до глубокой инвалидизации, что, возможно, происходит вследствие аксонального повреждения. Поздний возраст начала является фактором риска повторного обострения и трансформации в РС (вследствие чего таким пациентам рекомендовано наблюдение в специализированном центре по демиелинизирующим заболеваниям).
Диагностика ОРЭМ основывается преимущественно на результатах нейровизуализации. В настоящее время клинический анализ ОРЭМ обычно дополняется проведением МРТ (КТ малоинформативна для ОРЭМ, хотя примерно в половине случаев возможно выявление гиподенсивных очагов у больных с данной патологией, особенно в тех случаях, когда участки демиелинизации в ЦНС занимают обширную площадь). МРТ-исследование является более чувствительным для выявления очагов демиелинизации в головном и спинном мозге. На Т2-взвешенных изображениях (Т2-ВИ) и на Fluid-Attenuated Inversion Recovery (FLAIR) в типичных случаях выявляются двусторонние, гомогенные или незначительно негомогенные участки усиления интенсивности сигнала, расположенные чаще несимметрично в глубинном белом веществе полушарий мозга, субкортикально и инфратенториально. Очаги при ОРЭМ варьируют по своим размерам, они могут быть достаточно мелкими (менее 1 см), округлой формы или же крупными (более 2 см), бесформенными. При этом разные по своим размерам и формам очаги часто могут присутствовать одновременно в ЦНС одного и того же пациента. Участки демиелинизации при ОРЭМ иногда достигают очень крупных размеров и могут иметь схожую МРТ-картину с опухолями ЦНС.
Одной из особенностей МРТ-картины ОРЭМ считается нечеткость границ очагов демиелинизации, в отличие от очагов при РС, где они имеют четкую очерченность. В 50% случаев перивентрикулярная зона при ОРЭМ остается неповрежденной. Замечено, что у детей перивентрикулярная зона в большинстве случаев остается интактной, в отличие от взрослых. При ОРЭМ в патологический процесс редко вовлекается мозолистое тело.
МРТ-картина ОРЭМ характеризуется обширным поражением белого вещества, в некоторых случаях можно увидеть вовлечение более 50% вещества головного мозга. И, наконец, наиболее специфичным для ОРЭМ является обнаружение очагов в подкорковой области и коре головного мозга. Они встречаются почти у 80% пациентов с ОРЭМ. У половины больных возможна регистрация очагов повреждения в области базальных ядер, а в 20 — 30% случаев обнаруживается симметричное двустороннее вовлечение таламуса ([смотреть] МРТ-скан) в патологический процесс.
Очаги демиелинзации в спинном мозге при ОРЭМ чаще поражают грудной отдел, на МРТ обнаруживаются достаточно крупные сливные интрамедуллярные очаги, которые имеют тенденцию к распространению на протяжении нескольких спинальных сегментов. Накопление контраста очагами демиелинизации при ОРЭМ наблюдается в 30 — 100% случаев и не имеет особого специфического характера. При ОРЭМ одномоментно все очаги или большинство из них могут накапливать контраст, что говорит об остром их возникновении в нервной системе в течение короткого времени. В крови больных приблизительно в половине случаев обнаруживается повышение СОЭ, возможно наличие и других признаков воспаления (лейкоцитоз, лимфопения, повышение СРБ у 35%), но они все выражены умеренно.
увеличить
Описано 4 варианта МРТ при ОРЭМ: [1] с малыми очагами (менее 5 мм); [2] с крупными, сливающимися или опухолеподобными очагами, часто с масс-эффектом и окружающим отеком; [3] с дополнительным симметричным вовлечением зрительных бугров; [4] с очагами кровоизлияния в больших очагах (вариант острого геморрагического энцефаломиелита).
читать статью: МРТ-диагностика многоочагового поражения головного мозга (на laesus-de-liro.livejournal.com) [читать]
Предлагается считать исчезновение или уменьшение очагов на МРТ через 6 месяцев после острого эпизода окончательным подтверждением диагноза ОРЭМ. Однако даже при нормализации МРТ- картины рекомендуется в течение 5 лет периодически осуществлять ее контроль.
Обратите внимание! Некоторые вирусные энцефалиты могут иметь сходную с ОРЭМ клиническую и нейро-визуализационную картину, а также сходные изменения в ликворе. В их числе флавивирусные (японский энцефалит, лихорадка Западного Нила) и герпетические энцефалиты (герпес-зостер, Эпштейна–Барр, простой герпес, а также несеротипируемые вирусы герпеса).
Критерии диагностики ОРЭМ у взрослых (2008):
■ подострая энцефалопатия (нарушение сознания, поведения, когнитивных функций);
■ развитие симптомов от 1 недели до 3 месяцев; появление новых симптомов в течение 3 месяцев от начала заболевания допускается с условием, что они не разделены от первых симптомов периодом полной ремиссии;
■ сопровождается выздоровлением или улучшением; возможен остаточный неврологический дефицит;
■ на МРТ выявляются очаги, вызывающие неврологическую симптоматику: [1] активные очаги; [2] множественные очаги, редко одиночный крупный очаг; [3] супра- или инфратенториальная локализация, возможно их сочетание; [4] обычно визуализируется 1 крупный (>2 см) очаг; [5] контрастирование не обязательно; [6] возможно поражение базальных ганглиев, но не обязательно.
читать статью: Диагностические критерии рассеянного склероза (на laesus-de-liro.livejournal.com) [читать]
Терапия ОРЭМ должна начинаться максимально рано, так как отсроченное начало лечения приводит к ухудшению прогноза. Терапия (! патогенетическая — подавление избыточного ответа иммунной системы) основана на назначении кортикостероидов — метилпреднизолон 10 — 30 мг/кг/сутки или до максимальной дозы 1 г в сутки в течение 3 — 5 дней. Альтернативой метилпреднизолону может быть дексаметазон ([у взрослых] внутривенно струйно медленно в 10 — 20 мл изотонического раствора натрия хлорида или капельно в 100 мл изотонического раствора натрия хлорида 4 раза в сутки в течение 8 дней в дозе: с 1-го по 4-й день — 16 — 40 мг/сут.; с 5-го по 8-й день — 8-20 мг/сут.; далее с 9-го по 12-й день дексаметазон вводится внутримышечно по 4 — 12 мг 1 — 3 раза в сутки; с 13-го дня препарат отменяют или постепенно снижают дозу препарата на 4 мг через день). Однако следует учитывать тот факт, что в исследованиях применение метилпреднизолона показывало лучший результат в оценке степени инвалидизации. При положительной динамике по завершению курса инфузий метилпреднизолона назначается преднизолон 0,5 — 1 мг/кг/сутки с приемом per os через день в течение 3 — 6 недель.
При наличии бактериального триггера или ассоциации ОРЭМ с бактериальным инфекционным процессом, в случае бактериальных осложнений или для их профилактики необходимо использовать антибиотики. При установлении вирусной природы триггерного фактора или выявления хронического персистирования вирусов в организме целесообразно использовать препараты a-интерферона или интерфероногенов.
При отсутствии динамики после курса метилпреднизолона назначается курс плазмафереза или иммуноглобулины. Плазмаферез — курс из 4 — 6 сеансов, выполняемых через день или ежедневно. Показания: неэффективность пульс-терапии стероидами. Внутривенный иммуноглобулин (или иммуноглобулин для внутривенного введения — ВВИГ) назначается в качестве альтернативы плазмаферезу. Доза ВВИГ составляет 0,2 — 0,4 г/кг/сутки в течение 5 дней.
В случаях отсутствия положительного ответа на плазмаферез и ВВИГ следующим этапом обосновано назначение иммуносупрессивной терапии митоксантроном. Митоксантрон 10 мг/м2 , растворенный в 250 мл физиологического раствора в/в. Инфузии проводят сначала с частотой 3 раза и промежутками в 4 недели, затем проводят поддерживающее лечение в течение 3 месяцев. Максимальная общая доза — 100 мг/м2 . Предусмотреть профилактическое применение противорвотных средств. После введения: регулярный контроль анализа крови (каждые 3 — 4 дня) до достижения наименьшего уровня лейкоцитов в течение 10 — 14 дней после введения и регистрация нового нарастания лейкоцитов перед новым введением митоксантрона.
При невозможности назначения митоксантрона следует рассмотреть как альтернативу препараты циклофосфамид или азатиоприн. Циклофосфамид назначается из расчета 0,05 — 0,1 г/сутки (1 — 1,5 мг/кг/сутки), при хорошей переносимости до 3 — 4 мг/кг в/в капельно 1 раз в 3 — 4 недели. Продолжительность курса индивидуальна. Азатиоприн назначается из расчета по 1,5 — 2 мг/кг/сутки в 3 — 4 приема. В случае необходимости суточная доза может быть увеличена до 200 — 250 мг в 2 — 4 приема. Длительность курса лечения устанавливается индивидуально.
Литература: 1. клинический протокол диагностики и лечения «Острый рассеянный энцефаломиелит» одобрено Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения и социального развития Республики Казахстан от «29» ноября 2016 года (Протокол № 16) [читать]; 2. статья «Случай позднего развития острого рассеянного энцефаломиелита (клиническое наблюдение)» И.Ф. Хафизова, Н.А. Попова, Э.З. Якупов, ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России, Казань, Россия (журнал «Вестник современной клинической медицины» 2014 Том 7, приложение 2) [читать]; 3. статья «Диагностика, дифференциальная диагностика и принципы терапии острого рассеянного энцефаломиелита» Н.Н. Спирин, И.О. Степанов, Д.С. Касаткин, Е.Г. Шипова; ГОУ ВПО Ярославская государственная медицинская академия Росздрава; МУЗ Клиническая больница № 8, Ярославль (журнал «Неврология и ревматология» №2, 2008; портал «Consilium Medicum») [читать]; 4. статья «Острый рассеянный энцефаломиелит и рассеянный склероз: открытые вопросы дифференциальной диагностики на примере клинического случая» М.В. Мельников, О.В. Бойко, Н.Ю. Лащ, Е.В. Попова, М.Ю. Мартынов, А.Н. Бойко; Кафедра неврологии и нейрохирургии Российского национального исследовательского медицинского университета им. Н.И. Пирогова; Московский городской центр рассеянного склероза на базе Городской клинической больницы №11, Москва (Журнал неврологии и психиатрии, 9, 2012; Вып. 2). [читать]
Источник