Клеточный фактор врожденного иммунитета
К клеточным факторам врожденного иммунитета относят все фагоциты, объединенные в единую мононуклеарную фагоцитирующую систему. В нее включены:
макрофаги ¾ это фиксированные или тканевые, например, альвеолярные, перитонеальные клетки, эпидермоциты кожи (клетки Лангерганса и Гренстейна), звездчатые ретикулоэндотелиоциты в печени (клетки Купфера) и подвижные мигрирующие макрофаги (моноциты);
микрофаги ¾ полиморфно-ядерные лейкоциты (нейтрофилы, базофилы, эозинофилы) или циркулирующие микрофаги.
Микрофаги способны захватывать частички не менее 0,1 мк; макрофаги могуг поглощать молекулы биополимеров, вирусы (размеры меньше 0,1 мк).
Функции фагоцитов:
1) удаляют из организма отмирающие клетки и их структуры (эритроциты, раковые клетки);
2) удаляют неметабилизируемые неорганические вещества, попадающие во внутреннюю среду организма тем или иным путем (например, частички угля, минеральную и другую пыль, проникающую в дыхательные пути);
3) поглощают и инактивируют микробы (бактерии, вирусы, грибы);
4) синтезируют разнообразные биологически активные вещества, необходимые для обеспечения резистентности организма (некоторые компоненты комплемента, лизоцим, интерферон, интерлейкины и др.);
5) участвуют в регуляции иммунной системы;
6) осуществляют «презентацию» антигенов Т-хелперам, т. е. участвуют в кооперации иммунокомпетентных клеток.
Фагоцитоз(от греч. phages ¾ пожираю, cytos ¾ клетка) ¾ процесс, открытый и изученный И. И. Мечниковым (Нобелевская премия 1908 года), обеспечивает резистентность организма, защиту от инородных веществ, в том числе микробов. Это наиболее древняя форма иммунной защиты, которая появилась уже у кишечнополостных организмов. Механизм фагоцитоза состоит в поглощении, переваривании, инактивации инородных для организма веществ специализированными клетками — фагоцитами.
Стадии фагоцитоза:
1) хемотаксис (от греч. chymeia — искусство сплавления металлов и taxis — расположение, построение)- фагоциты способны активно перемещаться к объекту фагоцитоза по градиенту концентрации особых биологически активных веществ хемоаттрактантов. Это АТФ-зависимый процесс, в котором участвуют сократительные белки актин и миозин. К числу хемоаттрактантов относятся, например, фрагменты компонентов комплемента (СЗа и С5а), интерлейкин 8, продукты распада клеток и бактерий.
2) адсорбция микроорганизмов на поверхности фагоцита осуществляется за счет слабых химических взаимодействий и происходит либо спонтанно, неспецифически, либо путем связывания со специфическими рецепторами (к иммуноглобулинам, компонентам комплемента). Кроме того, поверхность бактерий имеет гидрофобные группы, которые способствуют их взаимодействию с рецепторами фагоцитов.
3) поглощение объекта путем инвагинации клеточной мембраны с образованием в протоплазме фагосомы, содержащей поглощенный объект. Поглощение адсорбированного на фагоците вещества происходит путем эндоцитоза. Это энергозависимый процесс, связанный с преобразованием энергии химических связей молекулы АТФ в сократительную активность внутриклеточного актина и миозина. Фагоцитируемый объект окружается цитоплазматической мембраной и образуется внутриклеточная вакуоль ¾ фагосома.
4) слияние фагосомы с лизосомой клетки с образованием фаголизосомы;
5) киллинг (уничтожение жизнеспособных микробов), осуществляемый при участии кислородзависимых и кислороднезависимых механизмов, и переваривание (процессинг) объекта в фаголизосоме с помощью протеаз, нуклеаз и др.;
6) презентация (представление) антигенных пептидов Т-хелперам ¾ антигенные пептиды в цитоплазме макрофага образуют комплекс с молекулами II класса главного комплекса гистосовместимости, которые перемещаются на поверхность клетки и, в последующем, связываются с соответствующими рецепторами Т-хелперов.
Различают завершенный и незавершенный фагоцитоз. Завершенным фагоцитоз считается в том случае, если произошли все стадии процесса. Однако в ряде случаев фагоцитоз носит незавершенный характер: поглощенные бактерии (например, иерсинии), вирусы (например, возбудитель ВИЧ-инфекции, натуральной оспы), риккетсии блокируют ферментативную активность фагоцита, не погибают, не разрушаются и даже размножаются в фагоцитах. Такой процесс получил название незавершенный фагоцитоз.
Источник
Иммунитет — (лат. immunitas — освобождение) — защита организма от генетически чужеродных организмов и веществ, к которым относятся микроорганизмы, вирусы, черви, различные белки, клетки, в том числе и собственные изменённые клетки организма.
Иммунология — наука, изучающая иммунитет.
Иммунный ответ — это реакция организма на внедрение чужеродных агентов.
Антиген — любое чужеродное вещество или организм.
Антитело — вещество организма, распознающее антигены.
Антитела (иммуноглобулины) — особый класс гликопротеинов, присутствующих на поверхности B-лимфоцитов в виде рецепторов (рис. 1). Реагируя на присутствие антигена, они отделяются от мембраны В-лимфоцита и присутствуют в сыворотке крови и тканевой жидкости в виде растворимых молекул (антител). Антитела способны избирательно связываться с конкретными видами чужеродных молекул, которые в связи с этим называют антигенами.

Рис. 1. В-лимфоцит с мембрансвязанными рецепторами
Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов.
Антигены, как правило, являются белками или полисахаридами и представляют собой части бактериальных клеток, вирусов и других микроорганизмов.
К антигенам немикробного происхождения относятся белки пыльцы растений, яичный белок и белки трансплантатов тканей и органов, а также поверхностные белки клеток крови при переливании крови.
Аллергены — это антигены, вызывающие аллергические реакции.
История изучения иммунитета
Фундамент иммунологии был заложен изобретением микроскопа, благодаря чему удалось обнаружить первую группу микроорганизмов — болезнетворные бактерии.
В конце XVIII в. английский сельский врач Эдвард Дженнер сообщил о первой удачной попытке предотвратить заболевание посредством иммунизации. Его подход вырос из наблюдений за одним интересным явлением: доярки часто заражались коровьей оспой и впоследствии не болели натуральной оспой. Дженнер ввёл маленькому мальчику гной, взятый из пустулы (нарыва) коровьей оспы, и убедился в том, что мальчик оказался иммунным к натуральной оспе.
Работа Дженнера дала начало изучению теории микробного происхождения заболеваний в XIX в. Пастером во Франции и Кохом в Германии. Они отыскали антибактериальные факторы в крови животных, иммунизированных микробными клетками.
Луи Пастер успешно выращивал различные микробы в лабораторных условиях. Как часто бывает в науке, открытие было сделано случайно при культивировании возбудителей холеры кур. Во время работы одна из чашек с микробами была забыта на лабораторном столе. Было лето. Микробы в чашке несколько раз нагревались под солнечными лучами, высохли и потеряли способность вызывать заболевание. Однако куры, получившие эти неполноценные клетки, оказались защищёнными против свежей культуры холерных бактерий. Ослабленные бактерии не только не вызывали заболевание, а, напротив, давали иммунитет.
В 1881 г. Луи Пастер разработал принципы создания вакцин из ослабленных микроорганизмов с целью предупреждения развития инфекционных заболеваний.
В 1908 г. Илья Ильич Мечников и Пауль Эрлих были удостоены Нобелевской премии за работы по теории иммунитета.
И. И. Мечников создал клеточную (фагоцитарную) теорию иммунитета, согласно которой решающая роль в антибактериальном иммунитете принадлежит фагоцитозу.
Сначала И. И. Мечников как зоолог экспериментально изучал морских беспозвоночных фауны Чёрного моря в Одессе и обратил внимание на то, что определённые клетки (целомоциты) этих животных поглощают все инородные частицы (в т. ч. бактерии), проникающие во внутреннюю среду. Затем он увидел аналогию между этим явлением и поглощением белыми клетками крови позвоночных животных микробных телец. И. И. Мечников осознал, что это явление не питание данной единичной клетки, а защитный процесс в интересах целого организма. Учёный назвал действующие таким образом защитные клетки фагоцитами — «пожирающими клетками». И. И. Мечников первым рассматривал воспаление как защитное, а не разрушительное явление.
Против теории И. И. Мечникова в начале XX в. выступали большинство патологов, так как они считали лейкоциты (гной) болезнетворными клетками, а фагоциты — разносчиками инфекции по организму. Однако работы И. И. Мечникова поддержал Луи Пастер. Он пригласил И. И. Мечникова работать в свой институт в Париже.
Пауль Эрлих открыл антитела и создал гуморальную теорию иммунитета, установив, что антитела передаются ребёнку с грудным молоком, создавая пассивный иммунитет. Эрлих разработал метод изготовления дифтерийного антитоксина, благодаря чему были спасены миллионы детских жизней.
Теория иммунитета Эрлиха говорит о том, что на поверхности клеток есть специальные рецепторы, распознающие чужеродные вещества (антигенспецифические рецепторы). Сталкиваясь с чужеродными частицами (антигенами), эти рецепторы отсоединяются от клеток и в качестве свободных молекул выходят в кровь. В своей статье П. Эрлих назвал противомикробные вещества крови термином «антитело», так как бактерий в то время называли «микроскопические тельца».
П. Эрлих предполагал, что ещё до контакта с конкретным микробом в организме уже есть антитела в виде, который он назвал «боковыми цепями». Теперь известно, что он имел в виду рецепторы лимфоцитов для антигенов.
В 1908 г. Паулю Эрлиху вручили Нобелевскую премию за гуморальную теорию иммунитета.
Чуть раньше Карл Ландштейнер впервые доказал наличие иммунологических различий индивидуумов в пределах одного вида.
Питер Медавар доказал удивительную точность распознавания иммунными клетками чужеродных белков: они способны отличить чужеродную клетку всего по одному изменённому нуклеотиду.
Френк Бёрнет постулировал положение (аксиома Бёрнета), что центральным биологическим механизмом иммунитета является распознавание своего и чужого.
В 1960 г. Нобелевскую премию по физиологии и медицине получили Питер Медавар и Френк Бёрнет за открытие иммунологической толерантности (лат. tolerantia — терпение) — это распознавание и специфическая терпимость к некоторым антигенам.
Уничтожение генетически изменённых клеток
Одна из функций иммунной системы — это уничтожение генетически изменённых (мутантных) клеток организма. В процессе клеточного деления постоянно происходят ошибки, и одна из миллиона образовавшихся клеток становится мутантной, т. е. генетически чужеродной. В организме человека благодаря мутациям в каждый конкретный момент должно быть более 10 миллионов мутантных клеток. Мутации приводят к изменению функций клетки. Большинство мутантных клеток не способны выполнять свои функции, а многие выходят из-под контроля организма (например, при нарушении апоптоза) и становятся раковыми клетками. Появление таких клеток может привести к возникновению серьёзных заболеваний и гибели организма.
Один из механизмов иммунитета, осуществляемый лимфоцитами (НК-лимфоцитами), направлен на уничтожение именно раковых клеток.
Виды иммунитета
Иммунитет можно разделить на клеточный и гуморальный (рис. 2)
Рис. 2. Клеточный и гуморальный иммунитет
Все разнообразные формы иммунного ответа можно разделить на два типа: врождённый иммунитет и приобретённый иммунитет (рис. 3).
Рис. 3. Классификация иммунитета
Приобретённый иммунитет — это специфический индивидуальный иммунитет, т. е. это иммунитет, который имеется конкретно у определённых индивидуумов и к определённым возбудителям или агентам.
Главными характеристиками приобретённого иммунитета являются специфичность и иммунологическая память. Чем чаще организм встречается с патогеном, тем быстрее и активнее вырабатываются антитела, следовательно — сильнее защита.
Врождённый иммунитет с самого рождения (ещё до первой встречи с антигеном) защищает организм против всего чужеродного, т. е. он не специфичен.
Таким образом, повторная встреча с тем или иным патогенным микроорганизмом не приводит к изменениям врождённого иммунитета, но повышает уровень приобретённого.
Врождённый иммунитет активируется при первом появлении патогена быстрее, но распознаёт патоген с меньшей точностью. Он реагирует не на конкретные специфические антигены, а на определённые классы антигенов, характерные для патогенных организмов (белки вирусного капсида, продукты метаболизма глистов и т. п.).
Врождённый иммунитет может быть наследственным (видовым) и индивидуальным.
Наследственный (видовой) иммунитет — это невосприимчивость всех представителей данного вида к определённому антигену, приобретённая в процессе эволюции:
болезни, которыми болеет человек, но не болеют животные и птицы (корь, натуральная оспа, проказа, вирусный гепатит, холера, гонорея, дизентерия, брюшной тиф и др.);
болезни, которыми болеют животные, но не болеет человек (чума крупного рогатого скота, пироплазмоз собак);
болезни, которыми болеют птицы, но не болеет человек (куриная холера);
болезни, которыми болеют животные и человек, но не болеют птицы (сибирская язва, бешенство и др.).
Индивидуальный врождённый иммунитет определяется теми особенностями, которые передаются организму с родительскими генами и в процессе эмбрионального развития.
В процессе эмбрионального развития через плаценту плоду передаются антитела матери, которые противостоят инфекциям. Передача антител от мамы к ребёнку происходит в основном в последнем триместре беременности.
Иммунитет подразделяется на естественный и искусственный.
Естественный иммунитет возникает самостоятельно в процессе жизни организма.
Естественный иммунитет делится на активный (после перенесённых заболеваний) и пассивный (например, с молоком матери).
До 6 месяцев малыша защищают антитела, передающиеся от матери с грудным молоком. Поэтому важным является исключительно грудное вскармливание. Иммунитет матери защищает ребёнка. Дети, которые находятся на искусственном вскармливании, слабо защищены, т. к. собственных антител у них мало. Только к 6 месяцам организм самостоятельно начинает вырабатывать антитела. Собственный иммунитет ребёнка формируется только к концу первого года жизни.
Искусственный иммунитет организм приобретает в результате применения медицинских препаратов (вакцин и сывороток).
Вакцина — медицинский препарат, содержащий ослабленные или убитые микроорганизмы.
Вакцина вводится абсолютно (!) здоровому человеку для предотвращения заболевания в будущем.
Сыворотка — медицинский препарат плазмы крови без фибриногена, содержащий готовые антитела к определённому патогену (заражающему микроорганизму). Сыворотку получают из крови заражённого данным заболеванием животного (коровы, лошади и т. п.).
Сыворотка с чужими антителами вводится заболевшему человеку в случае, когда организм не способен произвести достаточное количество антител.
Источник
Врождённый
иммунитет — наиболее ранний защитный
механизм как в эволюционном плане (он
существует практически у всех
многоклеточных), так и по времени ответа,
развивающегося в первые часы и дни после
проникновения чужеродного материала
во внутреннюю среду, т.е. задолго до
развития адаптивной иммунной реакции.
Значительную часть патогенов инактивируют
именно врождённые механизмы иммунитета,
не доводя процесс до развития иммунного
ответа с участием лимфоцитов. И только
если механизмы врождённого иммунитета
не справляются с проникающими в организм
патогенами, в «игру» включаются лимфоциты.
При этом адаптивный иммунный ответ
невозможен без вовлечения механизмов
врождённого иммунитета. Кроме того,
врождённый иммунитет играет главную
роль в удалении апоптотических и
некротических клеток и реконструировании
повреждённых органов. В механизмах
врождённой защиты организма важнейшую
роль играют первичные рецепторы для
патогенов, система комплемента, фагоцитоз,
эндогенные пептиды-антибиотики и факторы
защиты от вирусов — интерфероны. Функции
врождённого иммунитета схематично
представлены на рис. 3-1.
Рецепторы распознавания «чужого»
На
поверхности микроорганизмов
присутствуют повторяющиеся
молекулярные углеводные и липидные
структуры, которые
в подавляющем большинстве случаев
отсутствуют на клетках организма
хозяина. Особые рецепторы, распознающие
этот «узор» на поверхности патогена, —
PRR (Pattern
Recognition Receptors –РRP-рецептор)
— позволяют клеткам врождённого иммунитета
обнаруживать микробные клетки. В
зависимости от локализации выделяют
растворимые и мембранные формы PRR.
• Циркулирующие
(растворимые) рецепторы для
патогенов — белки сыворотки крови,
синтезируемые печенью: липополисахаридсвязывающий
белок (LBP — Lipopolysaccharide
Binding Protein), компонент
системы комплемента C1q и белки острой
фазы MBL и С-реактивный белок (СРБ). Они
непосредственно связывают микробные
продукты в жидких средах организма и
обеспечивают возможность их поглощения
фагоцитами, т.е. являются опсонинами.
Кроме того, некоторые из них активируют
систему комплемента.
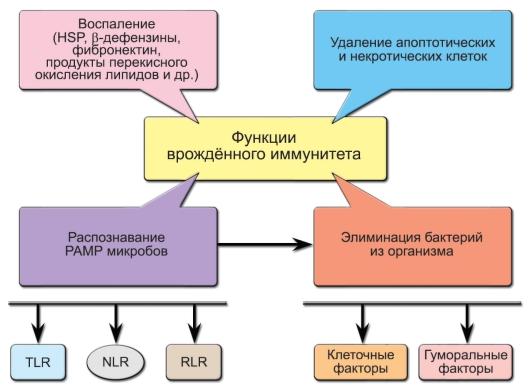
Рис.
3-1. Функции
врождённого иммунитета. Обозначения:
PAMP (PathogenAssociated
Molecular Patterns) —
молекулярные структуры микроорганизмов,
HSP (Heat
Shock Proteins) —
белки теплового шока, TLR (Toll-Like
Receptors), NLR (NOD-Like
Receptors), RLR (RIG-Like
Receptors) —
клеточные рецепторы
— СРБ, связывая
фосфорилхолин клеточных стенок ряда
бактерий и одноклеточных грибов,
опсонизирует их и активирует систему
комплемента по классическому пути.
— MBL принадлежит
к семейству коллектинов. Имея сродство
к остаткам маннозы, экспонированным на
поверхности многих микробных клеток,
MBL запускает лектиновый путь активации
комплемента.
— Белки
сурфактанта лёгких — SP-A и SP-D принадлежат
к тому же молекулярному семейству
коллектинов, что и MBL. Они, вероятно,
имеют значение в опсонизации (связывании
антител с клеточной стенкой микроорганизма)
лёгочного патогена — одноклеточного
грибка Pneumocystis
carinii.
• Мембранные
рецепторы. Эти
рецепторы расположены как на наружных,
так и на внутренних мембранных структурах
клеток.
— TLR (Toll-Like
Receptor —
Toll-подобный рецептор; т.е. сходный с
Toll-рецептором дрозофилы). Одни из них
непосредственно связывают продукты
патогенов (рецепторы для маннозы
макрофагов, TLR дендритных и других
клеток), другие работают совместно с
иными рецепторами: например, CD14 молекула
на макрофагах связывает комплексы
бактериального липополисахарида (ЛПС)
с LBP, а TLR-4 вступает во взаимодействие с
CD14 и передаёт соответствующий сигнал
внутрь клетки. Всего у млекопитающих
описано 13 различных вариантов TLR (у
человека пока только 10).
• Цитоплазматические
рецепторы:
— NOD-рецепторы (NOD1
и NOD2) находятся в цитозоле и состоят из
трёх доменов: N-концевого CARD-домена,
центрального NOD-домена (NOD — Nucleotide
Oligomerization Domain —
домен олигомеризации нуклеотидов) и
C-концевого LRR-домена. Различие между
этими рецепторами заключается в
количестве CARD-доменов. Рецепторы NOD1 и
NOD2 распознают мурамилпептиды — вещества,
образующиеся после ферментативного
гидролиза пептидогликана, входящего в
состав клеточной стенки всех бактерий.
NOD1 распознаёт мурамилпептиды с концевой
мезодиаминопимелиновой кислотой
(meso-DAP), которые образуются только из
пептидогликана грамотрицательных
бактерий. NOD2 распознаёт мурамилдипептиды
(мурамилдипептид и гликозилированный
мурамилдипептид) с концевым D-изоглутамином
или D-глутаминовой кислотой, являющиеся
результатом гидролиза пептидогликана
как грамположительных, так и
грамотрицательных бактерий. Кроме того,
NOD2 имеет сродство к мурамилпептидам с
концевым L-лизином, которые есть только
у грамположительных бактерий.
— RIG-подобныерецепторы (RLR, RIG-Like
Receptors): RIG-I (Retinoic
acid-Inducible Gene I),
MDA5 (Melanoma
Differentiation-associated Antigen 5)
и
LGP2 (Laboratory
of Genetics and Physiology 2).
Все
три рецептора, кодируемые этими генами,
имеют сходную химическую структуру и
локализуются в цитозоле. Рецепторы
RIG-I и MDA5 распознают вирусную РНК. Роль
белка LGP2 пока неясна; возможно, он
выполняет роль хеликазы, связываясь с
двуцепочечной вирусной РНК, модифицирует
её, что облегчает последующее распознавание
с помощью RIG-I. RIG-I распознаёт односпиральную
РНК с 5-трифосфатом, а также относительно
короткие (<2000 пар оснований) двуспиральные
РНК. MDA5 различает длинные (>2000 пар
оснований) двуспиральные РНК. Таких
структур в цитоплазме эукариотической
клетки нет. Вклад RIG-I и MDA5 в распознавание
конкретных вирусов зависит от того,
образуют ли данные микроорганизмы
соответствующие формы РНК.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
