Методы оценки в системы иммунитета
(ГУМОРАЛЬНЫЙ ИММУНИТЕТ).
Гуморальный иммунный ответ обеспечивается антителами, или иммуноглобинами. У человека различают 5 основных классов иммуноглобинов: IgA, IgG, IgM, IgE, IgD. Все они имеют как общие, так и специфические детерминанты.
Иммуноглобины класса G.У человека являются наиболее важными. Концентрация их достигает 9-18 г/л. Иммуноглобины этого класса обеспечивают противоинфекционную защиту, связывают токсины, усиливают фагоцитарную активность, активируют систему комплемента, вызывают аглютинацию бактерий и вирусов, они способны переходить через плаценту, обеспечивая новорожденному так называемый пассивный иммунитет.
Иммуноглобины класса А. Делят на 2 разновидности: сывороточные и секреторные. Первые из них находятся в крови, вторые – в различных секретах. Соответственно этому сывороточный иммуноглобин А принимает участие в общем, иммунитете, а секреторный обеспечивает местный иммунитете, создавая барьер на пути проникновения инфекций и токсинов в организм.
Секреторный находится в наружных секретах – в слюне, слизи трахеобронхиального дерева, мочеполовых путей, молоке. Молекулы иммуноглобина А, присутствующие во внутренних секретах и жидкостях, существенно отличаются от молекул наружных секретов. Секреторный компонент, по всей видимости, образуется в эпителиальных клетках и в дальнейшем присоединяется к молекуле IgA.
IgA нейтрализует токсины и вызывает аглютинацию микроорганизмов и вирусов. Концентрация сывороточных IgA колеблется от 1,5 до 4 г/л.
Содержание IgA резко возрастает при заболеваниях верхних дыхательных путей, пневмониях, инфекционных заболеваниях желудочно-кишечного тракта и др.
Иммуноглобины класса Е.Принимают участие в нейтрализации токсинов, опсонизации, аглютинации и бактериолизисе, осуществляемом комплементом. К этому классу также относятся некоторые природные антитела, например к чужеродным эритроцитам. Содержание IgE повышается при инфекционных заболеваниях у взрослых и детей.
Иммуноглобины класса D.Представляют собой антитела, локализующиеся в мембране плазматических клеток, в сыворотке их концентрация невелика. Значение IgD пока не выяснено, предполагают, что они участвуют в аутоиммунных процессах.
Для оценки В-системы иммунитета применяется несколько методов.
1. Определение В-лимфоцитов в крови.
2. Определение в крови уровня иммуноглобулинов. Проводят определение суммарной концентрации иммуноглобулинов и количество иммуноглобулинов разных классов.
3. Определение наличия и уровня изогемагглютининов в сыворотке крови, а также естественных (нормальных) антител к широко распространенным бактериям и вирусам. В качестве антигенов можно использовать кишечную палочку, стафилококковые токсины, вирус герпеса и др. Следует отметить и иметь в виду, что альфа- и бета-изогемагглютинины относятся к Jg M.
4. Стимуляция биосинтеза иммуноглобулинов В-лимфоцитами in vitro.
5. Исследование антителогенеза (первичного и вторичного ответа) после активной иммунизации несколькими убитыми вакцинам .Применяют коклюшную и убитую полиомиелитную вакцины, дифтерийный и столбнячный анатоксин, полисахаридные антигены, выделенные из пневмококков, менингококков и бактерий кишечной группы.
6. Исследование катаболизма иммуноглобулинов в организме. В кровь вводят меченый препарат человеческого иммуноглобулина.
7. Биопсия лимфатических узлов, костного мозга, участков слизистой оболочки кишечника. Эту процедуру проводят с целью гистологического обнаружения плазматических клеток, наличие и структуры лимфоидных фолликулов.
8. Кожные реакции, выявляющие гиперчувствительность немедленного типа. К таким пробам относятся ШИК-реакция и другие.
Источник
. Иммунный статус. Влияние климато-географических,
социальных, экологических и медицинских факторов. Оценка иммунного статуса,
определение состояния гуморального и клеточного иммунитета. Основные показатели
и методы их определения.
Состояние функциональной активности иммунной системы
человека в целом имеет жизненно важное значение для организма и обозначается
понятием «иммунный статус».
Иммунный
статус это количественная и
качественная характеристика состояния функциональной активности органов
иммунной системы и некоторых неспецифических механизмов про-тивомикробной
защиты.
Влияние
факторов
Среди
климато-географических факторов на иммунный статус оказывают влияние
температура,влажность, солнечная радиация, длина светового дня и т.д.Например:
фагоцитарная активность и кожные аллергические пробы менее выражены у жителей
северных районов, чем у южан.Вирус Эпштейна Барр у людей белой расы вызывает
инфекционное заболевание-мононуклеоз а у лиц негроидной расы онкопатологию и
т.д.Жители Африки менее подвержены заб дифтерии чем европейское население.
К
социальным факторам относятся питание, жилищно-бытовые условия,
профессиональные вредности и т.д. Важное значение имеет сбалансированное и
рациональное питание.
Экологические
факторы:загрязнение окружающей среды радиоактивными веществами, широкое
применение пестицидов в сельском хозяйстве, выбросами химических предприятий и
автотранспорта.
Медицинские
факторы: диагностические и лечебные медицинские манипуляции лекарственные
средства стресс.например рентгенография, травмы,операции,антибиотики. Стресс
приводит к нарушениям в работе Т-системы иммунитета действуя в первую очередь
через ЦНС.
Оценка
иммунного статуса
Можно
определить путем постановки комплекса лабороторных тестов включающих оценку
состояния факторов неспецифической резистентности гуморального(В-система) и
клеточного(Т-система)иммунитета.Оценка иммунного статуса проводится в клинике
при трансплантации органов и тканей аутоиммунных заболеваний аллергиях для
выявления иммунологической недостаточности при различных заболеваниях для
контроля эффективности лечения болезней связанных с нарушениями иммунной
системы.В зависимости от возможностей лаборотории оценка иммунного статуса чаще
всего базируется на определении комплекса следующих показателей:1.общего
клинического обследования2.состояния факторов естественной
резистентности3.гуморального иммунитета4.клеточного иммунитета5.дополнительных
тестов.При общем клиническом обследовании учитывают жалобы пациента
анамнез клинические симптомы результаты общего анализа крови,данные
биохимического исследования(спрашивают у пациента наличие профессиональных
вредностей,аллергии,инфекции, перенесенные в детстве заболевания,о
травмах,операциях,о лекарственных препаратах которые принимает,при осмотре
обращают внимание на чистоту кожных покровов и слизистых,при пальпации и
перкуссии уделяют внимание тимусу лимфатич узлам селезенке,обследуют анализ
крови о состоянии иммунокомпетентных клеток(лимфоциты,фагоциты). При
оценке состояния факторов резистентности определяют фагоцитоз компемент
интерфероновый статус колонизационную резистентность. Функциональную активность
фагоцитов определяют по их подвижности, адгезии,поглощению,расщеплению
захваченный частиц, образованию активных форм кислорода. С этой целью
используют такие тесты как определение фагоцитарного индекса,НСТ-тест и
др.Состояние системы комплемента определяют в реакции гемолиза. Интерфероновый
статус выявляют путем трирования на культуре клеток уровня интерферона в
сыворотке крови. Колонизационную резистентность определяют по степени дисбиоза
различных биотопов организма(чаще толстой кишки)
Гуморальный иммунитетопределяют по уровню иммуноглобулинов классов G,M,A.D,E в сыворотке крови количеству специфических антител,
катаболизму иммуноглобулинов, ГНТ, показателю В-лимфоцитов в переферической
крови и т.д. Для определения концентрации иммуноглобулинов в сыворотке крови
обычно используют иммунодиффузию по Манчини.Титр специфических антител
определяют в различных иммунологических реакциях(агглютинация, РПГА, ИФА и др.)
Число В-лимфоцитов устанавливают путем определения специфических рецепторов на
клетках с помощ моноклональных антител. фУнкциональное состояние В-лимфоцитов
определяют в реакции бласттрансформации путем стимуляции клеток митогенами,
например туберкулин и др. При оптимальных условиях культивирования В-лимф с
митогенами показатель трансформации в бласты может достигать 80%.Подсчет
бластов производят под микроскопом . Состояние клеточного иммунитетаоценивают по количеству Т-лимфоцитов а
также субпопуляций Т-лимфоцитов в периферической крови, бласттрансформации
Т-лимф под действием Т-клеточных митогенов, определению гормонов тимуса, уровню
цитокинов, а также кожные пробы с аллергенами. Для постановки кожных
аллергических проб с используются антигены, к которым в норме должна быть
сенсибилизация, например проба Манту с туберкулином. Для определения числа
Т-лимфоцитов в периферической крови используют реакцию розеткообразования Е-РОК
поскольку эритроциты барана образуют с Т-лимфоцитами спонтанные розетки.
Бласттрансформацию Т-лимфоцитов определяют путем стимуляции Т-клеточными
митогенами. Для оценки состояния функции тимуса чаще всего применяют
определение уровня α1-тимозина и тимулина. В качестве дополнительных тестов для
оценки иммунного статуса можно использовать такие тесты как определение
бактерицидности сыворотки крови, титрование С3, С4 компонентов комплемента,
определение содержания С-реактивного белка в сыворотке крови. Все тесты
разделены на две группы: Тесты 1-го уровня могут быть выполнены в любой
клинической иммунологической лаборотории первичного звена здравоохранения, они
используются для первичного выявления лиц с явно выраженной иммунопатологией.
Они вкяючают в себя определение:
‘
общего и относительного числа лимфоцитов;
—основных субпопуляций (Т- и В-клетки);
—фагоцитарной активности лейкоцитов;
—концентрации иммуноглобулинов разных классов в
сыворотке крови.
Общее
(абсолютное) и относительное число лимфоцитов определяют по данным клинического
анализа крови. Содержание Т- и B-лимфоцитов подсчитывают в реакции
иммунофлюорес-ценции, используя меченые моноклональные флюоресцирующие
сыворотки к специфическим поверхностиым антигенным маркерам,
обозначаемым
символами CD(clasterdifferentiation). Таких
антигенных маркеров известно несколько десятков, но отдельные из них
характерны для того или иного типа клеток:
•
рецептор CD3 — всех ‘Г-лимфоцитов;
•
рецепторы CD 19, 20. 21, 72 — В-лимфоцитов;
•
рецепторы CD4 — Т-хелперы;
•
рецепторы CD8 — Т-супрессоры;
•
рецепторы CD 16 — NK-клетки
(натуральные киллеры).
Для более точной диагностики используются
тесты 2-го уровня позволяют провести более глубокий анализ состояния иммунной
системы и уточнить характер дефектов, выявленных с помощью тестов 1-го уровня.
К ним относятся, например, определение отдельных субклассов иммуноглобулинов
(особенно IgG, секреторного IgA) и B-лимфоцитов, регу-ляторных и эффекторных клеток.
Кроме того,
с помощью иммуноферментных и радиоиммунных методов можно определить
концентрации отдельных цитоки-нов главных регуляторных молекул,
определяющих тип иммунного ответа.
Источник
Иммунный статус (ИС) – совокупность количественных и функциональных показателей, отражающих состояние иммунной системы человека в данный момент времени. Это понятие введено для объективной оценки состояния иммунной системы человека. Изучение показателей иммунитета при иммунных нарушениях должно включать исследования количества и функциональной активности основных компонентов иммунной системы. Все нарушения функции иммунной системы классифицируют, исходя из проявлений различных заболеваний. Выделяют первичные и вторичные иммунодефициты, аутоиммунные, аллергические и лимфопролиферативные заболевания.
Для оценки функционирования всех компонентов иммунной системы, Т и В системы иммунитета, фагоцитарной и системы комплемента, должны быть включены количественные и функциональные методы. Для оценки гуморального звена иммунитета выполняют следующие исследования: определение продукции иммуноглобулинов разных классов в сыворотке крови; определение относительного и абсолютного содержания В-лимфоцитов и их субпопуляций, компонентов комплемента и циркулирующих иммунных комплексов, функциональные тесты (реакция бласттрансформации с митогенами), определение специфических антител, кожные пробы.
Для оценки Т-клеточного звена проводят исследования с определением относительного и абсолютного количества Т-лимфоцитов и их субпопуляций (Т-хелперов, ЦТЛ), натуральных киллеров, их активационных маркеров, функциональные тесты (реакция бласт-трансформации с митогенами), определение продукции цитокинов.
Состояния фагоцитарной системы оценивают по многим тестам: адгезивная способность нейтрофилов по прилипанию к волокнам нейлона; миграция, хемотаксис в реакции торможения миграции нейтрофилов; метаболическая активность и образование активных форм кислорода по восстановлению нитросинего тетразолия; фагоцитарная активность нейтрофилов в тестах спонтанного и стимулированного микробными полисахаридами фагоцитоза; иммунофенотипирование нейтрофилов.
Ранее эти методы были разделены на тесты 1-го и 2-го уровня. Тесты 1-го уровня являются ориентировочными и направлены на выявление грубых дефектов в иммунной системе. Тесты 2-го уровня направлены на идентификацию конкретной “поломки” в иммунной системе.
Тесты 1-го уровня
- определение относительного и абсолютного количества лейкоцитов, нейтрофилов, моноцитов, лимфоцитов и тромбоцитов периферической крови;
- определение функциональной активности нейтрофилов (НСТ тест);
- тесты иммунофенотипирования для определения относительного и абсолютного количества Т- и В-лимфоцитов, натуральных киллеров;
- определение концентрации иммуноглобулинов основных классов (IgA, IgM, IgG, IgE);
- определение гемолитической активности комплемента.
С помощью минимального набора тестов можно диагностировать первичные иммунодефициты: хроническую грануломатозную болезнь, Х-сцепленную агамма-глобулинемию, гипер–IgM–синдром, селективный дефицит IgA, синдром Вискотта-Олдрича, тяжелый комбинированный иммунодефицит.
Тесты 2-го уровня
- тесты иммунофенотипирования для определения относительного и абсолютного количества популяций и субпопуляций Т-, В-, NK-лимфоцитов;
- активационные маркеры лимфоцитов;
- оценка различных этапов фагоцитоза и рецепторного аппарата фагоцитарных клеток;
- определение основных классов и подклассов иммуноглобулинов;
- циркулирующие иммунные комплексы;
- определение концентрации компонентов комплемента в сыворотке крови (С3, С4, С5, С1-ингибитор);
- функциональная активность различных субпопуляций лимфоцитов;
- оценка пролиферативной активности Т- и В-лимфоцитов;
- исследование интерферонового статуса;
- кожные пробы и т.д.
Набор полученных показателей при иммунологическом обследовании называется иммунограммой.
Следует особо подчеркнуть, что полноценный анализ иммунограммы возможен только в комплексе с клиническим состоянием и анамнезом пациента. Отсутствие характерных сдвигов в иммунограмме при выраженных клинических симптомах следует считать атипичной реакцией иммунной системы, что является отягощающим признаком заболевания. Полученные данные пациента сравниваются со средними значениями для данного аналита, полученными в регионе проживания пациента. Среднестатистические показатели различаются в зависимости от региона и подчиняются климатогеографическим условиям, экологической обстановке, условиям жизни. Необходимо также учитывать возраст пациента и циркадные ритмы.
Исследование показателей ИС имеет большое значение для диагностики и дифференциальной диагностики, особенно при первичных иммунодефицитах и лимфопролиферативных заболеваниях, для оценки тяжести, активности, длительности течения и прогноза различный заболеваний, оценки эффективности проводимого лечения.
Источник
Для оценки В-системы иммунитета применяют несколько методов.
Определение В-лимфоцитов в крови. Используют три свойства лимфоцитов этого типа.
Наличиерецепторов к комплементу дает возможность подсчитать так называемые комплементарные розетки, т.е. лимфоциты, образующие розетки с эритроцитами, несущими на своей поверхности комплекс антитело — комплемент (ЕАС-розеткообразование). К розеткообразованию способны не только лимфоциты, но и гранулоциты. И. Вонг, А. Уилсон в 1975 г. описали технику постановки ЕА- и ЕАС-розеткообразования нейтрофилами, что доказало наличие у этих клеток Fс-рецепторов. В 1976 г. И. В. Петрова и соавт. описали способность нейтрофилов к спонтанному розеткообразованию с эритроцитами барана и было показано, что эта субпопуляция нейтрофилов резко возрастает при иммунодепрессивной терапии. По аналогии с лимфо- цитами нейтрофилы делят на спонтанные розеткообразующие клетки, комплементарные розеткообразующие клетки и нулевые. У здоровых людей спонтанных розеткообразующих нейтрофилов имеется от 25 до 35%, а комплементарных — от 14 до 20%.
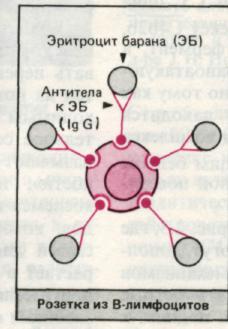
рис. 1. Розеткообразование В- клеток.
Наличие у В-лимфоцитов рецепторов к Fс-фрагменту иммуноглобулинов приводит к тому, что они адсорбируют на себе агрегированный γ-глобулин. Выявить В-лимфоциты можно с помощью флюоресцентного или радиографического метода, используя меченые агрегаты γ-глобулинов. Человеческие В-лимфоциты образуют розетки с мышиными эритроцитами. Наконец, с помощью иммунофлюоресцентного метода Кунса, применяя антиглобулиновые сыворотки, можно обнаружить и подсчитать все лимфоциты, несущие иммуноглобулиновые детерминанты, т. е. В-лимфоциты. При этом можно провести дифференцированный подсчет клеток, несущих IgМ-, IgG или 1gА-детерминанты. Так же необходимо определять не только процент В-клеток, но и их абсолютное количество в 1 мкл крови.
Определение в крови уровня иммуноглобулинов. Проводят определение суммарной концентрации иммуноглобулинов и количество иммуноглобулинов разных классов. Первое осуществляется методом высаливания сульфа-том цинка с последующей турбидиметрической оценкой, электрофорезом или иммуноэлектрофорезом. Нормальный уровень суммарных иммуноглобулинов у человека составляет от 10 до 20 г/л. Определение количества IgМ, IgG и IgА чаще всего осуществляется методом радиальной иммунодиффузии по Манчини. IgЕ определяется радиоиммунологическим методом. Верхняя граница нормы составляет 0,0005 г/л.
Определение наличия и уровня изогемагтлютининов в сыворотке крови, а также естественных (нормальных) антител к широко распространенным бактериям и вирусам. В качестве антигенов можно использовать кишечную палочку, стафилококковые токсины, вирус герпеса и др. Следует иметь в виду, что ά- и β-изогемагглютинины относятся к IgМ.
Исследование антителогенеза (первичного и вторичного ответа) после акти-вной иммунизации несколькими убитыми вакцинами. Применяют коклюшную и убитую полиомиелитную вакцины, дифтерийный и столбнячный анатоксины, полисахаридные антигены, выделенные из пневмококков, менингококков и бактерий кишечной группы. Необходимость использования нескольких антигенов связана с генетически детерминированной конкретностью иммунного ответа. Получение низкого иммунного ответа на какой-то один антиген может оказаться результатом того, что данный индивидуум относится к низкоотвечающему на данный антиген генотипу. Реакция на другие антигены может быть нормальной. Вот почему диагноз функциональной неполноценности В-системы можно поставить только при угнетении иммунного ответа на несколько разных антигенов.
Исследование катаболизма иммуноглобулинов в организме. В кровь вводят меченый препарат человеческого иммуноглобулина. Клиренс метки из крови и ее накопление в моче и испражнениях дают возможность определить период полужизни иммуноглобулина. В норме период полужизни IgG равен 24 дням. При экссудативной энтеропатии, нефрозах и некоторых других заболеваниях возникает состояние гиперкатаболизма иммуноглобулинов. Для установления факта избирательного их гиперкатаболизма параллельно определяют период полужизни меченого альбумина.
Биопсия лимфатических узлов, костного мозга, участков слизистой оболочки кишечника. Эту процедуру проводят с целью гистологического обнаружения плазматических клеток, наличия и структуры лимфоидных фолликулов. Кожные реакции, выявляющие гиперчувствительность немедленного типа. К таким пробам относится ШИК-реакция. У людей, иммунизированных против дифтерии, в организме которых содержатся антитела против дифтерийного токсина, внутрикожная инъекция этого токсина не приводит к развитию типичной эритемы.
Стимуляция биосинтеза иммуноглобулинов В-лимфоцитами in vitro. Оценка функциональной активности В-лимфоцитов из крови человека возможна благодаря тому, что некоторые митогены, например митоген лаконоса, обладают способностью вызывать поликлональную стимуляцию В-лимфоцитов. «Валовую» продукцию В-клеток, синтезирующих иммуногло-булины, определяют в культуральной жидкости радиоиммунологическим методом через 7—12 дней культивирования лимфоцитов с митогеном.
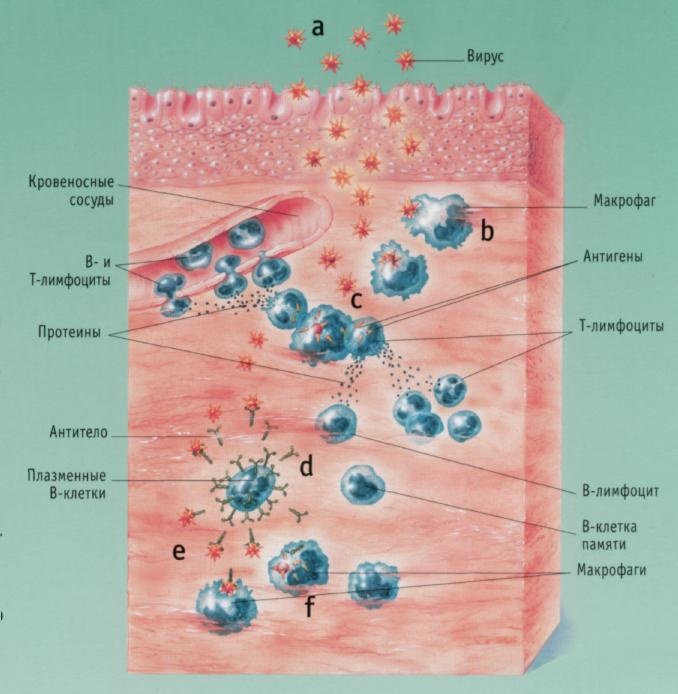
рис. 2. Гуморальный иммунный ответ.
В-лимфоциты вырабатывают антитела, помогая распознавать и удалять чужеродные антигены (переносимые бактериями или вирусами). Им помогают циркулирующие в крови Т-лимфоциты и макрофаги.

а) Вирусные частицы через поверхностные клетки проникают в ткань и размножаются.
б) Макрофаги пожирают вирусные частицы,
в) Макрофаги передают антигены циркулирующим в крови Т-лимфоцитам. Это приводит к мобилизации дополнительного количества Т- и В-лимфоцитов.
г) В-лимфоциты распадаются на плазматические В-клетки, которые производят антитела, специфичные для проникшего вируса, и В-клетки памяти.
д) Циркулирующие в крови антитела взаимодействуют с вирусными частицами.
е) Макрофаги распознают и пожирают вирусы, защищая организм от инфекций. 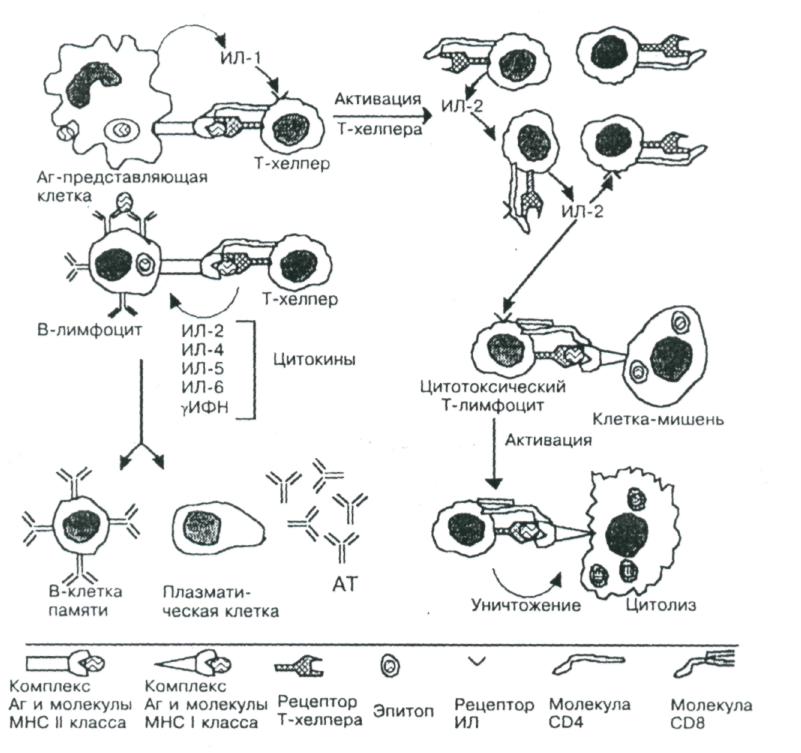
рис.3. Взаимодействие клеток при иммунном ответе.
Рецептор Т-хелпера распознаёт антигенную детерминанту (эпитоп) вместе с молекулой ГКГ 11 класса, выставленные на поверхности Аг-представляющей клетки. В молекулярном взаимодействии участвует дифференцировочный Аг Т-хелпера СD4. В результате подобного взаимодействия Аг- представляющая клетка секретирует ИЛ-1, стимулирующий в Т-хелпере синтез и секрецию ИЛ-2, а также синтез и встраивание в плазматическую мембрану того же Т-хелпера рецепторов ИЛ-2. ИЛ-2 стимулирует пролиферацию Т-хелперов и активирует цитотоксические Т-лимфоциты. Отбор В-лимфоцитов произво-дится при взаимодействии Аг с Fаb -фрагментами Ig М на поверхности этих клеток. Эпитоп этого Аг в комплексе с молекулой ГКГ II класса узнаёт рецептор Т-хелпера, после чего из Т-лимфоцита секретируются цитокины, стимулирующие пролиферацию В-лимфоцитов и их дифференцировку в плазматические клетки, синтезирующие АТ против данного Аг. Рецептор цитотоксических Т-лимфоцитов связывается с антигенной детерминантой в комплексе с молекулой ГКГ I класса на поверхности вирус- инфицированной или опухолевой клетки. В молекулярном взаимодействии участвует диффе-ренцировочный Аг цитотоксического Т-лимфоцита СD 8. После связывания молекул взаимодействующих клеток цитотоксический Т-лимфоцит убивает клетку-мишень.
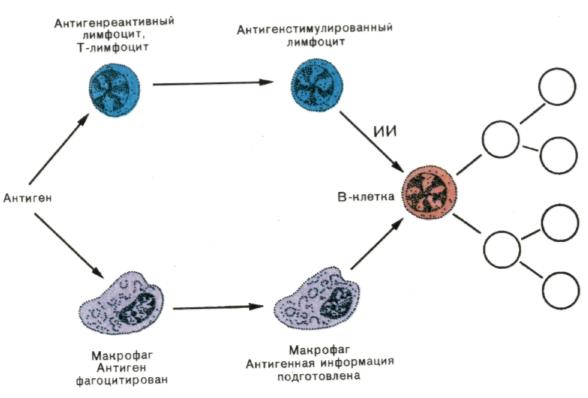
Рис. 5. Трехклеточная система взаимодействия при развитии гуморального иммунного ответа.
В-лимфоцит получает специфическую информацию об антигене от поглотившего чужеродный материал макрофага и неспецифическую — от индуктора иммунопоэза (ИИ), секретируемого Т-лимфоцитом после распознавания антигена. В условиях, когда кооперируют все три типа клеток, развивается полноценный иммунный ответ. Если В-клетка получает только информацию об антигене от макрофага, а помощь со стороны Т-клетки отсутствует, то индуцируется специфическая неотвечаемость — толеран-тность. При действии на В-клетку только ИИ происходит синтез неспецифических иммуноглобулинов.
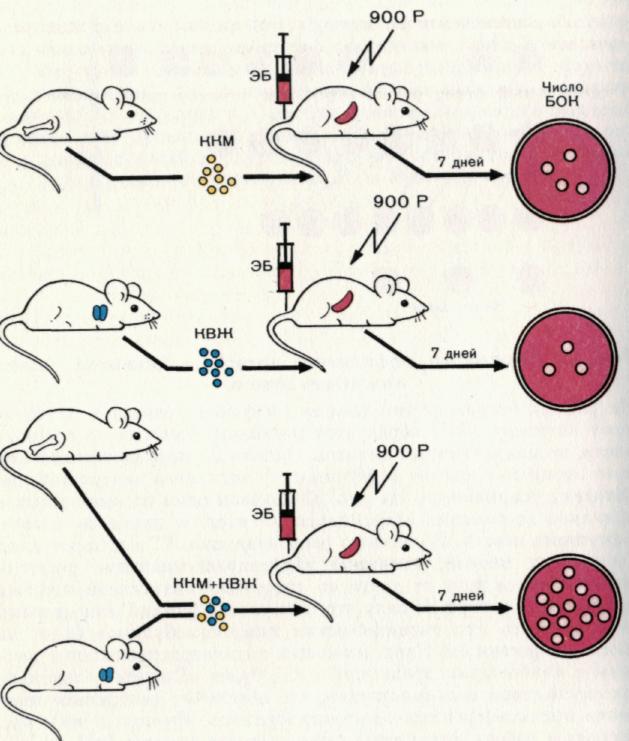
Рис. 6. Взаимодействие между клетками вилочковой железы (источника Т-клеток) и клетками костного мозга (источника В-клеток) при индукции гуморального иммунного ответа.
Гуморальный ответ развивается как комплексный процесс, который включает несколько типов клеток. Введение облученным мышам только клеток костного мозга — ККМ (В-лимфоцитов) или только клеток вилочковой железы — КВЖ (Т-клеток) не обеспечивает развитие иммунного ответа достаточной силы. В то же время введение смеси этих клеток приводит к формированию интенсивной продукции антител к эритроцитам барана. Причем ответ при таком совместном введении клеток значительно выше, чем сумма ответов при раздельном введении клеток различного происхождения. Иначе кооперация различных типов клеток приводит к синергическому эффекту. Ответ оценивали по количеству бляшкообразующих клеток (БОК) в селезенке.
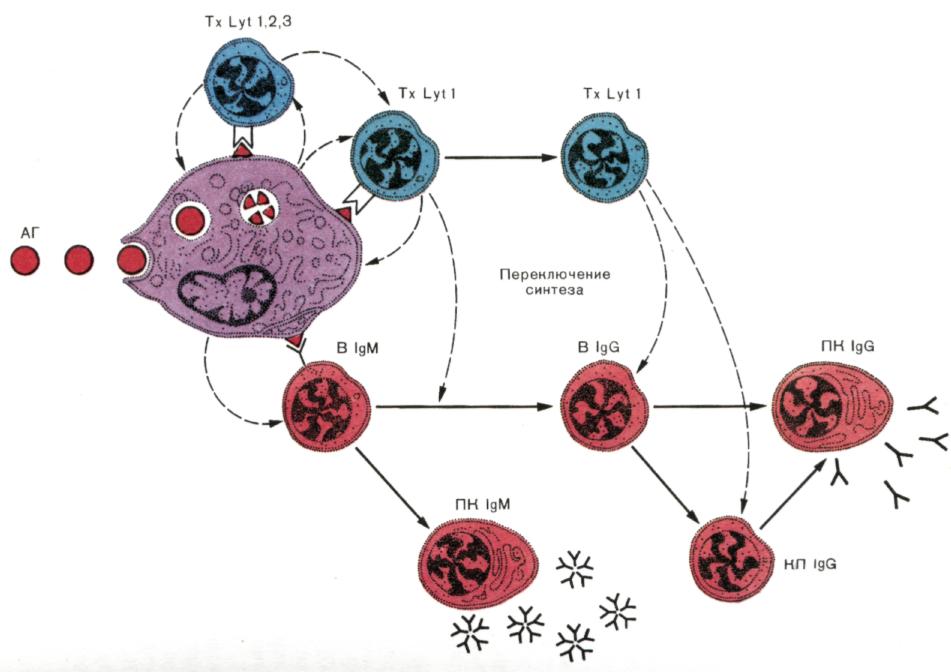
Рис. 7. Развитие гуморального иммунного ответа.
«Суммарная» схема, учитывающая субпопуляции лимфоцитов, которые участвуют в индукции антителогенеза, переключение синтеза IgМ на синтез IgG и создание клеток памяти. Захваченный макрофагами (МФ) антиген (АГ) выводится на клеточную поверхность в иммуногенной форме. В реакцию распознавания АГ вступают «ранние» Т-хелперы с фенотипом, которые способствуют созреванию «поздних» Т-хелперов, помогающих антителопродукции. Развитие первичного IgМ-ответа не требует помощи со стороны Тх Lуt1. Для накопления плазматических клеток, продуцирующих IgМ-антитела (ПК IgМ), очевидно, достаточно простого распознавания АГ на поверхности МФ. Однако помощь Тх Lуt1необходима для внутриклеточного переключения синтеза IgМ на синтез IgG, накопления плазматических клеток, синтезирующих и секретирующих IgG (ПК IgG) и вступления клеток памяти (КП IgG) во вторичный иммунный ответ.
Клеточный иммунный ответ характеризуется пролиферацией коммитированных иммунокомпетентных клеток, реагирующих с Аг в комплексе с молекулой ГКГ I класса на поверхности чужеродных клеток или эндогенными иммуногенами в комплексе с молекулой ГКГ I класса на поверхности собственных вирус- инфицированных и опухолевых клеток. В клеточном иммунном ответе участвует цитотоксический Т-лимфоцит. Цитотоксический Т-лимфоцит (Тс). Предъявленный на поверхности клетки-мишени Аг в комплексе с молекулой ГКГ I класса связывается с рецептором цитотоксического Т-лимфоцита. В этом процессе участвует молекула СD8 клеточной мембраны Тс. Секретируемый Т-хелперами ИЛ-2 стимулирует пролиферацию цитотоксических Т-лимфоцитов. Уничтожение клетки-мишени. Цитотоксический Т-лимфоцит распознаёт клетку-мишень и прикрепляется к ней. В цитоплазме активированного цитотоксического Т-лимфоцита присутствуют мелкие тёмные органеллы, напоминающие запасающие гранулы секреторных клеток. Гранулы концентрируются в той части Т-киллера, которая расположена ближе к месту контакта с клеткой-мишенью. Параллельно происходят переориентация цитоскелета и смещение в эту область комплекса Гольджи, в котором и формируются гранулы. В них содержится цитолитический белок перфорин.
Выделяемые Т-киллером молекулы перфорина полимеризуются в мембране клетки-мишени в присутствии Са2+. Сформированные в плазматической мембране клетки-мишени перфориновые поры пропускают воду и соли, но не молекулы белка. Если полимеризация перфорина произойдет во внеклеточном пространстве или в крови, где в избытке имеется кальций, то полимер не сможет проникнуть в мембрану и убить клетку. Специфическое действие Т-киллера проявляется только как результат тесного контакта между ним и клеткой-мишенью, который достигается за счёт взаимодействия Аг на поверхности жертвы с рецепторами Т-киллера. Сам Т-киллер защищен от цитотокси-ческого действия перфорина. Механизм самозащиты неизвестен. Альтернативный механизм уничтожения клетки-мишени, согласно которому цитотоксические Т-лимфоциты и NK-клетки являются источником сигнала, который запускает уже предсуществующую суицидальную программу в клетке-мишени. Действие этого сигнала усиливают глюкокортикоиды.
| | | следующая лекция ==> | |
| | |
Источник
