На введение в организм вакцин возникает иммунитет
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 мая 2020;
проверки требуют 8 правок.
Иммуните́т (лат. immunitas — освобождение) человека и животных — способность организма поддерживать свою целостность и биологическую индивидуальность путём распознавания и удаления чужеродных веществ и клеток[1] (в том числе болезнетворных бактерий и вирусов). Характеризуется изменением функциональной активности преимущественно иммуноцитов с целью поддержания гомеостаза внутренней среды.
Назначение[править | править код]
Простейшие защитные механизмы, имеющие своей целью распознавание и обезвреживание патогенов, существуют даже у прокариот: например, ряд бактерий обладает ферментными системами, которые препятствуют заражению бактерии вирусом[2]. Одноклеточные эукариотные организмы применяют токсичные пептиды, чтобы предотвратить проникновение бактерий и вирусов в свои клетки[3].
По мере эволюции сложно организованных многоклеточных организмов у них формируется многоуровневая иммунная система, важнейшим звеном которой становятся специализированные клетки, противостоящие вторжению генетически чужеродных объектов[4].
У таких организмов иммунный ответ происходит при столкновении данного организма с самым различным чужеродным в антигенном отношении материалом, включая вирусы, бактерии и другие микроорганизмы, обладающие иммуногенными свойствами молекулы (прежде всего белки, а также полисахариды и даже некоторые простые вещества, если последние образуют комплексы с белками-носителями — гаптены[5]), трансплантаты или мутационно изменённые собственные клетки организма. Как отмечает В. Г. Галактионов, «иммунитет есть способ защиты организма от всех антигенно чужеродных веществ как экзогенной, так и эндогенной природы; биологический смысл подобной защиты — обеспечение генетической целостности особей вида в течение их индивидуальной жизни»[6]. Биологическим смыслом такой защиты является обеспечение генетической целостности особей вида на протяжении их индивидуальной жизни, так что иммунитет выступает как фактор стабильности онтогенеза[7].
Характерные признаки иммунной системы[8]:
- способность отличать «своё» от «чужого»;
- формирование памяти после первичного контакта с чужеродным антигенным материалом;
- клональная организация иммунокомпетентных клеток, при которой отдельный клеточный клон способен, как правило, реагировать лишь на одну из множества антигенных детерминант.
Классификации[править | править код]
Иммунная система исторически описывается состоящей из двух частей — системы гуморального иммунитета и системы клеточного иммунитета. В случае гуморального иммунитета защитные функции выполняют молекулы, находящиеся в плазме крови, а не клеточные элементы. В то время как в случае клеточного иммунитета защитная функция связана именно с клетками иммунной системы.
Иммунитет также классифицируют на врождённый и адаптивный.
Врождённый (неспецифический, наследственный[9]) иммунитет обусловлен способностью идентифицировать и обезвреживать разнообразные патогены по наиболее консервативным, общим для них признакам, дальности эволюционного родства, до первой встречи с ними. В 2011 году была вручена Нобелевская премия в области медицины и физиологии за изучение новых механизмов работы врождённого иммунитета (Ральф Стайнман, Жюль Хоффман и Брюс Бётлер)[10].
Осуществляется большей частью клетками миелоидного ряда, не имеет строгой специфичности к антигенам, не имеет клонального ответа, не обладает памятью о первичном контакте с чужеродным агентом.
Адаптивный (устар. приобретённый, специфический) иммунитет имеет способность распознавать и реагировать на индивидуальные антигены, характеризуется клональным ответом, в реакцию вовлекаются лимфоидные клетки, имеется иммунологическая память, возможна аутоагрессия.
Классифицируют на активный и пассивный.
- Приобретённый активный иммунитет возникает после перенесённого заболевания или после введения вакцины.
- Приобретённый пассивный иммунитет развивается при введении в организм готовых антител в виде сыворотки или передаче их новорождённому с молозивом матери или внутриутробным способом.
Другая классификация разделяет иммунитет на естественный и искусственный.
- Естественный иммунитет включает врождённый иммунитет и приобретённый активный (после перенесённого заболевания), а также пассивный иммунитет при передаче антител ребёнку от матери.
- Искусственный иммунитет включает приобретённый активный после прививки (введение вакцины) и приобретённый пассивный (введение сыворотки).
Органы иммунной системы[править | править код]
Выделяют центральные и периферические органы иммунной системы. К центральным органам относят красный костный мозг и тимус, а к периферическим — селезёнку, лимфатические узлы, а также местноассоциированную лимфоидную ткань: бронхассоциированную (БАЛТ), кожноассоциированную (КАЛТ), кишечноассоциированную (КиЛТ, пейеровы бляшки).
Красный костный мозг — центральный орган кроветворения и иммуногенеза. Содержит самоподдерживающуюся популяцию стволовых клеток. Красный костный мозг находится в ячейках губчатого вещества плоских костей и в эпифизах трубчатых костей. Здесь происходит дифференцировка В-лимфоцитов из предшественников. Содержит также Т-лимфоциты.
Тимус — центральный орган иммунной системы. В нём происходит дифференцировка Т-лимфоцитов из предшественников, поступающих из красного костного мозга.
Лимфатические узлы — периферические органы иммунной системы. Они располагаются по ходу лимфатических сосудов. В каждом узле выделяют корковое и мозговое вещество. В корковом веществе есть В-зависимые зоны и Т-зависимые зоны. В мозговом есть только Т-зависимые зоны.
Селезёнка — паренхиматозный зональный орган. Является самым крупным органом иммунной системы, кроме того, выполняет депонирующую функцию по отношению к крови. Селезёнка покрыта капсулой из плотной соединительной ткани, которая содержит гладкомышечные клетки, позволяющие ей при необходимости сокращаться. Паренхима представлена двумя функционально различными зонами: белой и красной пульпой. Белая пульпа составляет 20 %, представлена лимфоидной тканью. Здесь имеются В-зависимые и Т-зависимые зоны. И также здесь есть макрофаги. Красная пульпа составляет 80 %. Она выполняет следующие функции:
- Депонирование зрелых форменных элементов крови.
- Контроль состояния и разрушения старых и повреждённых эритроцитов и тромбоцитов.
- Фагоцитоз инородных частиц.
- Обеспечение дозревания лимфоидных клеток и превращение моноцитов в макрофаги.
Иммунокомпетентные клетки[править | править код]
К иммунокомпетентным клеткам относят макрофаги и лимфоциты. Эти клетки совместно участвуют в инициации и развитии всех звеньев адаптивного иммунного ответа (система трёхклеточной кооперации).
Клетки, участвующие в иммунном ответе[править | править код]
T-Лимфоциты[править | править код]
Субпопуляция лимфоцитов, отвечающая главным образом за клеточный иммунный ответ. Включает в себя субпопуляции Т-хелперов (дополнительно разделяются на Th1, Th2, а также выделяют Treg, Th9, Th17, Th22,), цитотоксических Т-лимфоцитов,NKT. Включает в себя эффектор, регуляторы и долгоживущие клетки-памяти. Функции разнообразны: как регуляторы и администраторы иммунного ответа (Т-хелперы), так и киллеры (цитотоксические Т-лимфоциты).
B-Лимфоциты[править | править код]
Субпопуляция лимфоцитов, синтезирующая антитела и отвечающая за гуморальный иммунный ответ.
Натуральные киллеры[править | править код]
Натуральные киллеры (NK-клетки) — субпопуляция лимфоцитов, обладающая цитотоксичной активностью, то есть они способны: контактировать с клетками-мишенями, секретировать токсичные для них белки, убивать их или отправлять в апоптоз. Натуральные киллеры распознают клетки, поражённые вирусами и опухолевые клетки.
Нейтрофилы[править | править код]
Нейтрофилы — это неделящиеся и короткоживущие клетки. Они составляют 65-70 % от гранулоцитов. Нейтрофилы содержат огромное количество антибиотических белков, которые содержатся в различных гранулах. К этим белкам относятся лизоцим (мурамидаза), липопероксидаза и другие антибиотические белки. Нейтрофилы способны самостоятельно мигрировать к месту нахождения антигена, так как у них есть рецепторы хемотаксиса (двигательная реакция на химическое вещество). Нейтрофилы способны «прилипать» к эндотелию сосудов и далее мигрировать через стенку к месту нахождения антигенов. Далее проходит фагический цикл, и нейтрофилы постепенно заполняются продуктами обмена. Далее они погибают и превращаются в клетки гноя.
Эозинофилы[править | править код]
Эозинофилы составляют 2—5 % от гранулоцитов. Способны фагоцитировать микробы и уничтожать их. Но это не является их главной функцией. Главным объектом эозинофилов являются гельминты. Эозинофилы узнают гельминтов и экзоцитируют в зону контакта вещества — перфорины. Эти белки встраиваются в билипидный слой клеток гельминта. В них образуются поры, внутрь клеток устремляется вода, и гельминт погибает от осмотического шока.
Базофилы[править | править код]
Базофилы составляют 0,5-1 % от гранулоцитов. Существуют две формы базофилов: собственно базофилы, циркулирующие в крови, и тучные клетки, находящиеся в ткани. Тучные клетки располагаются в различных тканях, лёгких, слизистых и вдоль сосудов. Они способны вырабатывать вещества, стимулирующие анафилаксию (расширение сосудов, сокращение гладких мышц, сужение бронхов). При этом происходит взаимодействие с иммуноглобулином Е (IgE). Таким образом они участвуют в аллергических реакциях. В частности, в реакциях немедленного типа.
Моноциты[править | править код]
Моноциты превращаются в макрофаги при переходе из кровеносной системы в ткани, существуют несколько видов макрофагов в зависимости от типа ткани, в которой они находятся, в том числе:
- Некоторые антигенпредставляющие клетки, в первую очередь дендритные клетки, роль которых — поглощение микробов и «представление» их Т-лимфоцитам.
- Клетки Купфера — специализированные макрофаги печени, являющиеся частью ретикулоэндотелиальной системы.
- Альвеолярные макрофаги — специализированные макрофаги лёгких.
- Остеокласты — костные макрофаги, гигантские многоядерные клетки позвоночных животных, удаляющие костную ткань посредством растворения минеральной составляющей и разрушения коллагена.
- Микроглия — специализированный класс глиальных клеток центральной нервной системы, которые являются фагоцитами, уничтожающими инфекционные агенты и разрушающими нервные клетки.
- Кишечные макрофаги и т. д.
Функции их разнообразны и включают в себя фагоцитоз, взаимодействие с адаптивной иммунной системой и инициацию и поддержание иммунного ответа, поддержание и регулирование процесса воспаления, взаимодействие с нейтрофилами и привлечение их в очаг воспаления, выделение цитокинов, регуляция репарации, регуляция процессов свертывания крови и проницаемости капилляров в очаге воспаления, синтез компонентов системы комплемента.
Макрофаги, нейтрофилы, эозинофилы, базофилы и натуральные киллеры обеспечивают прохождение врождённого иммунного ответа, который является неспецифичным (в патологии неспецифичный ответ на альтерацию называют воспалением, воспаление является неспецифической фазой последующих специфических иммунных).
Иммунно привилегированные области[править | править код]
В некоторых частях организма млекопитающих и человека появление чужеродных антигенов не вызывает иммунного ответа. К таким областям относятся мозг и глаза, семенники, эмбрион и плацента. Нарушение иммунных привилегий может становиться причиной аутоиммунных заболеваний.
Иммунные заболевания[править | править код]
Аутоиммунные заболевания[править | править код]
При нарушении иммунной толерантности или повреждении тканевых барьеров возможно развитие иммунных реакций на собственные клетки организма. Например, патологическая выработка антител к ацетилхолиновым рецепторам собственных мышечных клеток вызывает развитие миастении[11].
Иммунодефицит[править | править код]
См. также[править | править код]
- Иммунная система
- Врождённый иммунитет
- Приобретенный иммунитет
- Иммунотерапия рака
- Иммунитет растений
- Химера (биология)
Примечания[править | править код]
- ↑ ИММУНИТЕТ • Большая российская энциклопедия — электронная версия. bigenc.ru. Дата обращения 8 апреля 2020.
- ↑ Bickle T. A., Krüger D. H. Biology of DNA restriction // Microbiological Reviews. — 1993. — Vol. 57, no. 7. — P. 434—450. — PMID 8336674.
- ↑ Черешнев В.А. Черешнева М.В. Иммунологические механизмы локального воспаления. Медицинская иммунология 2011 т.13 №6 стр.557-568 РО РААКИ. cyberleninka.ru. Дата обращения 16 мая 2020.
- ↑ Travis J. On the Origin of the Immune System // Science. — 2009. — Vol. 324, no. 5927. — P. 580—582. — doi:10.1126/science.324_580. — PMID 19407173.
- ↑ Genetics of the Immune Response / Ed. by E. Möller and G. Möller. — New York: Plenum Press, 2013. — viii + 316 p. — (Nobel Foundation Symposia, vol. 55). — ISBN 978-1-4684-4469-8. — P. 262.
- ↑ Галактионов В.Г. Проблемы эволюционной иммунологии. cyberleninka.ru. Медицинская иммунология 2004 т.6 №3-5 РО РААКИ. Дата обращения 16 мая 2020.
- ↑ Галактионов, 2005, с. 8.
- ↑ Галактионов, 2005, с. 8, 12.
- ↑ Иммунитет // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2.
- ↑ Нобелевская премия по физиологии и медицине 2011 (англ.). www.nobelprize.org.
- ↑ Галактионов, 2005, с. 392.
Литература[править | править код]
- Галактионов В. Г. . Эволюционная иммунология. — М.: Академкнига, 2005. — 408 с. — ISBN 5-94628-103-8.
- Хаитов Р. М. . Иммунология. — М.: ГЕОТАР, 2006. — 320 с. — ISBN 978-5-9704-1288-6.
- Ярилин А. А. . Иммунология. — М.: ГЕОТАР, 2010. — 737 с. — ISBN 978-5-9704-1319-7.
Источник
Профилактика инфекций посредством вакцинации доказала свою эффективность, является на протяжении двух столетий неотъемлемой частью при формировании защитного иммунитета у населения. Иммунология начала зарождаться в 18 веке, когда Э. Дженнер установил, что доярки, взаимодействующие с зараженными оспой коровами, не болеют впоследствии черной оспой, поражавшей людей того времени. Не зная ничего об иммунитете, его механизмах, доктор создал вакцину, позволившую снизить уровень заболеваемости.
Последователем Дженнера считают Луи Пастера, который определил наличие микроорганизмов, являющихся возбудителями инфекций, получил вакцину против бешенства. Постепенно ученные создали препараты от коклюша, кори, полиомиелита и других, ранее опасных для жизни, здоровья человечества болезней. В 21 веке иммунопрофилактика остается главным инструментом создания специфического иммунитета среди граждан.
Что такое вакцина
Иммунный препарат в состав, которого входят ослабленные, либо убитые вирусные компоненты возбудителей получил название вакцина. Она служит для выработки в организме человека антител, противостоящих антигенам (чужеродным структурам) на протяжении длительного временного периода, отвечающих за устойчивый иммунный барьер.
Разработаны средства (сыворотки) действующие не более нескольких месяцев, отвечающие за выработку пассивного иммунитета. Они вводятся сразу же после инфицирования, позволяют спасти человека от смерти, серьезных патологий. Вакцинация – механизм, обеспечивающий организм специфическими антителами, которые он получает не болея.
Вакцина до прохождения сертификации проходит длительный экспериментальный путь. К использованию допускают препараты со следующими характеристиками:
- Безопасность — после введения вакцины отсутствуют тяжелые осложнения у граждан.
- Протективность – длительное стимулирование защитного потенциала против введенного возбудителя, сохранение иммунологической памяти.
- Иммуногенность – способность к индукции активного иммунитета с долгосрочным эффектом вне зависимости от специфичности антигена.
- Иммунная активность – направленная стимуляция выработки нейтрализующих антител, эффекторных Т-лимфоцитов.
- Вакцина должна быть: биологически стабильной, неизменчивой при транспортировке, хранении, обладать низкой реактогенностью, доступной стоимостью, удобной при применении.
Перечисленные свойства вакцин позволяют свести к минимуму проявление местных реакций и осложнений. В чем заключается разница между понятиями:
- поствакцинальные реакции или местные – кратковременный ответ организма, возникающий на введение вакцины. Он проявляется в виде припухлости, отечности или покраснения в месте инъекции, общих недомоганий – подъема температуры, головной боли. Продолжительность периода составляет в среднем 3 суток, коррекция состояний носит симптоматический характер;
- осложнения после вакцины – возникают отсрочено, принимают патологические формы. К ним относят: аллергические реакции, процессы нагноения, спровоцированные нарушением правил асептики, обострение хронических болезней, наслоение инфекций, полученных в поствакцинальный период.
Разновидности вакцин
Иммунологи разделяю вакцины на типы, отличающиеся способом получения, механизмом действия, компонентным составом и рядом других признаков. Выделяют:

Аттенуированные – препараты производят из живых, но сильно ослабленных вирусов, либо патогенных штаммов микроорганизмов измененных генетически, либо из родственных штаммов (дивергентные суспензии), которые не в состоянии вызвать заражение человека. Корпускулярные вакцины характеризуются сниженной вирулентностью (уменьшенной способностью антигена заражать) при сохранении иммуногенных свойств, то есть способности вызывать иммунный ответ и формировать устойчивый иммунитет.
Примерами живых вакцин служат средства, используемые при иммунизации против чумы, гриппа, кори, краснухи, эпидемического паротита, бруцеллеза, туляремии, натуральной оспы, сибирской язвы. После некоторых прививок, например БЦЖ, требуется ревакцинация для сохранения иммунитета на протяжении жизненного периода.
Инактивированные – состоят из «мертвых» микробных частиц, выращиваемых в других культурах, например, на куриных эмбрионах, затем, убитых под воздействием формальдегида и очищенных от белковых примесей. К обозначенной категории вакцин относятся:
- корпускулярные – добывают из целостных штаммов (цельновирионные), либо из бактерий вируса (цельноклеточные). Примером первых являются противогриппозные суспензии, от клещевого энцефалита, вторых – лиофилизированные массы против лептоспироза, коклюша, брюшного тифа, холеры. Вакцины не вызывают инфицирование организма, но тем не менее содержат протективные антигены, могут спровоцировать аллергии и сенсибилизацию. Преимуществом корпускулярных составов в их стабильности, безопасности, высокой реактогенности;
- химические – изготавливают из бактериальных единиц, имеющих определенную химическую структуру. Отличительной особенностью считают минимальное наличие балластных частиц. К ним причисляют вакцины от дизентерии, пневмококка, брюшного тифа;
- конъюгированные – содержат комплекс из токсинов и бактериальных полисахаридов. Подобные комбинации усиливают индуцирование иммуногеном иммунитета. Например, сочетание вакцины анатоксина дифтерийного и Ar Haemophilus influenzae;
- сплит или субвирионные расщепленные – состоят из внутренних и поверхностных антигенов. Вакцины хорошо очищены, поэтому переносятся без выраженных побочных проявлений. Примером служат некоторые средства против гриппа;
- субъединичные – образованы из молекул инфекционных частиц, то есть имеют изолированные антигены микробов. Например, Гриппол, Инфлювак. Отдельно обозначают анатоксин – состав, выработанный из обезвреженных токсинов бактерий, который сохранил анти- и иммуногенность. Анатоксины способствуют формированию напряженного иммунитета длительностью до 5 лет и больше;
- рекомбинантные генно-инженерные – получают при содействии рекомбинантных ДНК, переносимых из вредоносного микроорганизма. Например, вакцина от ВГВ.
Сравнительный анализ вакцин
Таблица №1
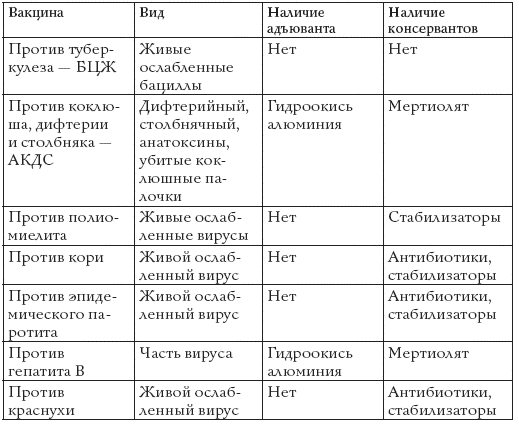
Особенности поствакцинального иммунитета
После тех или иных прививок, у человека вырабатывается иммунитет специфичный по отношению к введенным инфекционным возбудителям, формируется невосприимчивость к ним. Основными характеристиками иммунитета, возникшего от вакцины, считаются:
- выработка антител к специфичным антигенам инфекционного заболевания;
- формирование иммунитета через 2 – 3 недели;
- поддержание способности клеток длительно сохранять информацию, отвечать реакцией при выявлении гомогенного антигена;
- пониженная невосприимчивость к инфицированию при сравнении с иммунитетом, образованным после перенесенного заболевания.
Иммунитет, приобретенный человеком посредством прививок, не наследуется, при грудном кормлении не передается. В своем становлении он проходит 3 этапа:
- Скрытый. На протяжении первых 3 дней формирование протекает латентно, без видимых изменений в иммунном статусе.
- Период роста. Длится в зависимости от препарата, особенностей организма от 3 до 30 дней. Характеризуется увеличением количества антител по отношению к возбудителю, полученному при инъекции.
- Снижения иммунитета. Постепенное уменьшение ответа от прививок штаммов.
Получить полноценный ответ на Т-зависимые антигены, возможно при соблюдении ряда условий: применять следует протективные, правильно дозированные вакцины, обеспечивающие продолжительный контакт с иммунной системой. Длительность взаимодействия обеспечивают путем создания «депо», введением суспензии по схеме с соблюдением указанных интервалов, своевременной ревакцинацией. Устойчивость организма к инфекциям обеспечивается отсутствием стрессов, ведением подвижного образа жизни, сбалансированные питанием.
Вакцинацию откладывают при высоких показателях температуры, хронических заболеваниях в обостренной фазе, воспалительных процессах, иммуннодефиците, гемобластозе. Следует оценить риски вакцинации при планировании и в период беременности, аллергических состояниях при введении предыдущих вакцин.
Глобализация применения вакцин
Каждый гражданин должен понимать, что предотвратить распространение инфекции можно лишь профилактическими мероприятиями, которые отражены в календаре прививок отдельно взятого государства. В документе указана информация о перечне вакцин, эпидемиологически оправданных для конкретной территории, сроках их постановки.
ВОЗ создала расширенную программу иммунизации (РПИ) в 1974 году, направленную на предупреждение возникновения инфекций, сокращение их распространения.
Благодаря РПИ выделяют несколько значимых этапов, позволивших сократить возникновение очагов ряда заболеваний:
- 1974 – 1990 гг. – активная иммунизация против кори, столбняка, полиомиелита, туберкулеза, коклюша;
- 1990 – 2000 гг. – ликвидация краснухи беременных, полиомиелита, столбняка новорожденных. Снижение инфицирования корью, свинкой, коклюшем, параллельная разработка, применение суспензий, сывороток против японского энцефалита, желтой лихорадки;
- 2000 – 2025 гг. – реализуется введение ассоциированных препаратов, планируется ликвидация дифтерии, краснухи, кори, гемофильной инфекции, паротита.
Масштабный охват вызывает некоторые опасения со стороны населения, среди молодых родителей, опасающихся мельчайших признаков нездоровья ребенка. Следует помнить, что средства, формирующие иммунитет, защитят от специфичных заболеваний, предотвратят осложнения, патологические изменения, смерть при инфицировании в ситуациях отказа от прививки. Даже здоровый образ жизни не способен обезопасить организм от воздействия вирусов, бактерий.
В случаях заражения после прививки, например при ненадлежащем хранении средства, нарушениях введения препарата, болезнь протекает легко и без последствий, благодаря наличию иммунитета. Плановая вакцинация экономически оправдана, так как лечение в случае инфицирования потребует больше средств, чем стоимость вакцины.
Видео: сроки формирования БЦЖ
Источник
