Особенности иммунитета при сифилисе

Врожденного иммунитета к сифилису у человека не бывает. У переболевших сифилисом также нет стойкого иммунитета и возможно повторное заражение (реинфекция). В организме больного сифилисом развивается нестерильный инфекционный иммунитет, возникающий через 10—14 дней после появления твердого шанкра. И пока бледная трепонема находится в организме больного, он практически не восприимчив к новому заражению.
Иммунитет существует до тех пор, пока в организме имеется возбудитель, и исчезает, как только наступает выздоровление. В литературе описаны случаи многократного заражения сифилисом. Вместе с тем следует иметь в виду, что при поздних формах сифилиса иммунитет иногда выражен настолько слабо, что, несмотря на гуммозные проявления или симптомы спинной сухотки, прогрессивного паралича и др., у больного на месте повторного внедрения трепонем развивается твердый шанкр и иные симптомы ранних форм сифилиса. Так, Н. А. Черногубов и В. А. Рахманов (1931) описали проявления активного сифилиса на коже при прогрессивном параличе и спинной сухотке; Г. И. Мещерский и С. И. Богданов (1933) сообщили о редких случаях повторного заражения при третичном, врожденном и позднем скрытом сифилисе; И. Т. Акопян (1950) сообщил о больных (вторичный свежий и вторичный рецидивный сифилис), у которых имелась реинфекция на фоне симптомов нелеченой спинной сухотки.
Нестерильный иммунитет сопровождается аллергической реакцией. С исчезновением инфекционного иммунитета пропадает инфекционная аллергия. Следовательно, при сифилисе реактивность организма меняется в двух направлениях: повышенная (аллергия) и пониженная (иммунитет).
Важнейшим фактором иммунитета является фагоцитоз, при котором макрофаги, гистиоциты захватывают трепонему, окруженную лимфоцитом, а часть ее переходит в лимфоцит, который становится сенсибилизированным к данным антигенам. В ответ на нахождение в организме трепонемы образуются антитела-иммуноглобулины: IgM (реагины), IgG (иммобилизины), IgA (флюоресцеины). В разные периоды сифилиса появляются различные антитела: сначала флюоресцирующие (до появления шанкра), затем антитела на протеиновые антигены (реагины и преципетины) и в последнюю очередь иммобилизины. В начале заболевания обнаруживаются более крупные антитела (IgM, IgA), при поздних формах приобретенного и врожденного сифилиса образуются антитела практически только класса IgG. Антитела улучшают фагоцитоз, выполняя транспортную функцию и подводя антигены к макрофагам, а также усиливают их ферментактивную деятельность. В реализации иммунологического ответа организма на внедрение бледной трепонемы участвуют макрофаги, Т-и В-лимфоциты.
Процесс поглощения трепонемы мононуклеарными фагоцитами подразделяется на четыре стадии:
1. сближение фагоцита и трепонемы,
2. прилипание (аттракция),
3. погружение трепонемы в протоплазму,
4. переваривание.
Процесс фагоцитоза может быть завершенным и незавершенным. При завершенном процессе микроорганизм лизируется; при незавершенном, находясь в клетке, он может размножаться либо не размножаться, сохраняя при этом свою структуру и возможность для размножения, и, наконец, изменяясь морфологически, при благоприятных условиях может переходить в обычные бактериальные формы. Однако основной его формой при сифилисе является незавершенныйфагоцитоз. Особенности фагоцитоза при сифилисе следующие:
· участие в процессе всех клеточных форм,
· незавершенность фагоцитарной реакции,
· сохранение бледных трепонем в плазматических клетках,
· фагоцитоз трепонем клетками эндотелия капилляров и швановскими клетками.
Массовое размножение трепонем и их распространение в организме происходят в конце первичного и в начале вторичного периода сифилиса, т. е. развивается спирохетный сепсис, сопровождаемый иногда температурной реакцией, слабостью, недомоганием, болью в костях и суставах. Это приводит к развитию иммунобиологических реакций, способствующих частичной гибели трепонем, — наступает скрытый период вторичного сифилиса. В дальнейшем взаимоотношения между микро- и макроорганизмом обусловливают волнообразное течение инфекции во вторичном периоде сифилиса.
В третичном периоде, когда в тканях с трудом обнаруживаются трепонемы, организм больного, будучи ослабленным различными факторами и высокосенсибилизированным к трепонемам, даже на небольшое количество их реагирует своеобразной анафилактической реакцией (образуются гумма, бугорок).
За рубежом изучались аллергические реакции при сифилисе путем постановки внутрикожных проб из трепонемных экстрактов и с использованием люетина Ногучи. При ранних формах сифилиса и при третичном сифилисе lues-test почти в 100 % случаев давал положительный результат (Degos, 1944). Однако при спинной сухотке, прогрессивном параличе и других поздних формах нейро- и висцеросифилиса lues-test может оказаться отрицательным. На основании этого было сделано заключение, что в этих поздних стадиях РИБТ приобретает большее диагностическое значение, чем lues-test.
Суперинфекция — это состояние организма, больного сифилисом, когда в неосвободившийся от бледных трепонем организм поступают новые их порции (повторное заражение неизлеченного больного), т. е. происходит как бы наслоение новой сифилитической инфекции на уже имеющийся сифилис. В различные периоды заболевания это проявляется по-разному. Так, в инкубационном периоде, в первые 10—14 дней первичного периода сифилиса, когда выраженный инфекционный иммунитет еще отсутствует, повторное заражение приводит к последовательному развитию нового шанкра. Этот шанкр имеет меньшую величину, чем обычный, и возникает, как правило, после укороченного инкубационного периода (до 10—15 дней). Такие шанкры называются последовательными (ulcera indurata seccentuoria). Считается, что в других стадиях сифилиса при суперинфекции организм отвечает на новое заражение высыпаниями той стадии, в которой он находится во время поступления новой порции трепонем (например, во время вторичного скрытого периода возникают папулы, розеолы и т. д.). При третичном сифилисе прогрессивном параличе и спинной сухотке (правда, не во всех случаях), когда ослабленный организм при незначительном количестве очагов инфекции не способен поддержать на высоком уровне иммунобиологическую реактивность, суперинфекция может выглядеть как новое заражение с образованием твердого шанкра или симптомов вторичного периода сифилиса.
Реинфекция — повторное заражение после полного излечения ранее перенесенного сифилиса. Диагноз реинфекции довольно сложен и ответствен. Во избежание ошибок при его постановке следует придерживаться суммы критериев:
1. достоверность первого заражения (подтвержденного медицинским специальным учреждением);
2. полноценность полученного лечения по поводу первого заражения;
3. негативация серологических реакций и исчезновение сифилидов в обычные сроки;
4. стойкая негативация стандартных серореакций в процессе наблюдения за больным (после окончания лечения по поводу первого заражения должно пройти не менее 1 года);
5. при повторном заражении должен быть новый источник инфекции с активной формой сифилиса, подтвержденного нахождением бледной трепонемы.
Срок от момента полового контакта с больным заразной формой сифилиса до момента диагностики реинфекции должен соответствовать обычным срокам. Новый твердый шанкр имеет иную локализацию и сопровождается регионарным склераденитом. Диагноз реинфекции может быть констатирован на любом этапе течения инфекции.
Источник
Реакции иммунной системы организма при заражении сифилисом

Сифилис — это инфекционное заболевание, вызываемое бледной трепонемой (бактерией Treponema pallidum). Организм человека, заболевшего сифилисом, защищается от возбудителя заболевания с помощью механизмов иммунитета. Проникновение, длительное сохранение в организме (персистенция) и размножение возбудителя заболевания в организме хозяина приводят к выраженным изменениям со стороны иммунной системы.
После попадания бледных трепонем в организм и при их дальнейшем размножении, в организме больного человека происходят иммунные сдвиги. Механизм иммунного ответа при сифилисе исследован не полностью, однако имеются достаточно убедительные данные о том, что в этом процессе участвуют все звенья иммунной системы.
Активируются механизмы как врожденного неспецифического иммунитета, свойственного человеку как биологическуому виду, так и адаптивного, антиген-опосредованного иммунного ответа, вызванного контактом с антигеном. В иммунном ответе организма принимают участие как клеточные (макрофаги, Т-лимфоциты), так и гуморальные механизмы (синтез специфических иммуноглобулинов — антител).
Иммунную реакцию вызывают белки, входящие в состав структур бледной трепонемы; они являются чужеродными веществами для организма человека и относятся к антигенам. Все антигены трепонемы способны стимулировать организм больного вырабатывать антитела соответствующих классов. Вследствие этого, в сыворотке крови больных сифилисом отмечается множественность антител: протеиновых, комплементсвязывающих, полисахаридных реагинов, иммобилизинов, агглютининов.
Классы вырабатываемых антител меняются на разных этапах течения сифилиса — в различных стадиях болезни преобладают то одни, то другие антитела, относящиеся к разным классам иммуноглобулинов. Сила иммунного ответа и спектр антител, выявляемых на разных стадиях развития инфекции, зависит от особенностей организма у данного человека.
У больных вторичным и третичным сифилисом отмечаются признаки микробзависимой супрессии иммунитета.
Сифилис принадлежит к инфекциям, хроническое течение которых вступает в несоответствие с выраженным иммунным ответом на антигены возбудителя. Иными словами, «иммунитет» (т.е. резистентность к инфекции) и «иммунные сдвиги» при сифилисе не совпадают, а иногда и противоречат друг другу.
Во многих случаях иммунологический ответ не предотвращает поэтапного развития инфекции. Организм хозяина неспособен уничтожить сифилитическую инфекцию, что приводит к дальнейшей эволюции патологического процесса. Болезнь, начавшись с местного процесса, распространяется на весь организм и продолжается много лет.
Клеточный и гуморальный иммунный ответ на внедрение бледной трепонемы в организм
В иммунном ответе организма на заражение принимают участие клеточные и гуморальные механизмы иммунитета.
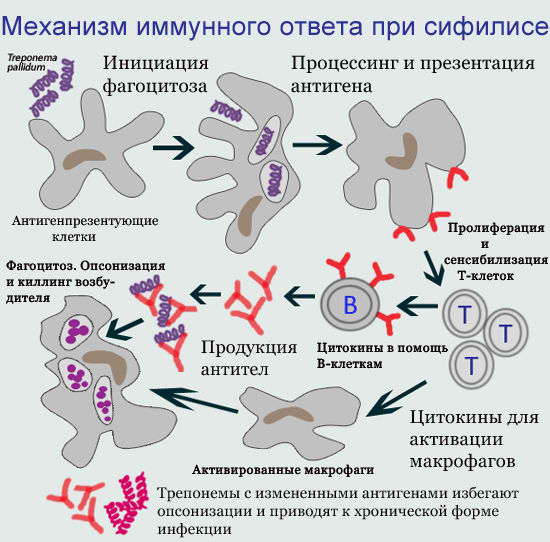
1. Клеточный иммунитет при заражении сифилисом
Клеточный иммунитет является одним из наиболее ранних ответов макроорганизма человека на внедрение бледной трепонемы и, в целом, играет значительную роль в формировании иммунной защиты и санации от сифилитической инфекции.
На клеточном уровне бледной трепонеме противодействуют высокоспециализированные клетки иммунной системы — макрофаги, T-лимфоциты, B-лимфоциты. Происходит изоляция и частичное уничтожение трепонем фагоцитами, в основном макрофагами. Фагоцитоз носит преимущественно незавершенный характер — при поглощении фагоцитом возбудитель не погибает, а остается в клетке, сохраняя свою структуру и способность к размножению. Более того, фагоцит оберегает от антител и воздействия антибиотиков бледную трепонему, которая становится недоступной для защитных сил организма.
Ранний сифилис характеризуется частичным угнетением клеточного иммунитета и развитием состояния иммуносупрессии, постепенно нарастающей активизацией гуморального иммунитета. Клеточное звено страдает в первую очередь, так как Т-лимфоциты более чувствительны к воздействию бактерий T. pallidum.
У больных вторичным, латентным и третичным сифилисом формируется клеточный иммунитет, признаки которого выявляются в реакциях in vivo (кожные пробы) и in vitro (стимуляция Т-лимфоцитов трепонемными антигенами).
2. Гуморальный иммунитет при заражении сифилисе
Гуморальный иммунный ответ заключается в продукции широкого спектра противосифилитических антител. В структуре бледной трепонемы выявлено большое количество соединений, имеющих выраженные антигенные свойства для иммунной системы человека. На начальных этапах развития сифилиса происходит более выраженный синтез антител к антигенам, имеющим высокое содержание в клетке T. pallidum и локализующимся в структуре мембран наружной клеточной стенки или протоплазматического комплекса.
3. Уклонение бледных трепонем от иммунного ответа
Клеточное и гуморальное звенья иммунитета не в состоянии обеспечить полное уничтожение и элиминацию бледных трепонем. Благодаря своему необычному молекулярному строению, T. pallidum обладает замечательной способностью уклоняться от защитной реакции макроорганизма.
В геноме T. pallidum существует нескольких повторяющихся участков, отвечающих за синтез белков, определяющих взаимодействие с иммунной системой организма. «Ускользание» бледной трепонемы от иммунной системы обусловлено вариабельностью этих поверхностных белков, структура которых определяется вариабельностью генов. Этот феномен способствует сохранению бледной трепонемы в организме, в том числе при скрытой инфекции.
Электронно-микроскопические исследования показали, что при сифилисе преобладает незавершенный фагоцитоз трепонем (захват и поглощение трепонем лейкоцитами, макрофагами и другими клетками). При этом трепонемы не погибают, а получают защиту от антибиотиков и антител, и могут даже размножаться в фагоцитирующей клетке. В течение всего инкубационного периода, а также в конце первичного и в начале вторичного периодов сифилиса, возбудители активно размножаются и распространяются по всему организму.
Гуморальный иммунный ответ. Противосифилитические антитела.
Гуморальный иммунный ответ заключается в продукции широкого спектра антител, которые можно разделить на две группы. Противосифилитические антитела могут быть неспецифическими — их называют «реагины» (или антикардиолипиновые антитела) и специфическими (противотрепонемные антитела).
1. Неспецифические антитела при сифилисе
Неспецифические антитела при сифилисе — это антикардиолипиновые антитела, исторически получившие название «реагины». Они направлены против липидных антигенов бледной трепонемы и против аутоантигенов, появляющихся вследствие повреждения и разрушения клеток больного.
Реагиновые антитела у больного сифилисом — это иммуноглобулины класса IgG и IgM. Они являются комплексным ответом на высвобождение липоидных молекулярных фрагментов из поврежденных клеток хозяина, а также на появление липопротеиноподобных структур, сходных с кардиолипином, входящих в состав бактериальной клетки бледной трепонемы.
Липидные антигены cоставляют значительную часть бактериальной клетки T. pallidum. Помимо других антигенов, в клеточной стенке бледной трепонемы содержится фосфолипид кардиолипин; на его долю приходится около 30% сухого вещества клетки спирохеты. В организме человека, больного сифилисом, могут присутствовать липиды, имеющие сходное строение с липоидными структурами клеточной стенки бледной трепонемы. Это аутоантигены, образующиеся в результате разрушения органов и тканей, в основном липиды митохондриальных мембран.
Аутоантигены — это компоненты клеток и тканей собственного организма, которые распознаются при определённых условиях как частично чужеродные. Аутоантитела к кардиолипину – это антитела, направленные организмом против собственного кардиолипина.
Клетки человека, больного сифилисом выделяют в большом количестве липоидный и липопротеиноподобный материал, сходный с кардиолипином. Бледная трепонема приводит к поражению внутренних органов, в частности, к повреждению печени и сердца, освобождая некоторые фрагменты тканей. При интенсивном размножении спирохет в организме больного происходит распад тканей, в результате чего из поврежденных клеток высвобождаются липоидные молекулярные фрагменты.
Иммунная система пациента реагирует, вырабатывая реагиновые антитела на эти фрагменты. Продукты распада клеток — липоидные белки — поступают в кровяное русло. Эти белки являются чужеродными для организма человека, поэтому реакция организма проявляется в виде выработки неспецифических антител (иммуноглобулинов) класса IgM и IgG к липоидному и липопротеиноподобному материалу. Именно эти антитела исторически называются реагинами.
Следует иметь в виду, что реагины с помощью кардиолипиновых тестов могут обнаруживаться в организме людей, никогда не болевших сифилисом, т.к. их количество повышается при различных физиологических и патологических состояниях, не связанных с сифилисом, например у пациентов с аутоиммунными, воспалительными и гематологическими заболеваниями. Эти реагины могут быть причиной так называемых биологических ложноположительных серологических реакций на сифилис.
Антилипидные (неспецифические) антитела появляются в организме человека со стадии первичного сифилиса —примерно через 7-14 дней после образования твердого шанкра, через 4-5 недель после заражения.
Антитела против кардиолипина выявляют посредством нетрепонемных серологических тестов. При нетрепонемных методах анализа на сифилис не различают тип антител (IgG, IgM или др.), а определяют суммарный ответ.
2. Специфические антитела при сифилисе
Специфические антитрепонемные антитела направлены против бледной трепонемы. Плазматические клетки организма вырабатывают специфические антитела, направленные против соответствующих антигенов возбудителя заболевания.
На ранних этапах развития сифилиса, как бактериальной инфекции, у заболевшего человека осуществляется выработка специфических антител, относящихся преимущественно к иммуноглобулинам класса M (первичный иммунный ответ). Трепонемоспецифические Ig класса M у больных сифилисом могут регистрироваться даже в период инкубации. Позднее происходит переключение на синтез IgG (вторичный иммунный ответ).
Параметры иммунного ответа могут изменяться в результате проводимого лечения. Адекватное лечение раннего сифилиса приводит к быстрому снижению титров неспецифических антител и специфических IgM.
По мере развития патологического процесса постепенно включаются механизмы образования антител классов G и А. Ведущая роль в гуморальном ответе переходит к специфическим антителам IgG и IgА. При этом специфические IgG обычно сохраняются в сыворотке крови в течение длительного периода времени,а иногда и всю жизнь
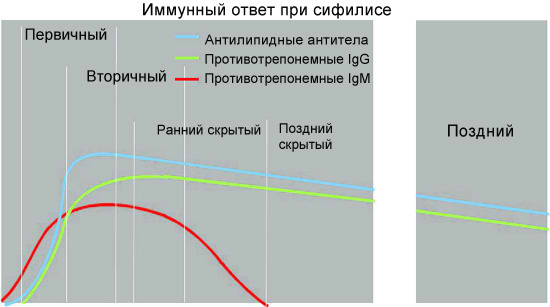
Динамика образования специфических антител у больного при сифилисе
По данным современных исследований, гуморальный ответ при сифилисе происходит в соответствии с общими закономерностями для бактериальных инфекций. Вначале вырабатываются иммуноглобулины класса M против наиболее иммуногенных и специфичных антигенов возбудителя. Специфические антитела класса M способны выявляться в крови пациентов, инфицированных T. pallidum, на самых ранних этапах развития инфекции, уже через 1,5-2 недели после заражения, что клинически соответствует скрытому инкубационному периоду заболевания. При первичном и вторичном сифилисе содержание указанных антител в крови больных быстро нарастает и сохраняется на высоком уровне; максимальное их содержание у больных сифилисом приходится на 6—9-ю неделю заболевания.
После успешного лечения антибактериальными препаратами специфические IgM у больных относительно быстро элиминируют из кровотока (через 3—12 месяцев). При лечении раннего сифилиса IgM исчезают через 3-6 месяцев, позднего – через 1 год. Большое диагностическое значение приобретает выявление антитрепонемных антител IgM в крови новорожденных. Так как IgM не проходит через плаценту, выявление антитрепонемных IgM-антител у новорожденного указывает на врожденный сифилис. Точно так же IgM-антитела не проникают через гематоэнцефалический барьер, и их появление в спиномозговой жидкости говорит о нейросифилисе.
Многие лабораторные методики диагностики сифилиса основаны именно на выявлении трепонемоспецифических IgM. Например, иммуноферментный анализ (ИФА) на твердой фазе и линейный иммуноблоттинг (ИБ) на микропористых стрипах с использованием антивидовых конъюгатов на основе моноклональных антител к тяжелой мю-цепи в структуре IgМ человека, а также реакция непрямой иммунофлюоресценции (РИФ) с исследованием 19S-фракции сыворотки крови, содержащей тяжелые IgМ.
Раннее определение специфических IgM также может быть применено для своевременного выявления случаев раннего врождённого сифилиса (определение специфических IgM в крови новорожденных) или случаев реинфекции у пациентов, ранее перенесших сифилис.
Без лечения, по мере развития болезни и разрешения клинических проявлений вторичного периода, уровень специфических IgМ в крови больных сифилисом постепенно понижается и начинает преобладать синтез IgG. Развитие иммунного ответа на антигенную стимуляцию в организме больного сифилисом сопровождается постепенным переключением с синтеза антител класса M на продукцию более мелких молекул иммуноглобулинов класса G.
Специфические иммуноглобулины класса G в кровотоке больных сифилисом появляются более поздно, в конце 3-й или на 4-й неделе после заражения и, как правило, достигают более высоких титров, чем IgM. Уже на 6 неделе после инфицирования уровень IgG преобладает над уровнем IgM и может сохраняться в таком состоянии годы.
Содержание специфических IgG, постепенно увеличиваясь, достигает максимальной выраженности через 1—1,5 года, после чего несколько снижается, подвергаясь волнообразным колебаниям в зависимости от активности инфекционного процесса. Количество специфических IgG в циркулирующей крови после адекватно проведенного лечения снижается медленно. Антитела этого класса могут сохраняться даже после клинического излечения пациента в течение десятков лет или пожизненно.
Кроме перечисленных видов антител, в гуморальном иммунитете при сифилисе принимают участие иммуноглобулины класса А. Антитела IgA вырабатываются в сравнительно небольших количествах. Вопрос о синтезе IgE и IgD в настоящее время изучен недостаточно.
Источник
