Презентации особенности противовирусного иммунитета

1.
ПРОТИВОВИРУСНЫЙ
ИММУНИТЕТ
2.
Особенности вирусов как облигатных внутриклеточных паразитов
определяют характер иммунитета при вирусных инфекциях.
Вирусы:
1. могут инфицировать ткани не вызывая воспалительных реакций;
2. могут реплицироваться в клетках на протяжении всей жизни не повреждая
их;
3. иногда нарушают некоторые специализированные функции клетки, не
вызывая явных нарушений функций целостного органа
В макроорганизме вирус может находиться в различных состояниях:
внеклеточно (вирион);
внутриклеточно, на разных стадиях быстрого или медленного
продуктивного взаимодействия с чувствительной клеткой (вирус);
быть интегрированным в геном клетки-мишени (непродуктивное
взаимодействие, провирус).
На вирус развиваются иммунологические реакции двух типов:
1) направленные против вириона (преимущественно гуморальные реакции);
2) действующие на клетку, инфицированную вирусом (преимущественно
клеточные).
3. Противовирусный иммунитет
Факторы
естественной(врожд
енной) защиты.
Кожные
покровы,
слизистые
Клеточные (естественные
киллеры,
макрофаги).
Гуморальные — (интерфероны,
система
комплемента,ингибиторы
вирусов)
Факторы адаптивного
иммунитета.
Клеточные
(цитотоксические
Тклетки СD 8+,
CD4+).
Гуморальны
факторы
(противовирусные
антитела)
4. Первый защитный барьер при вирусной инфекции – врожденный иммунитет
кожные покровы и слизистые оболочки (механические
барьеры)
гуморальные
факторы
сыворотки
и
других
биологических жидкостей
клеточные факторы: фагоцитирующие клетки, включая
нейтрофила и моноциты/макрофаги, и нормальные
киллеры (NK-клетки);
Лихорадкаповышенная
температура
может
непосредственно воздействовать на сложные вирусы,
ингибирует репликацию некоторых
вирусов.
5. Гуморальные факторы. Интерфероны
Интерфероны – гликопептиды, вырабатывающиеся и аккумулирующиеся во
всех ядросодержащих клетках крови и эпителиальных клетках слизистых
оболочек
являются цитокинами с широким спектром биологических активностей:
противовирусное действие, ингибирование гемопоэза; модуляция
иммунного и воспалительного ответов, регуляция пролиферации и
дифференцировки клеток и т.д.
При вирусной инфекции клетки синтезируют интерферон и секретируют его
в межклеточное пространство, где он связывается со специфическими
рецепторами соседних незараженных клеток.
Связанный интерферон оказывает противовирусное действие.
– Конечный результат состоит из образования барьера из устойчивых к вирусу
неинфицированных клеток вокруг очага инфекции, чтобы ограничить ее
распространение.
–
6. Интерфероны
α-интерфероны (α-ИФ) – лейкоцитарный ИФ — семейство
включает около 20 белков, продуцируются в основном
лейкоцитами и макрофагами;
β- интерфероны (β-ИФ) – фибробластный – известно β1 и
β2-ИФ, продуцируются в основном фибробластами;
γ- интерфероны – продуцируются активированными Т-
лимфоцитами хелперами 1-го типа и NK-клетками.
α-ИФ и β-ИФ – интерфероны 1 типа
γ- интерфероны – интерфероны 2 типа
7. Интерфероны
Основные эффекты
интерферонов.
α-интерфероны
β-интерфероны
γ-интерфероны
Противоопухолевое
действие
сильное
сильное
умеренное
Противовирусная
активность
сильная
сильная
слабая
Иммуномодулирующая
активность
умеренная
умеренная
сильная
Индукторы
вирусы
вирусы
антигены
Основные клеткипродуценты
МФ
Эпителий,
фибробласты
Т-лф, NK
8. Интерфероны
Все клетки человеческого организма в ответ на вирусную
инфекцию способны вырабатывать α-интерфероны или βинтерфероны .
Мощным индуктором синтеза этих интерферонов
является двухцепочечная РНК, поэтому РНКсодержащие вирусы активируют синтез сильнее, чем
ДНК-содержащие вирусы.
Интерфероны альфа и бета используют общий рецептор
(IFNAR), который экспрессируется на большинстве
клеток организма, в том числе на фибробластах, Тлимфоцитах, макрофагах или дендритных клетках.
Связывание с рецептором в конечном счете запускает
сигнальные пути в клетке
9.
Интерферон подавляет
репродукцию вирусов,
воздействуя на транскрипцию
их геномов тремя различными
способами.
Первый способ состоит в
индукции синтеза 2′,5’олигоаденилатсинтетазы . В
присутствии двухцепочечной
РНК 2′,5’олигоаденилатсинтетаза
полимеризует АТФ с
образованием 2′,5’олигоаденилатов, которые в
свою очередь активируют
рибонуклеазу L , разрушающую
одноцепочечные РНК.
Второй способ заключается в индукции синтеза протеинкиназы PKR . Эта
протеинкиназа, которая также активируется двухцепочечной РНК, путем
фосфорилирования блокирует фактор инициации трансляции eIF2альфа , что
приводит к подавлению синтеза белка в зараженной клетке.
В основе третьего способа лежит индукция синтеза белков Мх , обладающих
ГТФазной активностью. Mx белки препятствуют росту РНКовых вирусов, ингибируя
транскрипцию вирусных белков и другие шаги их жизненного цикла
Интерфероны действуют неизбирательно, блокируя синтез не только вирусных, но и
клеточных РНК и белков
10. Биологическая роль ИФН 1 типа в организме
11. Роль ИФН α/β, ИЛ-12, ИЛ-15 в активации NK-клеток и CD8+ T-лимфоцитов
12. Гуморальные факторы.
Комплемент способен инактивировать некоторые вирусы
( ретровирусы), имеют на поверхности белки, служащие рецептором
для CIq компонента комплемента;
Нормальные антитела – связывают внеклеточную форму вируса , а
в присутствие комплемента лизируют клетки, зараженные вирусом.
Ингибиторы
вирусов
–
протеины,
липопротеиды,
мукополисахариды.
Присутствуют в интактном организме.
Альфа-дефензины – семейство положительно заряженных
пептидов. Обладают антивирусной активностью. Взаимодействуют с
HIV.(см. презентация естественный иммунитет)
13. Нормальные киллеры (NK-клетки)
Нормальные киллеры
клетки)
(NK-
Нормальные киллеры или NK (от англ. natural killer) это большие зернистые лимфоциты
У человека составляют примерно 5% лимфоцитов периферической крови.
Лишены маркеров Т — и В-лимфоцитов.
NK узнают определенные структуры высокомолекулярных гликопротеинов, которые
экспрессируются на мембране инфицированных вирусом клеток.
Узнавание клетки-мишени и сближение с ней происходит за счет рецепторов NK.
В результате NK активируются, и содержимое гранул выбрасывается во внеклеточное
пространство.
Главная роль здесь принадлежит перфорину (цитолизину), имеющему некоторое
структурное сходство с компонентом комплемента C9 (антитела к перфорину
подавляют внеклеточное уничтожение).
Перфорин встраивается в мембрану клетки — мишени и образует трансмембранные
поры, что приводит к гибели клетки
Кроме того, гранулы NK содержат две сериновые протеинкиназы, которые могут
функционировать как цитотоксические факторы, но не вполне ясна их роль в NKзависимом лизисе
14. Нормальные киллеры (NK- клетки
Нормальные киллеры (NKклетки
Механизм дифференциации нормальных и
вирусинфицированных клеток связан с двумя
рецепторами, экспрессирующимися на
мембране НК-клеток. Один из них — NKR-P1 является основным в реализации киллерной
функции данных клеток.
В результате взаимодействия этого рецептора с соответствующим лигандом на любой из
возможных клеток создаются условия для реализации киллерного действия.
При этом действие НК-клеток против собственных нативных клеток блокируется
вторым рецептором — Ly49 , способным контактировать с молекулами I класса МНС ,
что предотвращает лизис нативных собственных клеток.
Инфицированные вирусом клетки становятся чувствительными к НК одним из двух
способов.
некоторые вирусы подавляют белковый синтез в клетках хозяина, в результате
селективно блокируется синтез молекул I класса МНС, индуцированный интерфероном,
и Ly49-рецептор будет не в состоянии предотвращать киллерную активность НК-клеток.
некоторые вирусы препятствуют экспрессии молекул I класса МНС, что также делает
вирусинфицированные клетки объектом киллерного действия НК-клеток.
15. Фагоцитирующие клетки
Моноциты и макрофаги являются одними из
первых типов клеток, которые сталкиваются
с вирионами в разных анатомических
областях организма.
Макрофаги обеспечивают противовирусную резистентность несколькими
путями:
внешняя резистентность проявляется в способности макрофагов
инактивировать внеклеточно расположенные вирусы; угнетать вирусную
репликацию в окружающих клетках за счет продукции интерферонов,
других цитокинов и белков системы комплемента, обладающих
противовирусными свойствами; разрушать инфицированные клетки,
включая антителозависимую цитотоксичность;
внутренняя резистентность характеризуется способностью макрофагов
угнетать вирусную репликацию внутри самих макрофагов, связанную с их
фагоцитарной функцией и, возможно, с блоком на отдельных стадиях
репликации вируса; фагоцитоз вирионов, пораженных вирусом клеток, а
также комплексов антиген — антитело может завершиться перевариванием,
но многие вирусы реплицируются или, по крайней мере, выживают внутри
макрофагов, что может быть источником распространения инфекции;
16. Противовирусный иммунитет
При острых инфекциях с коротким
периодом инкубации, высокой
скоростью репродукции основная
защита осуществляется факторами
врожденного иммунитета.
При продолжительной инфекции,
генерализованной инфекции, на более
поздних стадиях основная роль
принадлежит адаптивному иммунитету.
17. Гуморальные факторы адаптивного иммунитета
При образовании комплекса антиген (вирион)-антитело происходит
нейтрализация вируса, таким образом блокируется начальный этап
взаимодействия вируса с клеткой
Кроме того, антитела остаются прикрепленными к вирусам после
проникновения внутрь клетки, таким образом осуществляется запуск
внутриклеточного иммунного ответа, который блокирует вирионов в
цитозоле клетки. Было показано, что клетки обладают рецепторами
цитозольного IgG, белка, который распознаёт наличие антитела и включает
мощную систему распада вируса.
Антитела участвуют в разрушении инфицированных вирусом клеток,
активируя систему комплемента.
Антитела, связанные с вирусными антигенами на поверхности зараженных
клеток обеспечивают антителозависимую цитотоксичность, опосредованную
НК, макрофагами и нейтрофилами( при невысокой экспресси, вирусных
антигенов)
18. Гуморальные факторы адаптивного иммунитета
Антитела
1. Секреторный IgА
Эффекты
Блокирование связывания вируса с клеткой хозяина
(предохраняют от инфицирования и реинфекции)
2. IgА, IgМ, IgG
Блокирование проникновения вируса внутрь
клетки-хозяина
Агглютинация вирусных частиц
3. IgМ
4. IgМ, IgG
Усиление фагоцитоза вирусных частиц
(опсонизация вирусных частиц).
Активация комплемента и лизис вирусных частиц
Антитела малоэффективны в защите организма от хронических и медленных
инфекций.
Недостаточная концентрация антител может усиливать репродукцию вируса,
В отдельных случаях антитела даже могут защищать вирус от действия
протеолитических ферментов клетки, что в случае сохранения его
жизнеспособности в конечном итоге приводит к усилению репликации
вируса.
19.
20. Противовирусный Т- клеточный иммунитет.
Противовирусный Тклеточный иммунитет.
Основной формой защиты организма от вирусных инфекций является
клеточный иммунитет.
Основными эффекторами клеточного противовирусного иммунитета
являются Т-цитотоксические лимфоциты (CD8+-клетки).
При большинстве вирусных инфекций специфические Т-киллеры
появляются через 3-4 дня после инфицирования, а пик их количества
наблюдается к 7-10 дню. Это связано с тем, что процесс трансформации
наивных Т-киллеров в эффекторные Т-киллеры сопряжен со сложными
метаболическими и структурно-функциональными преобразованиями,
которые сопровождаются пролиферацией и дифференцировкой клеток.
Для цитотоксического действия Тс-лимфоцитам необходим
непосредственный контакт с клеткой-мишенью. После этого происходит
выделение Тс-лимфоцитом гранзимов или цитолизинов, вызывающих
изменение мембранной проницаемости клетки-мишени.
21. Противовирусный Т- клеточный иммунитет.
В отличие от В-системы иммунитета , которая
нейтрализует антиген с помощью антител, Т-система уничтожает
антигены, представленные на клетках, через прямое
взаимодействие субпопуляции T-клеток — специфических Тцитотоксических лимфоцитов (CD8+-клетки) с измененными
собственными или чужеродными клетками.
Вторая отличительная черта Т-клеток связана с особенностями распознавания
антигена: Т-клетки распознают не собственно антигенный пептид (эпитоп), а его
комплекс с молекулами I или II классов МНС
Индуцированные вирусными антигенами Т-лимфоциты распознают и уничтожают
только те зараженные клетки, на поверхности которых вирусный АГ сцеплен с АГ
главного комплекса гистосовместимости (МНС класса I).
Уничтожение зараженных клеток происходит на ранней стадии репродукции вирусов
до появления нового поколения вирусных частиц.
Источник

Противовирусный иммунитет Выполнила: Сливнева Анна Андреевна
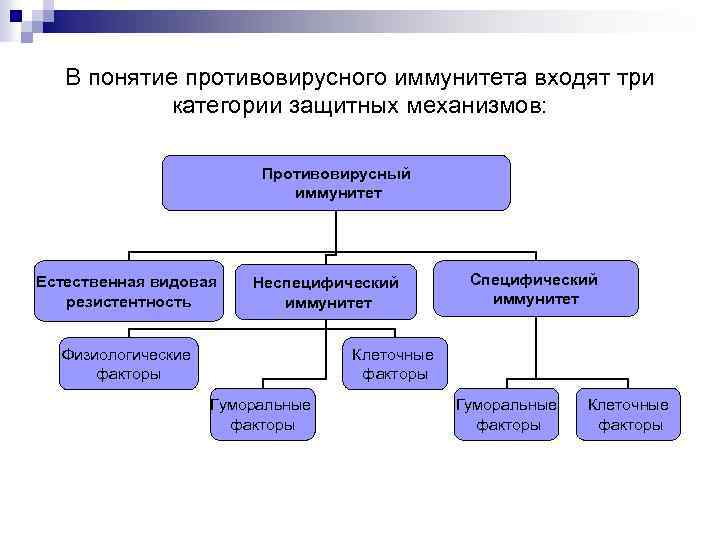
В понятие противовирусного иммунитета входят три категории защитных механизмов: Противовирусный иммунитет Естественная видовая резистентность Неспецифический иммунитет Физиологические факторы Специфический иммунитет Клеточные факторы Гуморальные факторы Клеточные факторы

Естественная видовая резистентность n n n Невосприимчивость животных. Обусловлена отсутствием условий для размножения вируса из за неспособности клеток обеспечивать проникновение и депротеинизацию вируса. В естественно невосприимчивом организме отмечается ничтожный выход вируса за пределы местного очага, подавляющая масса его разрушается в месте первичной локализации. например, лошади не болеют ящуром, КРС – сапом, собаки – чумой свиней. Влияние возраста. Примером влияния возраста на восприимчивость к вирусу является высокая чувствительность новорожденных мышат, крольчат и котят к вирусу ящура. Взрослые животные этих видов абсолютно резистентны к этому возбудителю. Генетическая обусловленность и наследование видового иммунитета. Видовой иммунитет (или его отсутствие) к определенному вирусу генетически обусловлен и передается из поколения в поколение в пределах определенных генетических линий одного и того же вида животных. Например, линия мышей РR-1 обладает 100% резистентностью к вирусу желтой лихорадки, тогда как мыши линии swiss восприимчивы к этому вирусу в 100% случаев.

Неспецифический иммунитет. Общие физиологические факторы n n Кожно-слизистые барьеры выдерживают первую атаку вирусов. Неповрежденная кожа и слизистая оболочка служат не только механической преградой, но и являются стерилизующим фактором. Если вирусы преодолели кожные и слизистые барьеры, то начинается их массивное проникновение в ткани. В инфицированный участок быстро прибывает огромная масса фагоцитов, и таким образом создается защитный вал вокруг воспалительного очага, при этом ограничивается распространение микробов в соседние органы и ткани. Роль температуры тела. При повышении температуры тела усиливаются процессы иммуногенеза, ускоряется обмен веществ, усиливается продукция интерферона, что в совокупности способствует выздоровлению. Повышение температуры тела вызывает непосредственную инактивацию внеклеточного вируса и способствует подавлению репродукции вируса внутри клетки, а также ускоряет обменные процессы в клетках и в организме, что сопровождается снижением р. Н внеклеточной и внутриклеточной среды. Кислая среда подавляет вирусы и, наоборот, благоприятно влияет на ингибиторы, содержащиеся в тканях и жидкостях организма.

n Выделительная система принимает участие в удалении вирусов. Вирусы через короткое время появляются в моче, они способны проходить через почечный фильтр. Это вирусы гриппа, кори, чумы, ящура. Вирусы выделяются из организма не только почками, но и другими выделительными системами со слюной (грипп, бешенство), секретами при респираторных заболеваниях, кишечником, пораженными клетками, эритроцитами. Выделение вирусов в окружающую среду способствует более быстрому восстановлению относительного постоянства внутренней среды организма.

Гуморальные факторы n Ингибиторы – это неспецифические противовирусные вещества белковой природы, которые присутствуют в нормальной сыворотке крови, секретах эпителия слизистых оболочек дыхательного и пищеварительного трактов, в экстрактах органов и тканей. Они обладают способностью подавлять активность вирусов внечувствительной клетке: при нахождении вируса в крови и жидкостях. Ингибиторы подразделяют на термолабильные – обладают широким диапазоном вируснейтрализующего действия, способны блокировать гемагглютинирующую активность вирусов и нейтрализовать инфекционные и иммуногенные свойства ингибиторочувствительных вирусов; и термостабильные – блокируют гемагглютинирующую, но неинфекционную активность вируса. Помимо сывороточных ингибиторов различают ингибиторы тканей, секретов и экстрактов. Они активны в отношении многих вирусов. Слизистые оболочки дыхательных путей – входные ворота для многих вирусов, часть которых размножается в этом районе. Попадая на поверхность носоглотки или трахеи, респираторные вирусы погружаются в слизистый секрет, наделенный противовирусной активностью.

Защитные факторы секрета имеют специфическую и неспецифическую природу: — специфический компонент секретов респираторного тракта представлен секреторным иммуноглобулином А; — неспецифическая активность секреторных ингибиторов связана с действием местных ингибиторов, которые обладают антигемагглютинирующей и вируснейтрализующей активностью. Механизм действия ингибиторов заключается в соединении их с вирусами, вызывая нейтрализацию вирусных рецепторов, что выражается в понижении их физико-химических адсорбционных свойств. В результате вирусы теряют способность адсорбироваться на поверхности чувствительных клеток и проникать в них; вирусные частицы отторгаются с поверхности чувствительных клеток. Защитная функция ингибиторов зависит от: — природы вируса; — количества вируса; — активности самих ингибиторов; — индивидуальных и возрастных особенностей.

n Пропердин (гамма-глобулин) содержится в нормальной сыворотке крови и принимает участие в нейтрализации вирусов. Активность проявляется за счет не самого пропердина, а системы пропердина (комплемента и двухвалентных ионов магния). n Гормоны опосредовано влияют на резистентность к вирусным агентам. В защитных реакциях организма принимают участие два антагонистически действующих гормона: кортизон (гидрокортизон) и соматотропный гормон. Большие дозы кортизона снижают резистентность организма как к бактериальным, так и к вирусным инфекциям; он понижает воспалительную и фагоцитарную реакции, замедляет клиренс крови от бактерий и вирусов, понижает продукцию антител и интерферона. Малые дозы, наоборот, повышают защитные функции организма. Соматотропный гормон, продуцируемый передней долей гипофиза, в отличии от кортизона активирует воспалительный процесс, усиливает активность плазматических клеток, которые продуцируют антитела.

Клеточные факторы n Фагоцитоз играет важную роль в защите организма от вирусных инфекций, но проявляется фагоцитозом не вирионов, а инфицированных ими чувствительных клеток, эритроцитов, тромбоцитов и других частиц, доступных для фагоцитоза. Макрофаги – это полиморфная группа клеток, активно фагоцитирующих чужеродный материал, попавший в кровоток: моноциты крови, клетки костного мозга, купферовские клетки печени, гистиоциты, макрофаги селезенки, лимфатических узлов и серозных полостей. Макрофаги принимают участие в процессе антителообразования, вступая в кооперацию с Т- и Вклетками (лимфоцитами). Т-лимфоциты – это тимусзависимые иммуноциты. В-лимфоциты – это клетки, происходящие из клеток предшественников костного мозга, которые мигрируют в определенные участки лимфатических узлов и селезенки. Большинство В-клеток локализовано в лимфатических тканях, другая их часть может циркулировать с лимфой и кровью. Фагоцитозу возбудителей макрофагами способствуют специфические антитела, оказывающие опсонирующее и агглютинирующие действия на вирусы. Также фагоциты являются продуцентами антител и интерферона.

Роль лейкоцитов в противовирусном иммунитете малоэффективна. Вирусы адсорбируются на лейкоцитах и поглощаются ими, но последующего разрушения их в клетках не происходит: весь процесс останавливается на стадии незавершенного фагоцитоза. Попытки в экспериментальных условиях перевести незавершенный фагоцитоз в завершенный не дали положительных результатов. Неспособность макрофагами переваривать вирусы – одна из основных особенностей механизма противовирусного и противобактериального иммунитета.

n Интерферон – особый противовирусный белок, продуцируемый зараженными клетками или целым организмом. Он обладает антивирусной, антипролиферативной и иммуномодулирующей активностью. По химической природе интерферон представляет собой гликопротеид. Он инактивируется при замораживании и оттаивании, при нагревании, облучении ультрафиолетовым излучением, разрушается трипсином и пепсином. На него не действуют рибонуклеаза и дезоксирибонуклеаза, специфические иммунные сыворотки. Он не обладает токсичностью и антигенностью; его активность проявляется как в кислой, так и в щелочной среде. Интерферон содержится в крови, моче, спинномозговой жидкости, смывах носоглотки, в различных тканях и органах организма. Интерферон не влияет на адсорбцию вируса, виропексис, депротеинизацию вирионов, освобождение вирусной нуклеиновой кислоты, композиция вирионов и выход их из клетки. Он не действует на внеклеточный вирус, он подавляет его репродукцию, т. е. действует на вирус опосредованно через чувствительные клетки, в которых не нарушен синтез клеточных белков. Интерферон обладает видотканевой специфичностью, т. е. более активен в той биологической системе, в которой репродуцирован. Интерферон связывается с клеточными рецепторами, находящимися на плазматической мембране, что служит сигналом для депрессии соответствующих генов. В результате индуцируется синтез протеинкиназы. Она фосфорилирует субъединицу инициирующего фактора трансляции и фосфорилирование блокирует активность инициирующего фактора.
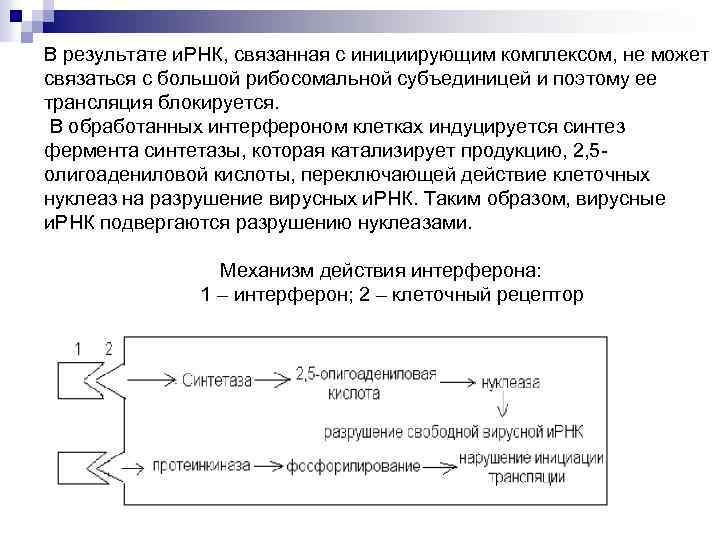
В результате и. РНК, связанная с инициирующим комплексом, не может связаться с большой рибосомальной субъединицей и поэтому ее трансляция блокируется. В обработанных интерфероном клетках индуцируется синтез фермента синтетазы, которая катализирует продукцию, 2, 5 олигоадениловой кислоты, переключающей действие клеточных нуклеаз на разрушение вирусных и. РНК. Таким образом, вирусные и. РНК подвергаются разрушению нуклеазами. Механизм действия интерферона: 1 – интерферон; 2 – клеточный рецептор

Блокирование интерфероном стадии инициации трансляции и разрушение и. РНК И обуславливает его универсальный механизм действия при инфекциях, вызванных вирусами с разным генетическим материалом. Интерферон защищает клетки от вирусной инфекции лишь в том случае, если воздействует на них до контакта с вирусом. В организме и в клеточных культурах он оказывает как иммуностимулирующее, так и иммуносупрессивное действие. Интерферон активизирует эффекторные клетки иммунной защиты, главным образом макрофаги и киллерные клетки, повышая их способность убивать опухолевые клетки. Он тормозит рост пролиферирующих клеток. Одним из многих свойств лейкоцитарного α- и фибробластного βинтерферона является их способность усиливать фагоцитарную активность макрофагов. Макрофаги, подвергнутые воздействию интерферона, имеют значительно больше вакуолей, быстрее прикрепляются к стеклу, активнее захватывают живых бактерий.

Специфический иммунитет. Гуморальные факторы n При вирусных инфекциях образуется вируснейтрализующие, комплементсвязывающие и преципитирующие антитела. Специфические противовирусные антитела вырабатываются на рибосомах плазматических клеток – в лимфоцитах при тесном взаимодействии их с Т-лимфоцитами и макрофагами. Противовирусные антитела связаны с глобулиновой фракцией сывороточных белков (Ig): A, M, G, E, D. Наибольшее значение имеют Ig. G, Ig. A, Ig. M, в то время как защитная функция Ig. D и Ig. E сравнительно не велика, а Ig. Е связывают с возникновением аллергии. Роль антител в противовирусном иммунитете высока. Существует прямая зависимость между восприимчивостью организма и концентрацией антител в крови. Формирование иммунитета при вирусных инфекциях зависит от сроков появления антител; степень напряженности иммунитета возрастает по мере повышения уровня антител. Действие специфических противовирусных антител направлено на вирусную частицу или ее отдельные компоненты, а не на клетки.

В основе первичного взаимодействия антител с гомологичным вирусом лежит процесс специфической адсорбции: молекула антитела присоединяется к поверхности вирусной частицы, изменяет ее физико-химические свойства. В результате вирус становится неспособным соединяться с рецептором чувствительной клетки и проникать в нее. Нейтрализация вируса антителами представляет собой подвижный процесс, который зависит от: — массы; — количества этих двух реагирующих систем; — ионной концентрации солей; — температуры; — других факторов, влияющих на взаимодействие вируса и антитела. При избытке антител инактивация вируса может быть полной. Скорость иммунологической реакции зависит от: — концентрации антител; — времени их воздействия на вирус.

Действие специфических противовирусных антител направлено на инактивацию вирусов, находящихся только вне клетки в экстрацеллюлярной среде. И это действие осуществляется на молекулярном уровне на трех линиях защиты: — в местах входных ворот вирусов; — на пути продвижения их к восприимчивым клеткам; — на самой территории клеток с вирусами, находящимися в клетках. Противовирусные антитела способны вступать в реакцию с вирусом, уже адсорбированным на поверхности клеток. При этом они вызывают нейтрализацию гемагглютинирующих свойств вируса, в результате чего происходит отторжение вирусных частиц с поверхности клетки. Антитела могут изменить развитие инфекции путем воздействия на чувствительные к вирусам клетки. Это доказано в результате применения иммунных сывороток при различных вирусных инфекциях (гриппе, кори, клещевом энцефалите). Введение иммунных сывороток в ранние сроки заболевания оказывает положительный лечебный эффект. В этом случае они блокируют уже пораженные вирусом клетки, которые остаются в первичном очаге. В результате этого предотвращается распространение патологического процесса. Структуры и функции пораженных вирусом клеток антитела не восстанавливаются.

Клеточные факторы включают: n n Т-лимфоциты формируются из незрелых стволовых клеток в тимусе, В-лимфоциты формируются – в фабрициевой сумке. Тлимфоциты первыми распознают чужеродный антиген в организме, вырабатывают особые вещества (медиаторы), которые активизируют моноциты и В-лимфоциты, убивают клетки с адсорбированными на них вирусами, вырабатывают интерферон. В-лимфоциты под действием переработанного моноцитами антигена и медиаторов превращаются в плазмоциты, вырабатывающие специфические антитела. Некоторые формы Т-лимфоцитов (киллеры, супрессоры, хелпер) и В-лимфоциты вместе с моноцитами образуют мощный клеточный фактор защиты организма от вирусов.
Источник
