Противогрибковый иммунитет что это такое

Автор Камуллина Анна Евгеньевна На чтение 6 мин. Просмотров 2k. Опубликовано 01.08.2019
Данный паразит размножается с помощью спор или мицелия. У него нет белковых сигнатур (фрагментов ДНК), по которым защитные тела обычно определяют и запоминают возбудителей «животного» типа – бактерии, вирусы, микроорганизмы. Потому противогрибковый иммунитет не вырабатывается даже после многократных заражений. Но разово и в зависимости от того, какие ткани были задеты, система резистентности способна остановить его распространение.
Противогрибковый иммунитет: что это такое?
Инфекции этого типа называются микозами, их могут провоцировать свыше 30 видов грибков. У некоторых есть своя «специализация», а некоторые всеядны и вызывают системные микозы. Наибольшей устойчивостью к ним среди всех органов тела отличается кожа.

Грибкам, как и любым растениям, кровоснабжение не нужно – достаточно только тепла, влаги и питательной среды, в роли которой выступают клетки тела. Кожа способна сопротивляться распространению грибковых инфекций благодаря:
- кислому балансу пота и кожного жира – он неблагоприятен для разрастания мицелия;
- блокирующим свойствам кожного жира – он связывает споры еще до контакта с эпидермисом;
- кератиноцитам – многофункциональным клеткам, ответственным за регенерацию, устойчивость кожи к механическим воздействиям, удержание в ней влаги, синтез медиаторов, запускающих воспаление в месте инфекции;
- клеткам Лангерганса – кожной разновидности макрофагов (поглощают возбудителя и переносят его в лимфоузлы для «знакомства» с внутриклеточными «инспекторами» лимфоцитами).
Ногти и волосы подвержены грибковым инфекциям намного сильнее, поскольку образующие их кератиноциты в одиночку с возбудителем не справятся, а «позвать на помощь» другие иммунные агенты они не могут из-за отсутствия кровоснабжения.
Помимо поверхности эпидермиса, грибки также могут попасть в ротовую полость и пищеварительный тракт с пищей или загрязненными пальцами/ногтями, в дыхательную систему – с воздухом. Желудок защищает от них себя и кишечник с помощью резко кислой среды, а щелочная благоприятна для их размножения.
Ротовой полости и пищеводу тоже нечего противопоставить им, кроме слюны с ее слабым расщепителем полисахаридов птиалином. Бронхи и легкие защищены от возбудителей различных типов, но размножающиеся спорами грибки составляют несчастливое исключение из списка. Их с трудом удается связать только слизью бронхов. А удалить их из легких при кашле или блокировать с помощью антител в легочном круге кровообращения невозможно.
Почему ослабевает?
Заражение грибами внутренних органов всегда носит вторичный характер. Несмотря на наличие ряда пробелов в «познаниях» медицины об иммунитете и его механизмах, уже доказано, что максимальную эффективность против них дают:
Народными средствами
28.57%
Проголосовало: 70
- ПМЯЛ – полиморфноядерные лейкоциты (фагоциты);
- Т-лимфоциты;
- NK-лимфоциты.
Лимфоциты являются тельцами лимфы и «родными братьями» лейкоцитов крови, способными, в отличие от них, проникать внутрь клеток. Они зарождаются и обучаются в тимусе – вилочковой железе, расположенной за грудинной костью. Их особенность как одного из иммунных звеньев заключается в почти полном отсутствии «аппетита» на только попавшие в организм вирусы с бактериями.
Лимфоциты исследуют клетки на наличие любых отклонений в структуре и уничтожают подобные «находки». А уже среди спровоцировавших агрессию лимфоцитов дефектов на равных могут оказаться ДНК вируса, встроенная в код клетки, простейшее или микроорганизм, прячущиеся за ее мембраной от прочих защитных тел, врожденный порок развития. Лимфоцитарную защиту еще часто называют клеточной. Она служит единственным для тела средством избавления от потенциально злокачественных клеток и внутриклеточных инфекций. Лимфо- и фагоцитарный иммунитет может ухудшиться из-за:
- наследственных иммунодефицитов;
- ВИЧ-инфекции;
- заражения вирусом герпеса (размножается в В-лимфоцитах);
- длительной работы «на износ» (особенно физической и/или сопровождающейся недоеданием);
- голода (включая диеты, дефицит животных продуктов и вегетарианство);
- сахарного диабета;
- радиоактивного облучения (особенно тимуса, что может спровоцировать и злоупотребление рентгеном грудной клетки);
- хронического стресса;
- приема иммунодепрессантов;
- терапии антибиотиками;
- химиотерапии.
Другая сторона вопроса в том, что даже нормальное функционирование указанных звеньев иммунитета не гарантирует от заражения грибами. Так, споры криптококков защищены от поглощения защитными агентами капсулой, а гистоплазмы упорны к попыткам их разрушить. Кокцидии же сами способны захватывать и уничтожать атаковавшие их тела.
Как повысить противогрибковый иммунитет?
Приблизительная норма содержания лимфоцитов в кровотоке равна 32-40%. Повышенный (не больше 46-48%) лимфоцитоз – еще не повод для беспокойства. Такое случается при ряде инфекций, беременности, у лиц с удаленной селезенкой, питающихся однообразно, недавно перенесших хирургическое вмешательство.

Главное здесь – убедиться, что он не злокачественный (есть отдельная форма рака лимфатической системы – лимфома). А вот пониженный (меньше 18%) указывает на растущий риск рака других тканей, грибковой и герпесвирусной инфекции. Его повышению способствует употребление в пищу:
- животных белков. Лимфоциты состоят из белков и строятся из аминокислот. Животный белок содержит их все, а растительный – только часть. Потому вегетарианство иммунитет определенно не укрепляет;
- ретинола. Или его предшественников каротинов. Витамином А богаты морковь, шпинат, курага, тыква, салат. Он усваивается, только будучи растворенным в любом жире. В день нужно съедать около 300 г моркови или 400-500 г – остальных продуктов (норма витамина в сутки – 100 000 МЕ);
- токоферола. Витамин Е также жирорастворим, а самым известным продуктом среди богатых им является растительное масло, особенно подсолнечное. Подойдут также семечки и орехи всех видов, белокочанная капуста, спаржа, авокадо, манго. Суточная норма токоферола составляет 100 мг, достичь ее можно со 150 мл растительных масел или примерно 450 г овощей/фруктов в день.
- цинка. Его одинаково часто можно встретить в растительных и животных продуктах – фасоли, говядине и индюшатине, злаках, устрицах и крабовом мясе. Суточная норма цинка составляет 11 мг, получить ее можно с 300 г и больше указанных продуктов;
- селена. Им богаты медуница лекарственная, чеснок, тунец, мясо краба, устрицы. В сутки его требуется примерно 60 мкг – около 250 г указанных продуктов.
Профилактика
Особенности противогрибкового иммунитета не исчерпываются лимфоцитарной защитой. Большая часть микопаразитов хорошо размножаются на коже благодаря оптимальным условиям – влаге, темноте и теплу. Оттого кожный грибок и предпочитает области между пальцами, в подмышечных впадинах, под молочными железами. А значит, в борьбе с грибками также важно:
- соблюдать идеальную гигиену кожи (пораженные участки можно обрабатывать слабыми антисептиками, начиная с уксуса и заканчивая хлоргексидином), одежды и обуви (глажка, включая носки, обработка паром, сушка);
- чаще загорать (в том числе, в солярии);
- не касаться здоровых участков кожи пальцами и предметами, которые только что контактировали с очагами инфекции;
- отказаться от спиртного – вредного для печени и повышающего температуру кожи наряду с потливостью.
В целях предупреждения инфекций не следует колоть дрова или разбирать завалы из трухлявого дерева голыми руками, без респиратора. Требует осторожности и контакт с сеном, особенно прошлогодним. Плесень на стенах комнат, включая ванную, или кранах, раковине, в других типичных местах следует своевременно протравливать с помощью хлора и альтернативных моющих средств. При ослабленном лимфоцитарном иммунитете к употреблению в пищу не допускаются плесневые сыры и продукты, изготовленные путем сбраживания (в том числе, квас, пиво и свежий хлеб), жирная ухаживающая косметика.
Источник
Особенности противовирусного, противогрибкового,
противоопухолевого, трансплантационного иммунитета.
Противовирусный иммунитет. Основой противовирусного
иммунитета является клеточный иммунитет. Клетки-мишени, инфицированные
вирусом, уничтожаются цитотоксическими лимфоцитами, а также NK-клетками и
фагоцитами, взаимодействующими с Fc-фрагментами антител, прикрепленных к
вирусспецифическим белкам инфицированной клетки. Противовирусные антитела
способны нейтрализовать только внеклеточно расположенные вирусы, как и факторы
неспецифического иммунитета — сывороточные противовирусные ингибиторы. Такие
вирусы, окруженные и блокированные белками организма, поглощаются фагоцитами
или выводятся с мочой, потом и др. (так называемый «выделительный иммунитет»).
Интерфероны усиливают противовирусную резистентность, индуцируя в клетках
синтез ферментов, подавляющих образование нуклеиновых кислот и белков вирусов.
Кроме этого, интерфероны оказывают иммуномодулирующее действие, усиливают в
клетках экспрессию антигенов главного комплекса гистосовместимости (МНС).
Противовирусная защита слизистых оболочек обусловлена секреторными IgA, которые, взаимодействуя с вирусами, препятствуют их
адгезии на эпителиоцитах.
Противогрибковый иммунитет. Антитела (IgM, IgG) при микозах
выявляются в низких титрах. Основой противогрибкового иммунитета является
клеточный иммунитет. В тканях происходит фагоцитоз, развивается эпителиоидная
гранулематозная реакция, иногда тромбоз кровеносных сосудов. Микозы, особенно
оппортунистические, часто развиваются после длительной антибактериальной
терапии и при иммунодефицитах. Они сопровождаются развитием
гиперчувствительности замедленного типа. Возможно развитие аллергических заболеваний после
респираторной сенсибилизации фрагментами условно-патогенных грибов родов Aspergillus, Penicillium, Mucor, Fusarium и др.Антигены
грибов имеют относительно низкую иммуногенность: они практически не индуцируют
антителообразование (титры специфических антител остаются низкими), но
стимулируют клеточное звено иммунитета — активированные макрофаги, которые
осуществляют антителозависимую клеточноопосредованную цит о токсичность г
рибов. Активированные макрофаги продуцируют перекисные и N0’—ион-радикалы
и ферменты,
которьК поражают мембрану клетки на расстоянии или
после фагоцитирования. Первичное распознавание чужеродных клеток происходит при
помощи FcR по антителам, которые связались с поверхностными антигенами
клеток-мишеней. При микозах наблюдается аллергизация макроорганизма. Кожные и
глубокие микозы сопровождаются, как правило, ГЗТ. Грибковые поражения слизистых
дыхательных и мочеполовых путей вызывают аллергизацию по типу ГНТ (реакция I
типа). Напряженность противогрибкового иммунитета оценивается по результатам
кожно-аллергических проб с грибковыми аллергенами.
Трансплантационным
иммунитетом — иммунную реакцию
макроорганизма, направленную против пересаженной в него чужеродной ткани
(трансплантата). Иммунная реакция на чужеродные клетки и ткани обусловлена чем,
что в их составе содержатся генетически чужеродные для организма антигены-
гистосовместимости, наиболее полно представлены на ЦПМ клеток. Реакция
отторжения не возникает лишь у однояйцовых близнецов. Выраженность реакции от
степени чужеродности, объема трансплант ируемою материала и состояния
иммунореактивност и реципиента. Основным фактором клеточного
трансплантационного иммунитета являются Т-киллеры. После сенсибилизации
антигенами донора мигрируют в ткани трансплантата и оказывают на них
антителонезависимую клеточноопосредованную цитотоксичность.Специфические
антитела, которые образуются на чужеродные антигены (гемагглютинины,
гемолизины, лейкотоксины, цитогоксины), имеют важное значение в формировании
трансплантационного иммунитета. Они запускают ан тителоопосредованный ци толиз
трансплантата (комплемен-опосредованный и антителозависимая
клеточноопосредован- ная цитотоксичность).
Механизм отторжения. В первой фазе вокруг трансплантата и сосудов
наблюдается скопление иммунокомпетентных клеток (лимфоидная инфильтрация), в
том числе Т- киллеров. Во второй фазе происходит деструкция клеток
трансплантата Т-киллерами, активируются макрофагапьное звено, естественные
киллеры, специфический антителогенез. Возникает иммунное воспатение, тромбоз кровеносных
сосудов, нарушается питание трансплантата и происходит его гибель. Разрушенные
ткани утилизируются фагоцитами.-В процессе реакции отторжения формируется клон
Т- и B-клеток иммунной памяти. Повторная попытка пересадки тех же органов и
тканей вызывает вторичный иммунный ответ, который протекае т очень бурно и
быстро заканчивае тся отторжением трансплантата. С клинической точки зрения
выделяют ос трое, сверхострое и отсроченное отторжение трансплантата.
Различаются они по времени реализации реакции и отдельным механизмам. Острое
отторжение — это «нормальная» реакция иммунной системы по механизму
первичного ответа, которая развивается в течение первых недель или месяцев
после трансплантации в отсутствие иммуносупрессивной терапии. В ее основе лежит
комплекс всевозможных цитолитических реакций, как с участием антител, так и
независимых от них.
Отсроченное
отторжение имеет тот же механизм, что
и острое. Возникает через несколько лет после операции у пациентов, получавших
иммуносупрессивную терапию. Сверхострое отторжение, или криз
отторжения, развивается в течение первых суток после трансплантации у
пациентов, сенсибилизированных к антигенам донора, по механизму вторичного
иммунного ответа. Основу составляет антительная реакция: специфические антитела
связываются с антигенами эндотелия сосудов трансплантата и поражают клетки,
активируя систему комплемента по классическому пути. Параллельно инициируется
иммунное воспаление и свертывающая система крови. Быстрый тромбоз сосудов
трансплан тата вызывает его острую ишемию и ускоряет некрогизацию пересаженных
тканей.
Иммунитет
противоопухолевый. Мутантиые клетки возникают в результате нелетального действия химических,
физических и биологических канцерогенов Мутантные клетки отличаются от
нормальных метаболическими процессами и антигенным составом, имеют измененные
антигены гистосовместимости.Они активируют гуморальное и клеточное звенья
иммунитета, осуществляющие надзорную функцию. Важную роль в этом процессе
играют специфические антитела (запускают комплемент-опосредованную реакцию и
антителозависимую клеточно-опос- редованную цитотоксичность) и Т-киллеры,
осуществляющие антителонезависимую клеточноопосредованную цитотоксичность.
Противоопухолевый
иммунитет имеет свои особенности,
связанные с низкой иммуногенностью раковых клеток. Эти клетки практически не
отличаются от нормальных, интактных морфологических элементов собственного
организма. Специфический антигенный «репертуар» опухолевых клеток также
скуден. В число опухольассоциированных антигенов входит группа раково-
эмбриональных антигенов, продукты онкогенов, некоторые вирусные антигены и
гиперэкспрессируемые нормальные белки. Слабому иммунологическому распознаванию
опухолевых клеток способствует отсутствие воспалительной реакции в месте
онкогенеза, а также их иммуносупрессивная активность — биосинтез ряда
«негативных» цитокинов, а также экранирование раковых клеток противоопухолевыми
антителами.
Механизм
основную роль в нем играют активированные макрофаги; определенное значение
имеют также естественные киллеры. Защитная функция гуморального иммунитета во
многом спорная — специфические антитела могут экранировать антигены опухолевых
клеток, не вызывая их цитолиза.
Вместе с тем, в последнее время
получила распространение иммунодиагностика рака основана на определении
раково-эмбриональных антигенов и опухоль-ассоциированных
Источник
Оглавление темы «Клеточные имунные реакции. Иммунная память. Иммунное реагирование при инфекциях. Иммунодефициты.»:
1. Клеточные имунные реакции. Индукция Т-клеточно-опосредованных реакций. Клеточный иммунитет.
2. Уничтожение клетки-мишени цитотоксическими Т лимфоцитами. Альтернативный механизм уничтожения клетки-мишени. Реакции ГЗТ. Реакции гиперчувствительности замедленного типа.
3. Иммунная память. Бустер эффект. Вакцинопрофилактика.
4. Иммунное реагирование при инфекциях. Иммунный ответ при вирусных инфекциях. Гуморальные иммунные реакции при вирусемии ( вирусных инфекциях ).
5. Клеточные иммунные реакции при вирусных инфекциях. Иммунный ответ при бактериальных инфекциях.
6. Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
7. Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.
8. Толерантность иммунитета. Устойчивость иммунной системы. Механизмы поддержания толерантности иммунитета.
9. Естественная толерантность иммунитета. Искусственная толерантность иммунной системы. Иммунный паралич. Расщеплённая толерантность иммунитета. Нарушения толерантности иммунной системы. Аутоимунные заболевания.
10. Иммунодепрессивное состояние. Иммунодефициты. Врождённые иммунодефициты. Гиперкортицизм ( синдром Кушинга ). Двусторонняя гиперплазия коры надпочечников ( болезнь Иценко-Кушинга ) при иммунодефицитах. Ионизирующая радиация и иммунодефицит.
Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
Грибковые клетки и их продукты — сильные иммуногены. Их распознавание иммунной системой проявляется в виде клеточных и гуморальных реакций. Многие грибковые Аг проявляют сенсибилизирующее действие, поэтому аллергический компонент — важное звено патогенеза микозов. Однако при микозах сенсибилизация не строго специфична, не отражает уровня иммунного реагирования и нередко не имеет прогностическое значение. Патогенные грибы содержат большой набор Аг.
Гуморальные реакции иммунитета при грибковых инфекциях
Большинство грибковых поражений сопровождается образованием высоких титров AT. Вид AT и нарастание концентрации отражают статус и прогрессирование инфекции. При микозах образуются высокие титры AT классов IgM, IgG и IgA; при сенсибилизирующем действии грибковых Аг дополнительно образуются IgE. Значение цитотоксического действия AT в комплементзависимом цитолизе невелика, так как комплемент непосредственно действует на грибковую клетку, активирующую его по классическому и альтернативному пути. Сложность антигенной структуры возбудителей микозов приводит к появлению значительного пула AT, не участвующих напрямую в уничтожении возбудителя и не проявляющих строгой видоспецифичности.
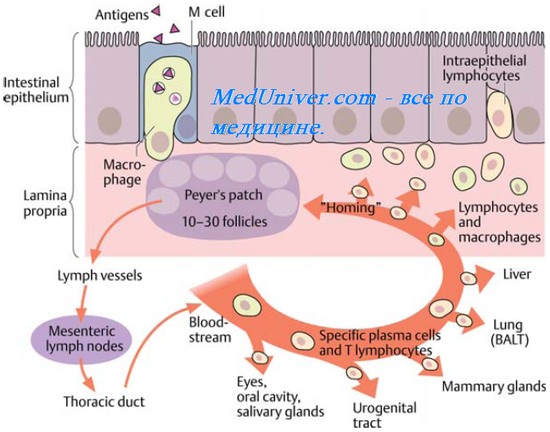
Клеточный иммунитет при грибковых инфекциях
Клеточные реакции играют основную роль в элиминации патогенных грибов. Исключая поверхностные микозы (где нет контакта между Аг и иммунокомпетентными клетками), у заражённых лиц развивается реакция ГЗТ, обнаруживаемая уже через 10-14 сут.
Предполагается, что основная роль в формировании резистентности принадлежит именно клеточным реакциям, но клинических данных, подтверждающих это положение, нет. В эксперименте показана важная роль ЦТЛ, так как их перенос сингенным реципиентам (клетки или организмы с идентичным набором Аг МНС) приводит к состоянию резистентности; участие Т-хелперов реализуется в активации клеток макрофагально-моноцитарной системы и полиморфноядерных клеток (при респираторных микозах) и стимуляции их фагоцитарной активности.
В ряде случаев иммунные реакции не только не препятствуют, но и способствуют развитию патологических реакций (гиперчувствительность, аутоиммунные поражения), что приводит к хроническому, рецидивирующему течению многих микозов.
— Также рекомендуем «Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.»
Источник
