Сигнал от опухоли на мрт

Преимущество МРТ перед иными методами обследования — возможность определить онкологию с самой ранней стадии заболевания и не только выявить метастазы, но и визуализировать их при локализации вне основного очага.
Послеоперационное сканирование позволяет уточнить влияние хирургического воздействия на основной очаг заболевания. Может ли МРТ показать рак еще до того, как малигнизированные атипичные клетки накопились в лимфоузлах? Какие перспективы в онко-диагностике открывает магнитно-резонансная томография?
МРТ в диагностике онкологических заболеваний
Можно ли на МРТ увидеть рак? Да — на самой ранней стадии, пока атипичные клетки еще не начали разрастаться. МРТ определяет рак в очагах, размеры которых еще не достигли 1 мм, то есть до появления новообразования. Если во время сканирования были визуализированы симптомы, указывающие на развитие опухоли, процедуру можно прервать и ввести контраст, чтобы уточнить топографию опухоли и стадию ее развития.
Отметим, что ответ на вопрос, видно ли опухоль на снимке, зависит от режима сканирования — чаще всего такие патологии диагностируются только при введении контрастного препарата в кровь пациента. Такое исследование позволяет дифференцировать на МРТ-снимках доброкачественную опухоль от злокачественной, оценить ее размеры, связь с другими тканями, полностью оценить объем предстоящего оперативного вмешательства.
При локализации злокачественных новообразований около важных жизненных структур может быть принято решение о консервативном лечении. Благодаря магнитно-резонансному сканированию возможно наблюдать за опухолью в динамике, отслеживать влияние терапевтического воздействия на пораженные ткани.
Диагностика рака при КТ также может показать развитие и стадии онкологического процесса, оценить прогресс лечения, но дополнительное воздействие рентгеновского излучения может оказаться дополнительной нагрузкой на изнуренный болезнью организм. Поэтому при отсутствии противопоказаний предпочтение отдают МРТ обследованию.
Может ли МРТ не показать опухоль?
При возникновении злокачественного новообразования возможность успешного лечения напрямую зависит от того, насколько быстро оно замечено. Магнитно-резонансная томография на сегодняшний день – самый совершенный инструмент аппаратной онкодиагностики. Томограф помогает разглядеть в любой области организма патологические элементы размером в несколько миллиметров. При такой величине ещё не начинается формирование метастазов, атипичные клетки не успевают отсеяться в лимфоузлы и соседние органы. На этой стадии рак можно победить консервативным лечением. Поэтому вполне оправдано направление на МР-сканирование при подозрении на злокачественную опухоль.
Чтобы можно было лучше увидеть опухоль на МРТ применяется контрастирование. Это несколько усложняет процесс и требования к подготовке к нему, зато на выходе имеется более чёткая информация о состоянии исследуемого органа. В случае бесконтрастной диагностики чаще всего можно обнаружить опухолевые образования больших размеров.
Магнитно-резонансная томография может не выявить опухоль в случае, если исследование проводилось на аппарате с низкой индукцией магнитного поля. Качества снимков, выполненных на таком оборудовании, может оказаться недостаточным для распознавания патологического процесса. Вот почему при подозрении на опухолевые заболевания пациентам категорически рекомендуется проходить обследование на современных высокопольных аппаратах.
Видны ли метастазы на МРТ?
Метастазы хорошо видны на снимках при любой локализации, но для повышения достоверности результатов пациенту вводят контрастное вещество.
Это необходимо делать в случае развития метастаз:
- в забрюшинном пространстве и органов брюшной полости, малого таза;
- в центральной нервной системе — отделах головного и спинного мозга;
- при подозрении на метастазы в мягких тканях, внутриорганные метастазы.
При локализации очагов в костной системе усиление контрастом используется редко.
Как выглядит рак на МРТ снимке?
 Вне зависимости от локализации злокачественного процесса, опухоль на снимках выглядит как затемненный очаг среди здоровых тканей. Границы его могут быть как четкими, так и нечеткими — это зависит от характера и стадии процесса.
Вне зависимости от локализации злокачественного процесса, опухоль на снимках выглядит как затемненный очаг среди здоровых тканей. Границы его могут быть как четкими, так и нечеткими — это зависит от характера и стадии процесса.
Внутри злокачественные опухоли содержат кальцинаты, в них часто образуются участки некроза — на фотографии ясно видна «рыхлость» среза. Раковые опухоли разрушают окружающие ткани — на снимке можно увидеть ореол вокруг темного пятна.
Онкологический процесс в сосудистых образованиях можно визуализировать только при использовании контрастного вещества. Злокачественные новообразования накапливают больше контрастного вещества, поскольку характеризуются густой сетью сосудов и интенсивным кровоснабжением.
Однако и при МРТ не всегда можно получить максимально-достоверный результат по поводу злокачественного процесса. В этом случае пациенту рекомендуют дополнительно сделать биопсию.
С помощью магнито-резонансной томографии можно получить достаточно достоверный результат, но диагноз на основании расшифровки результатов не ставится. Поэтому не стоит начинать самолечение по предварительным данным после скрининга. Окончательный диагноз ставит лечащий врач, учитывая жалобы больного и результаты всех обследований.
Как выглядит опухоль на МРТ-фото
МР томограмма – не просто фото, на котором видно, как выглядит опухоль. Специалисту она говорит о величине, конфигурации новообразования, его взаиморасположении с элементами нервной и сосудистой системы, соседними органами. На экране компьютера создаётся реконструкция поражённого раком участка организма. Бывает, что удалять опухоль очень опасно, тогда МРТ становится щадящим инструментом консервативного контроля состояния. Проводятся МРТ исследования и для отслеживания реакции на лучевую и химиотерапию, хирургическое вмешательство.
Источник
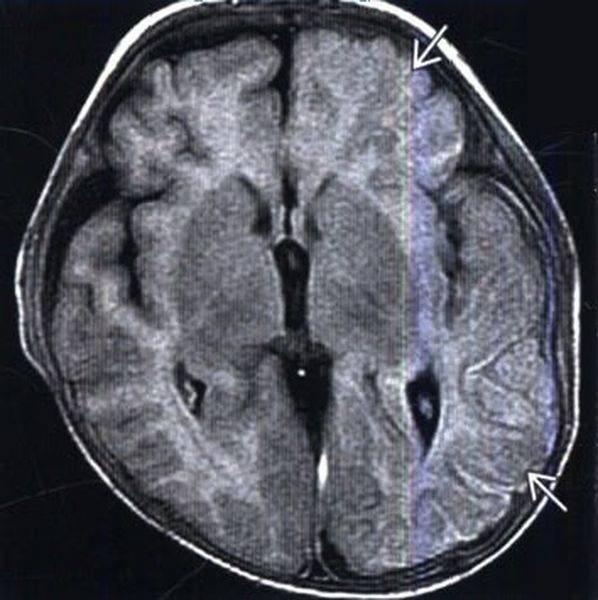 Посттравматический отек левого полушария (показано стрелками)
Посттравматический отек левого полушария (показано стрелками)Отек головного мозга – увеличение объема тканей, возникающее вследствие постепенного или стремительного накопления жидкости, изменения структур и функциональности клеток. Патологическое явление является осложнением ряда заболеваний. Опасность отека и набухания состоит в том, что церебральные структуры оказываются сдавлены черепом и отрогами твердой оболочки и не могут дальше увеличиваться в объеме. Данный процесс влечет за собой повышение внутричерепного давления, компрессию сосудов, дислокацию мозговых структур, нарушение кровообращения и, в конечном счете, — гибель нейронов. Смерть от отека мозга, если его не лечить, неизбежна. Вовремя проведенное обследование может помочь сохранить жизнь человеку.
Магнитно-резонансную и компьютерную томографии широко используют для быстрой диагностики патологических явлений в головном мозге. Обсуждаемый процесс может иметь несколько форм: цитотоксическую или вазогенную. Каждый вид отличается причинами возникновения и локализацией патологических проявлений.
Наиболее распространён вазогенный тип отека. Характеризуется переходом жидкости из сосудов в белое мозговое вещество. Патология возникает в связи с нарушением работы гематоэнцефалического барьера. Данный тип отека наблюдают вокруг опухолей (первичных и вторичных), при абсцессах, инсультах, ушибах, кровоизлияниях и пр. Подвидом рассматриваемого осложнения считают интерстициальный вариант, который возникает вследствие повышения давления в желудочках, что приводит к пропотеванию спинномозговой жидкости в интерстициальное пространство. Данный процесс вызывает отек белого вещества. Частыми причинами являются обструктивная гидроцефалия и менингит.
Цитотоксический (клеточный) вид патологии возникает в сером веществе, может быть вызван интоксикацией, отравлением, ишемическим инсультом, вирусными инфекциями, травмами головы и т.д. При данной форме отека на первом этапе не происходит повреждение гематоэнцефалического барьера, наблюдают изменение ионного баланса на поверхности клеточных мембран.
Любой из описанных вариантов патологии крайне непродолжительное время может существовать изолированно. Принято рассматривать отек и набухание головного мозга как звенья одного патологического процесса.
С помощью МРТ возможно определить преобладающий вариант, что обуславливает выбор схемы лечения.
Признаки отека головного мозга
 Снимки головного мозга на МРТ
Снимки головного мозга на МРТ
Основной симптом, по которому врачи безошибочно определяют отек и набухание головного мозга – расстройство сознания от легких до тяжелых форм.
На начальной стадии при медленном прогрессировании церебрального процесса больной остается в адекватен и ориентирован в себе, месте и времени, могут развиваться судороги. Выделяют следующие общие признаки, указывающие на возможный отек мозга:
- сильная головная боль, сопровождающаяся тошнотой и рвотой, особенно в утренние часы;
- нарушение двигательных функций, чувствительности, зрения, координации и т.п.;
- головокружение;
- галлюцинации;
- судороги;
- психомоторное возбуждение;
- нарушение вегетативных и витальных функций;
- панические атаки и пр.
Последние признаки из списка – самые опасные, так как сопровождают компрессию ствола мозга и требуют неотложной медицинской помощи.
При возникновении любых вышеуказанных настораживающих проявлений при неврологических заболеваниях или опухолях мозга и головы следует незамедлительно обращаться к врачу. После диагностики менингеальных симптомов и признаков нарушения сознания будет назначено соответствующее обследование на МРТ или КТ.
Отек мозга на МРТ, как выглядит?
Вазогенный отек чаще всего возникает вследствие опухоли, абсцесса. На МРТ регистрируют гиперинтенсивный сигнал в режиме Т2 взвешенного изображения и FLAIR (с подавлением сигнала свободной воды) без ограничения диффузии.
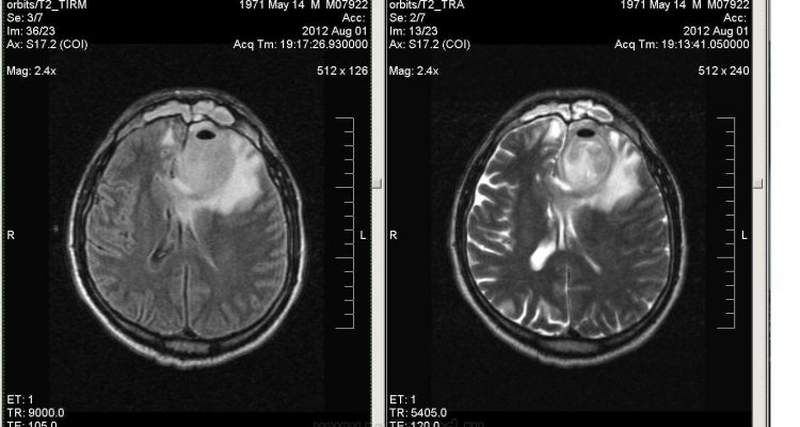 Вазогенный отек из-за абсцесса на МРТ
Вазогенный отек из-за абсцесса на МРТ
Цитотоксический отек головного мозга на МРТ невозможно определить на Т2 или Т1 режимах, так как процесс происходит из-за перераспределения воды из вне- во внутриклеточное пространство. Патологию определяют за счет соизмеримого снижения диффузии, которая проявляется повышенным сигналом на ДВИ (диффузионно-взвешенных изображениях). Данные изменения возможно выявить в подострой фазе (до 14 дней).
Пройти МРТ головы по назначению врача Вы можете в медицинском центре «Магнит». Для выбора оптимальной даты, времени процедуры заполните обратную форму связи на сайте, после чего наши консультанты свяжутся с Вами.
Источник
Уверенная дифференциация низкокачественных опухолей головного мозга
Статья является рекламно-просветительской, переведена без изменений с официального сайта Philips
Ссылка на первоисточник
Amide Proton Transfer (APT) — это новый метод МРТ, который генерирует контраст изображения, отличный от обычного МРТ. Весоизмерительная визуализация APT представляет собой метод MRI с переносом насыщения химическим обменом (CEST), и его сигнал основан на концентрации эндогенных белков и пептидов, типично присутствующих в высокосортной ткани опухоли головного мозга. Таким образом, взвешенное изображение APT не требует применения какого-либо контрастного агента.
Врачи клинической больницы Phoenix (PCH) изучали ценность APT в клинической практике, чтобы исследовать, в какой степени взвешенную визуализацию APT можно было бы использовать при диагностике и послетерапии изображений детей с опухолями головного мозга. Их результаты показывают, что взвешенная визуализация APT может обеспечить более высокую уверенность в определении как уровня опухоли, так и степени остаточной послеоперационной опухоли. Многие пути лечения основаны на точном определении агрессивности или «степени» опухолей для оптимального выбора среди вариантов лечения, чтобы предложить наилучший выбор для пациентов.
«Некоторые высокосортные опухоли не демонстрируют усиления гадолиния, а некоторые низкосортные опухоли иногда усиливают»
Поиск уверенной диагностик опухолей головного мозга
МРТ широко используется для визуализации первичных опухолей головного мозга и вторичных повреждений у пациентов с онкологией. Его превосходный контраст мягкой ткани и функциональная визуализация предоставляют радиологам информацию о местонахождении, размере, морфологии, составе и физиологии повреждений, чтобы помочь им в диагностике и постановке. Тем не менее, бывают случаи, когда рентгенологи хотели бы иметь дополнительные возможности для их диагностики, например, с более высокой степенью достоверности выделения высокосортных и низкосортных опухолей и, в конечном счете, для проведения многочисленных последующих МРТ-тестов без контрастного введения у детей после мозга резекция опухоли.
Только в Соединенных Штатах ожидается, что в 2017 году будет диагностировано около 80 000 новых случаев первичной опухоли головного мозга, включая более 26 000 первичных злокачественных опухолей головного мозга. [1] Глиомы составляют 75% всех злокачественных опухолей, а 55% из них — глиобластома с 12 930 случаями, предсказанными на 2017 год. [1,2]
Учитывая эту заболеваемость и влияние правильного диагноза и соответствующих путей лечения, онкологов и радиологов weclome инновационные инструменты для поддержки их текущих средств и стратегий. Одним из них может быть добавление взвешенного изображения APT к экзамену MRI. Контраст APT коррелирует с наличием белков и пептидов, которые могут быть связаны с пролиферацией клеток. Поскольку пролиферация клеток является особенностью опухолей, цветные карты APT могут быть полезны при идентификации и количественной оценке опухолевой ткани [3,4].
APT отражает концентрацию эндогенных белков в опухоли головного мозга
В методах взвешенного изображения APT и других методах CEST сигнал MRI генерируется механизмом, отличным от механизма основной МРТ. Эти методы CEST основаны на химическом обмене атомами водорода. Сигнал амидных протонов пептидных связей в белках слишком низок, чтобы его можно было измерить при нормальной МРТ. Обмен водородом (протоном) между белковыми амидными группами и окружающей водой позволяет по-разному измерять эти амидные протоны.
В APT для ослабления его MR-сигнала используется узкий RF-импульс (импульс насыщения) на частоте амидного водорода. Поскольку амидная группа и вода непрерывно обмениваются атомами водорода, количество насыщенных протонов будет накапливаться в воде, так что измеренный сигнал воды станет ниже. Изменение сигнала MRI воды обеспечивает косвенный способ измерения присутствия амида. Изображения APT обычно представлены в виде цветовых карт, созданных с использованием вычисления асимметрии, так что присутствие APT отображается как позитивный цветной сигнал.

Рис.1
Исследования показали, что сигнал APT коррелирует с концентрацией белка, который связан с пролиферацией клеток. Концентрация этого белка и, таким образом, сила сигнала APT реагирует на уровень злокачественных опухолей [5-7]. Контраст APT может потенциально выделять опухоли, которые иначе не наблюдались бы.
Оценка опухоли может повлиять на принятие важных решений
Выбор путей лечения часто сильно зависит от степени опухоли. Общие варианты лечения высокосортных опухолей включают хирургическую резекцию опухоли с последующей дополнительной терапией, такой как радиация и химиотерапия. Быстрые и решительные действия желательны в этих случаях, так как средняя выживаемость глиобластомы, например, составляет от 12,6 до 14,6 месяцев, хотя сообщалось о более высоких показателях [8,9]
Учитывая более низкие темпы роста опухоли низкосортных опухолей, для этих случаев существует ряд возможных вариантов лечения. Выбор наиболее подходящего лечения основан на балансе терапевтических преимуществ и побочных эффектов. Иногда визуализация наблюдения может играть определенную роль, в то время как выбор окончательной терапии рассматривается. [10]
МР-томография часто используется радиологами и врачами для оценки степени опухолей головного мозга, но иногда существует неопределенность. [9,11] Дифференциация между низкосортными и полноценными опухолями не является прямой, даже для высококвалифицированного радиолога. Усиление гадолиния не всегда специфично для опухолевого сорта, так как некоторые высокосортные опухоли не демонстрируют усиления гадолиния, а некоторые низкосортные опухоли иногда усиливаются (например, DNET). Усиление гадолиния также происходит в любой области нарушения гематоэнцефалического барьера, например, связанного с лечением травмы [12].
APT для классификации опухолей головного мозга с помощью МРТ
Хотя золотой стандарт для классификации глиомы является гистопатологией после биопсии, МРТ часто используется для мониторинга пациентов с глиомой, а APT может быть ценным дополнением к МРТ-обследованию у этих пациентов.
Было отмечено, что уровень опухоли и APT-сигнал обычно положительно коррелируют: высокосортные опухоли имеют тенденцию демонстрировать высокий контраст APT. [12-15] Изображения APT можно увидеть, чтобы визуализировать опухоль с большим вниманием, чем постконтрастные изображения, в результате чего сканирование, которое может быть легче интерпретировать. Научные исследования, сравнивающие уровни опухолей с сигналом APT во взрослой глиоме, свидетельствуют о том, что APT может поддерживать классификацию опухолей, отделяя высокосортные от низкосортных, даже когда традиционная МРТ неубедительна [5,13,14].
APT-визуализация полноценной опухоли
Оценка опухоли у 1-летнего ребенка с медуллобластомой. Этот агрессивный тип опухоли очень твердый и однородный. Высокий APT-сигнал соответствует постконтрастному изображению этой полноценной опухоли.

Рис.2
APT может быть мощным дополнением к визуализации опухолей на МРТ
Д-р Джеффри Миллер, педиатрический радиолог из PCH, также заметил связь между контрастом APT и опухолевыми классами в исследованиях, проведенных в его больнице. «В нескольких случаях мы наблюдали высокий APT-сигнал в высокосортных опухолях и умеренно увеличенный APT-сигнал в случаях с промежуточными и низкосортными опухолями, которые характеризуются высоким изменением сигнала на T2 и FLAIR, и без усиления контраста».
Он указывает на потенциальные клинические последствия этого наблюдения. «Когда мы сталкиваемся с пациентами, у которых диагноз несколько неоднозначен, нам часто приходится делать выбор и оценивать суждения, что может означать либо просто наблюдение за опухолью или поражением, с тем риском, что это может измениться, когда мы ошибались и может быть потеряно время. Или нам нужно идти в инвазивные ситуации, когда мы должны проводить биопсию ».
«Было бы очень эффектно и ценно иметь последовательность, подобную взвешиванию изображений APT, что могло бы помочь нам в принятии этих решений с большей уверенностью. Это было бы значимо для отдельных пациентов и проявлять некоторую двусмысленность в том, что мы делаем ».
«Однако для достижения этой высокой цели нам потребуется больше исследований, использование последовательности в более широком населении и более полное понимание ситуаций и условий, при которых APT имеет максимальную ценность».
«Было бы неплохо иметь такую последовательность, как APT, которая могла бы помочь нам в принятии этих решений с большей уверенностью»
APT — даёт важную информацию по МРТ после резекции опухоли
МРТ может быть выполнена после резекции опухоли, для поиска остаточной опухоли или роста опухоли. Также здесь может быть диагностирован различный контрастный механизм APT. Доктор Миллер вспоминает конкретный случай.
«После очень хорошей резекции мы увидели небольшие изменения на постконтрастных T1-взвешенных и взвешенных по T2 изображениях, которые выглядели как постхирургическое немного жидкости. Интересно, однако, что мы видели фокальную область сигнала APT, прямо в центре этой аномалии. Как мы обычно делаем, когда немного не уверены, мы следили за ним и, к сожалению, обнаружили опухоль в этом регионе », — говорит доктор Миллер. «Такие случаи мотивируют меня и других, кто заботится об этом населении, исследовать, как этот метод APT можно широко использовать в этой популяции и помочь нам в предоставлении высокоценной диагностической информации».
Врач больницы также видел случай, когда APT имела отрицательную прогностическую ценность. После резекции опухоли высокого ранга они увидели подобное небольшое изменение в изображениях этого пациента. Однако в этом случае сигнал APT был довольно низким. При недавнем повторном сканировании этого пациента рецидива не наблюдалось.
APT-изображение опухоли низкой степени злокачественности
Глиома низкой степени злокачественностич у 5-летнего пациента с нейрофиброматозом 1. Это низкосортное поражение не усиливается на постконтрастных изображениях, но показывает промежуточный сигнал APT. Стабильность поражения с течением времени подтверждает, что это низкосортная патология.

Рис.3
Последующее наблюдение

Рис.4
APT на МРТ в педиатрической нейроонкологии
Врач-радиолог Джон Карран, доктор медицинских наук, был основным исследователем в изучении взвешенного изображения APT в Детской больнице Феникса. «В это время APT был добавлен примерно к 70 исследованиям МРТ у детей с опухолью головного мозга, и мы увидели некоторые обнадеживающие ранние результаты», — говорит Джон Карран, доктор медицинских наук, радиолог в Детской больнице Феникса (PCH). «Нам потребуются более крупные исследования с большим количеством пациентов, чтобы точно утверждать корреляцию. Тем не менее, не нужно быть 100% -ной корреляцией, чтобы быть полезной при повторных исследованиях опухоли головного мозга, потому что мы также смотрим на FLAIR и на другие изображения. Цель состоит в том, чтобы поймать что-то, пока оно не станет слишком большим, если ему нужна новая операция или новая терапия, и если мы увидим что-то подозрительное — в отличие от определенного повторения — часто это не вопрос немедленных действий, а для последующего наблюдения ».
Специалисты PCH, участвующие в исследовании, в целом выражают осторожный оптимизм, что взвешенная визуализация APT может когда-нибудь значительно снизить потребность в контрастной инъекции у педиатрических пациентов. «Если мы сможем принести APT вперед в качестве разумной замены, особенно в наших последующих случаях опухолей головного мозга, которые будут иметь большую пользу», — говорит доктор Курран. «Использование контрастного агента жестко контролируется в нашей общей нейрорадиологической визуализации, а контрастный агент вводится только тогда, когда это действительно необходимо. Итак, наше исследование фокусируется на определении того, можем ли мы в будущем использовать APT для уменьшения использования контрастных агентов ».
«APT был добавлен примерно к 70 МРТ-исследованиям детей с опухолью головного мозга, и мы увидели некоторые обнадеживающие ранние результаты»
Перспективные результаты с APT
Д-р Курран сравнивал взвешенную визуализацию APT с постконтрастной МРТ у детей с историей опухолей головного мозга. «Во многих случаях мы видели, что APT является положительным, когда постконтрастная T1-взвешенная визуализация положительна. Итак, мы пытались оценить, достаточно ли это отношение, чтобы использовать APT вместо того, чтобы при определенных обстоятельствах давать контрастный агент для детей ». В исследовании используется исследовательское программное обеспечение APT, разработанное Philips в рамках исследовательского сотрудничества.
«МРТ опухоли головного мозга обычно включает в себя постконтрастное изображение. Таким образом, в нашем молодом пациенте наши проблемы связаны с необходимостью введения контрастного вещества на основе гадолиния при последующем сканировании у детей после резекции опухоли головного мозга. Исследование, опубликованное моим коллегой д-ром Миллером, показало, что если опухоль ресецируется у маленького ребенка, к тому времени, когда ребенок находится в молодом возрасте, в мозге было внесено значительное количество гадолиния [16]. APT не требует никакого контрастного агента. Таким образом, если мы сможем принести APT вперед в качестве разумной замены, особенно в наших последующих случаях опухолей головного мозга, это принесет большую пользу ».
APT в послеоперационной оценке

Рис.5
Большое метастатическое поражение головного мозга.
Этот 10-летний пациент подвергся резекции опухоли саркомы Юинга 7 лет назад, но было обнаружено, что теперь у нее большое метастатическое поражение в головном мозге. Это поражение показывает явно увеличенный сигнал APT.

Рис.6
МРТ с последующей резекцией APT.
Сразу же после резекции МРТ снова была выполнена. T2-взвешенные и постконтрастные T1-взвешенные изображения довольно неубедительны для выделения остаточной опухолевой ткани после послеоперационных изменений тканей. На изображении APT еще наблюдается высокий сигнал, который предполагает наличие остаточной опухолевой ткани.

Рис.7
Последующее наблюдение с течением времени.
В более поздних последующих исследованиях послеконтрастные взвешенные по T1 изображения предполагают повторный рост опухоли. Таким образом, было бы интересно изучить предсказательную ценность APT в большой группе пациентов.
Ожидания потенциала APT
По словам доктора Куррана, основной исследовательский центр APT в PCH до сих пор занимался исследованием его возможностей визуализации опухолей головного мозга и его потенциала для снижения потребности в контрасте. «Мы надеемся, что APT в будущем может помочь нам в дальнейшем охарактеризовать опухоли с помощью МРТ, но больше исследований нужно будет сделать, прежде чем мы полностью узнаем, что возможно и эффективно. Изучая специфические аспекты опухолей, которые являются положительными APT, мы надеемся сопоставить сигнал APT с более точными гистологическими или опухолевыми маркерами ».
« Мы с нетерпением ждем, что в будущем мы проведем тест, чтобы помочь нам в направлении терапии, например, выборе химиотерапии агентов, плюс или минус излучение и т. д. Возможно, APT может в будущем иметь потенциал, чтобы помочь нам там каким-то образом », — говорит д-р Курран. «Возможности кажутся очень широкими».
Д-р Миллер заканчивает, подводя итог: «У нас был действительно хороший опыт использования метода APT в клинической ситуации. Мы многому научились в этом процессе и видим много возможностей для этого в будущем ».
Список литературы:
American Brain Tumor Association, Brain Tumor Statistics.
Central Brain Tumor Registry of the United States, 2016 CBTRUS Fact Sheet.
Togao O, Hiwatashi A, Keupp J, Yamashita K, Kikuchi K, Yoshiura T, Yoneyama M, Kruiskamp MJ, Sagiyama K, Takahashi M, Honda H. Amide Proton Transfer Imaging of Diffuse Gliomas: Effect of Saturation Pulse Length in Parallel Transmission-Based Technique. PLOS ONE 2016; doi: 10.1371/journal.pone.0155925.
Togao O, Keupp J, Hiwatashi A, Yamashita K, Kikuchi K, Yoneyama M, Honda H. Amide Proton Transfer Imaging of Brain Tumors Using a Self-Corrected 3D Fast Spin-Echo Dixon Method: Comparison with Separate B0 correction Magn Res Med 2016 early view; doi: 10.1002/mrm.26322.
Togao O, Yoshiura T, Keupp J, Hiwatashi A, Yamashita K, Kikuchi K, Suzuki, YS, Iwak, T, Hata N, Mizoguchi M, Yoshimoto K, Sagiyama K, Takahashi M, Honda H Amide proton transfer imaging of adult diffuse gliomas: correlation with histopathological grades. Neuro-Oncology 2014; 16(3), 441–448.
Jiang S, Eberhart CG, Zhang Y, Heo HY, Wen Z, Blair L, Qin H, Lim M, Quinones- Hinojosa A6, Weingart JD, Barker PB, Pomper MG, Laterra J, van Zijl PCM, Blakeley JO, Zhou J. Amide proton transfer-weighted magnetic resonance image-guided stereotactic biopsy in patients with newly diagnosed gliomas. Eur J Cancer 201783:9-18; doi: 10.1016/j.ejca.2017.06.009.
Zhou, J. (2011). Amide Proton Transfer Imaging of the Human Brain. Magnetic Resonance Neuroimaging. Methods in Molecular Biology (Clifton, N.J.), 711, 227–237.
American Brain Tumor Association, Brain Tumor Information, Types of Tumors, Glioblastoma (GBM)
Lobera, A, Coobs, B, Naul, LG, Zee, CS. Imaging in Glioblastoma Multiforme. Medscape.
Paleologos, N. Low Grade Glioma: Update in Treatment and Care. ABTA Patient and Family Conference, 2014.
Upadhyay, N, Waldman, A D, Conventional MRI evaluation of gliomas. The British Journal of Radiology 2011; 84: S107–S111.
Wen, Z, Hu, S, Huang, F, Wang, X, Guo, L, Quan, X, Wang, S, Zhou, J, MR Imaging of High-Grade Brain Tumors Using Endogenous Protein and Peptide- Based Contrast. NeuroImage 20110; 51(2), 616–622.
Park KJ, Kim HS, Park JE et al. Added value of amide proton transfer imaging to conventional and perfusion MR imaging for evaluating the treatment response of newly diagnosed glioblastoma. Eur Radiol 2016, 26: 4390; doi: 10.1007/s00330- 016-4261-2.
Park JE, Kim HS, Park KJ, Kim SJ, Kim JH, Smith SA. Pre- and Posttreatment Glioma: Comparison of Amide Proton Transfer Imaging with MR Spectroscopy for Biomarkers of Tumor Proliferation. Radiology 2016, 278 :514; doi: 10.1148/ radiol.2015142979.
Wang X, Yu H, Jiang S, Wang Y, Wang Y, Zhang G, Jiang C, Song G, Zhang Y, Heo H-Y, Zhou J, Wen Z. Qualitative and quantitative analysis of amide proton transferweighted MR images at 3 Tesla of adult gliomas. Abstract #1105, ISMRM 2017.
Miller JH, Hu HH, Pokorney A, Cornejo P, Towbin R. MRI Brain Signal Intensity Changes of a Child During the Course of 35 Gadolinium Contrast Examinations. Pediatrics 2015;136;e1637.
Источник
