Сравнение врожденного и адаптивного иммунитета

 Добрый день! Продолжаем разговор об уникальности нашего организма. Его способность биологических процессов и механизмов, способна надёжно защищаться от болезнетворных бактерий. А две главные подсистемы, врождённый и приобретённый иммунитет в своем симбиозе способны находить вредные токсины, микробы и погибшие клетки и успешно удалять их, стерилизуя наш организм.
Добрый день! Продолжаем разговор об уникальности нашего организма. Его способность биологических процессов и механизмов, способна надёжно защищаться от болезнетворных бактерий. А две главные подсистемы, врождённый и приобретённый иммунитет в своем симбиозе способны находить вредные токсины, микробы и погибшие клетки и успешно удалять их, стерилизуя наш организм.
Механизмы врождённого иммунитета

Представьте себе огромный сложный комплекс, способный к самообучению, саморегулированию, самовоспроизведению. Это наша система защиты. Она с самого начала жизни служит нам постоянно, не прекращая своей работы. Обеспечивая нам индивидуальную биологическую программу, которая имеет задачу отторгать всё чужеродное, в любом виде агрессии и концентрации.
Если говорить о врожденном иммунитете на уровне эволюции, то он довольно древний и сконцентрирован на физиологии человека, на факторах и барьерах внешней стороны. Так наш кожный покров, секреторные функционалы в виде слюны, мочи и других жидких выделений реагируют на атаки вирусов.
В этот список можно включить кашель, чихание, рвоту, диарею, повышенную температуру, гормональный фон. Данные проявления, ни что иное, как реакция нашего организма на «чужих». Иммунные клетки еще не поняв и не распознав чужеродность вторжения, начинают активно реагировать и уничтожать всех, кто посягнул на «родную территорию». Клетки первыми вступают в бой и начинают уничтожать различные токсины, грибки, отравляющие вещества и вирусы.
Свойства врожденного иммунитета очень сильны, при столкновении с инфекционными паразитами реакция максимальна, подключены все звенья и клеточные и гуморальные. Он обнаруживается почти у всех биологических форм жизни, единственный его недостаток, он не имеет иммунной памяти.
Любая инфекция расценивается как однозначное и одностороннее зло. Но стоит сказать, что именно инфекционное поражение способно оказать иммунитету полезное действие, как бы странно это не звучало.
Именно в такие моменты происходит полная мобилизация всех защитных сил организма и начинается распознавание агрессора. Это служит своеобразной тренировкой и организм со временем моментально способен распознавать происхождение и более опасных болезнетворных микробов и палочек.
Врожденный иммунитет это неспецифичная система защиты, при первой реакции в виде воспаления, появляются симптомы в виде отеков, покраснений. Это говорит о моментальном притоке крови к пораженному месту, начинается вовлечение кровяных телец в процесс, происходящий в тканях.
Не будем говорить о сложных внутренних реакциях, в которых участвуют лейкоциты. Довольно сказать, что краснота от укуса насекомого или ожог, это как раз свидетельство работы врождённого защитного фона.
Факторы двух подсистем
Факторы врождённого и приобретённого иммунитета очень взаимосвязаны между собой. У них общие одноклеточные организмы, которые представлены в крови белыми тельцами (лейкоцитами). Фагоциты, и есть воплощение врожденной защиты. К ней относятся и эозинофилы, тучные клетки, и естественные киллеры.
Фагоциты буквально «глотают» паразитирующее в организме тело в виде раковых клеток – убийц или иных паразитов и успешно их переваривают. Данные клетки не только осуществляют неспецифический врожденный иммунитет, они активируют механизмы действия приобретённых защитных способов.
Клетки врожденного иммунитета, с названием дендритные, призваны к соприкосновению со средой извне, они находятся в кожных покровах, носовой полости, легочной, а также желудке и кишечнике. У них множество отростков, но с нервами их путать нельзя.
Этот вид клеток является связкой между врожденными и приобретенными способами борьбы. Они действуют посредством антигена Т – клеток, он базовый тип приобретённого иммунитета.
Многие молодые и неопытные матери беспокоятся о ранних заболеваниях детей, в частности, о ветряной оспе. Можно ли оградить чадо от инфекционной болезни, и какие могут быть для этого гарантии?
Врожденный иммунитет к ветрянке может быть только у новорождённых детей. Чтобы в дальнейшем не спровоцировать болезнь, необходимо поддерживать неокрепший организм грудным вскармливанием.
Тот запас иммунитета, который малыш получил от матери при рождении недостаточен. При длительном и постоянном грудном вскармливании, ребенок получает необходимое количество антител, а значит, может быть более защищён от вируса.
Специалисты утверждают, что даже если создать ребенку благоприятные условия, врожденная защита может быть только временной.
Взрослые люди гораздо тяжелее переносят ветрянку, и картина заболевания носит весьма неприятный характер. Если человек не болел данным заболеванием в детском возрасте, у него есть все основания бояться заражения таким недугом, как опоясывающий лишай. Это высыпания на кожных покровах в области межреберья в сопровождении высокой температуры.
Приобретённый иммунитет

Это тип, появившийся вследствие эволюционного развития. Приобретённый иммунитет создавшийся в процессе жизни более эффективен, имеет память, которая способна идентифицировать по уникальности антигенов чужеродный микроб.
Внутри нас, если говорить понятным языком, осуществляется некая «презентация» «чужаков», после которой происходят реагирования выборочного характера, и вступают в «сражение» только предназначенные для убийства данного паразита клетки. Если микроб инфицирован повторно, клетки помня о нем, активируются для его моментального уничтожения.
Рецепторы клеток узнают возбудителей приобретенного типа защиты на клеточном уровне, рядом с клетками, в тканевых структурах и плазме крови. Главными, при данном виде защиты, выступают В – клетки и Т – клетки. Они рождаются в стволовых клеточных «производствах» костного мозга, тимуса, и являются основой защитных свойств.
Материнская передача иммунитета своему ребёнку, является примером приобретенного пассивного иммунитета. Это происходит во время вынашивания плода, а также в период лактации. В утробе это происходит на третьем месяце беременности через плаценту. Пока новорождённый не в состоянии синтезировать собственные антитела, поддержка его осуществляется при помощи материнского наследства.
Интересно, что приобретенный пассивный иммунитет может быть передан от человека к человеку при помощи передачи активированных Т – лимфоцитов. Это довольно редкое явление, так как люди должны иметь гистосовместимость, то есть соответствие. Но таких доноров найти можно крайне редко. Это может произойти только путем пересадки стволовых клеток костного мозга.
Активный иммунитет способен проявиться после применения вакцинации или в случае перенесенного заболевания. В случае, если при недуге успешно справляются функции врожденного иммунитета, приобретенный спокойно ждет своего часа. Обычно командой к наступлению, является высокая температура, слабость.
Вспомните, во время простуды, когда на градуснике ртуть замерла на отметке 37,5, мы, как правило, выжидаем, и даем организму время, самостоятельно справиться с болезнью. Но стоит только ртутному столбику подняться выше, здесь уже следует принимать меры. Помощь иммунитету может быть применение народных средств или горячего питья с лимоном.
Если делать сравнение между этими видами подсистем, то она должна быть наполнена четким содержанием. Данная таблица наглядно показывает отличия.
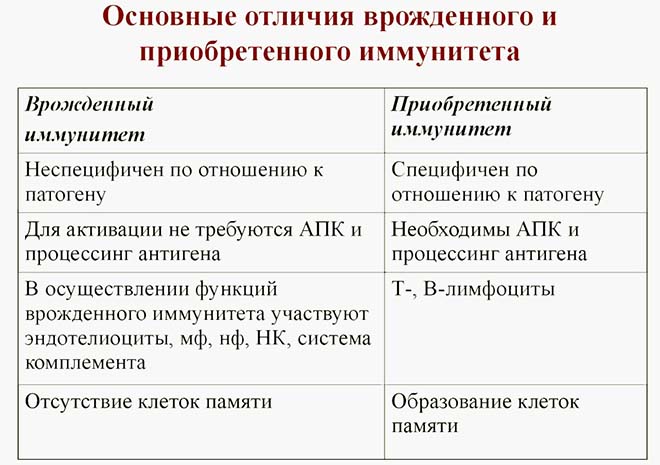
Сравнительная характеристика врожденного и адаптивного иммунитета
Врожденный иммунитет
- Реакция неспецифического свойства.
- Максимальная и моментальная реакция при столкновении.
- Работают клеточные и гуморальные звенья.
- Не имеет иммунологической памяти.
- Есть у всех биологических видов.
Приобретённый иммунитет
- Реакция специфического свойства и привязана к конкретному антигену.
- Между атакой инфекции и ответной реакцией есть латентный период.
- Наличие гуморальных и клеточных звеньев.
- Имеет память на определенные виды антигенов.
- Есть только у немногих существ.
Только при полном комплекте, имея врожденные и приобретенные способы борьбы с инфекционными вирусами, человек может справиться с любой болезнью. Для этого нужно помнить о самом главном – любить себя и свой уникальный организм, вести активный и здоровый образ жизни и иметь позитивную жизненную позицию!
Видео по теме:
Источник
Глава 1. ОСНОВНЫЕ ПОЛОЖЕНИЯ
Иммунитет — особое биологическое свойство многоклеточных организмов, направленное на защиту от генетически чужеродных факторов: микроорганизмов (бактерий, вирусов, простейших, грибов), инородных молекул и др. Иммунитет также обеспечивает невосприимчивость организма к инфекции при повторной встрече с патогеном. В медицинском смысле этот термин употребляли ещё до нашей эры в значениях: неприкосновенный, чистый, не затронутый заболеванием, невредимый, находящийся под хорошей защитой, устойчивый к заразной болезни.
Совокупность органных, тканевых, клеточных и молекулярных компонентов, функцией которых является осуществление иммунной защиты, называется иммунной системой. Иммунология — наука о строении и функциях иммунной системы как в норме, так и при различных патологических состояниях, в том числе и при нарушениях самой иммунной системы — иммунопатологиях.
Иммунную защиту обеспечивают два механизма: врождённый и адаптивный.
Врождённый иммунитет является присущей каждому организму с рождения, генетически закреплённой способностью противостоять инфекции. Это передовая линия обороны организма против патогенов, пытающихся проникнуть или уже проникших в покровные ткани или внутреннюю среду. Врождённый иммунитет срабатывает мгновенно или в течение первых нескольких часов после контакта с патогеном (возбудители, выделяемые ими токсины и другие чужеродные молекулы). Он включает четыре основных уровня защиты: анатомический, физиологический, фагоцитарный и воспалительный — покровные ткани, фагоциты, микробоцидные гуморальные вещества (протеазы, сильные окислители и свободные радикалы, продуцируемые фагоцитами, эндогенные противомикробные пептиды и др.), сосудистые реакции. Первичные рецепторы врождённого иммунитета — это молекулы многоклеточных, позволяющие «считывать» эволюционную память — информацию о том, чем отличаются микроорганизмы от собственных клеток.
Эти рецепторы способны распознавать консервативные молекулярные структуры — РАМР (Pathogen-Associated Molecular Patterns), характерные для групп сходных микроорганизмов. В настоящее время постоянно открывают новые патогенраспознающие рецепторы врождённого иммунитета. К ним относят мембраносвязанные паттернраспознающие рецепторы (Pattern Recognition Receptors, PRR), а также растворимые рецепторы — ряд белков сыворотки крови: C-реактивный белок (СРБ), маннозосвязывающий лектин (MBL — Mannose-Binding Lectin), компоненты комплемента.
Собственные возможности клеток врождённого иммунитета санировать организм от проникшего патогена часто недостаточны. Множество патогенов приспособилось выживать в присутствии факторов врождённой резистентности к инфекциям. Именно поэтому в процессе эволюции, начиная с челюстных рыб, к врождённому иммунитету добавился адаптивный иммунитет — специфический. Материальные носители адаптивного иммунитета — лимфоциты. Уникальное и отличительное свойство лимфоцитов как множества клеток — способность распознавать почти неограниченное (1018) разнообразие молекулярных объектов — антигенов. Лимфоциты характеризуются экспрессией Т-клеточных (TCR) или В-клеточных (BCR) рецепторов, распознающих только одну антигенную детерминанту либо небольшое число структурно очень близких детерминант, и поэтому, в отличие от PRR, обладающих высокой специфичностью (рис. 1-1).
Адаптивный (приобретённый) иммунитет формируется в течение жизни индивидуума. Активно приобретённый иммунитет — состояние невосприимчивости к инфекции после перенесённого инфекционного заболевания или после вакцинации (сам организм вырабатывает соответствующие антитела). Пассивно приобретённый иммунитет — состояние невосприимчивости к инфекции в результате поступления в организм уже готовых антител от матери или в результате инъекции (сам организм эти антитела не вырабатывает).
ИММУННЫЙ ОТВЕТ
Врождённая и адаптивная системы защиты организма включают клеточный и гуморальный компоненты и активно взаимодействуют друг с другом в процессе иммунного ответа. Иммунный ответ — многоэтапный процесс, заключающийся в распознавании и деструкции патогена и повреждённых им тканей. В его основе лежит уникальное свойство иммун-

Рис. 1-1. Сравнение врождённого и адаптивного иммунитета
ной системы отличать «свое» («sef») от «чужого» («nonself») и применять по отношению к «чужому» механизмы нейтрализации и уничтожения, а именно — иммунные реакции. Распознавание множества чужеродных антигенов происходит благодаря наличию в организме огромного разнообразия образующихся в тимусе клонов T-лимфоцитов (отбор клонов) и при помощи комплекса генов главного комплекса гистосовместимости (MHC) классов I и II. Нейтрализацию «чужого» осуществляют цирку-
лирующие в жидкостях организма антитела (гуморальный иммунитет) и цитотоксические лимфоциты (клеточный иммунитет).
Таким образом, основными характеристиками адаптивного иммунного ответа являются умение различать собственные антигены от чужеродных, специфичность и иммунная память.
• Различение «своего» и «чужого» выражается в дифференциации компонентов собственных тканей организма и чужеродных молекул. Специфическую неотвечаемость организма на собственные антигены обозначают как иммунную толерантность. Если же организм воспринимает собственные компоненты как чужеродные, развивается аутоиммунный ответ.
• Специфичность иммунного ответа проявляется в том, что иммунитет, сформировавшийся в результате контакта с определённым антигеном, будет обеспечивать защиту только против этого антигена.
• Иммунная память формируется в результате адаптивного иммунного ответа против конкретного возбудителя и сохраняется, как правило, в течение всей последующей жизни организма, защищая его от повторной инфекции, вызываемой этим же возбудителем. Такой механизм обеспечивается способностью иммунной системы к «запоминанию» антигенных детерминант патогена за счёт образования клеток иммунной памяти. Наличие иммунной памяти обусловливает развитие ускоренного и усиленного ответа (вторичный иммунный ответ) при повторном контакте с антигеном. Формирование иммунной памяти является основной целью вакцинации, т.е. процесса естественного или искусственного формирования иммунной защиты против определённой инфекции.
Схема развития иммунного ответа представлена на рис. 1-2. Содержание отдельных этапов иммунного ответа раскрыто ниже.
• Воспаление: участвуют клетки, поглощающие антигены (фагоциты, антигенпрезентирующие клетки) — в частности, дендритные клетки (ДК), макрофаги, эндотелиальные и другие клетки. Выделяются провоспалительные цитокины и хемокины.
• Переработка антигена (процессинг). После поглощения антигена антигенпрезентирующей клеткой (АПК) происходит его процессинг (расщепление и встраивание в молекулы MHC) и презентация на поверхности клетки. Это необходимо для распознавания антигена Т-лимфоцитами.
• Распознавание антигена происходит в периферических лимфоидных органах. Начало специфического иммунного ответа — про-

Рис. 1-2. Основные этапы иммунного ответа
лиферация и дифференцировка эффекторных и регуляторных лимфоцитов.
• Деструкция антигена и повреждённых патогеном тканей. При этом одни лимфоциты (помощники — хелперы) «нанимают» для выполнения эффекторных функций другие лимфоциты (эффекторные) и/или воспалительные лейкоциты (нейтрофилы, моноциты, базофилы, эозинофилы), тучные клетки, а также гуморальные литические системы типа комплемента.
• Выведение продуктов распада происходит с участием известных систем выделения.
КЛЕТКИ ИММУННОЙ СИСТЕМЫ
Клетки иммунной системы условно подразделяют на клетки врождённого и адаптивного иммунитета (рис. 1-3). Главным их различием является специфичность распознавания: низкая у первых и высокая у вторых. Существует и третья группа клеток — промежуточная, несущая черты обеих групп. Наличие этой группы показывает единство происхождения и способов защиты организма от чужеродных веществ антигенной природы.

Рис. 1-3. Клетки иммунной системы
В выполнении эффекторных иммунных функций очень важную роль играют АПК, T- и B-лимфоциты и NK-клетки (от англ. Natural Killer — естественный киллер, натуральный киллер).
• Антигенпрезентирующие клетки (АПК). К АПК относят макрофаги, дендритные клетки (включая клетки Лангерганса эпидермиса, М-клетки лимфатических фолликулов пищеварительного тракта и других слизистых оболочек, дендритные эпителиальные клетки тимуса), а также B-лимфоциты. АПК захватывают антиген, обрабатывают его (процессируют) и презентируют антигенные фрагменты на своей поверхности T-лимфоцитам (рис. 1-4).
• T-лимфоциты обусловливают клеточный иммунный ответ, а также помогают отвечать на антиген B-лимфоцитам при гуморальном иммунном ответе. Каждый T-лимфоцит несет на своей поверхности рецептор T-лимфоцитов (TCR — T-Cell Receptor) (см. рис. 5-1, в и рис. 6-1) строго одной специфичности, т.е. взаимодействующий с одним антигеном. T-клетки по экспрессии маркёрных антигенов CD (Cluster Differentiation) подразделяют на CD4+ и CD8+.
— CD4+ Т-лимфоциты (хелперы). Среди T-клеток, экспрессирующих мембранные маркёры CD4, выделяют Т-лимфоциты с эффекторными функциями (Th1, Th2, Th17) и Т-регуляторные клетки (естественные — Treg и индуцированные — Th3, или Tr1).

Рис. 1-4. Взаимодействие клеток в ходе гуморального иммунного ответа. Рецептор T-хелпера (TCR) распознаёт антигенную детерминанту (эпитоп), экспрессированную на поверхности антигенпрезентирующей клетки вместе с молекулой главного комплекса гистосовместимости класса II (MHC-II). Во взаимодействии участвует маркёрная молекула T-хелпера — CD4. В результате подобного взаимодействия антигенпрезентирующая клетка секретирует интерлейкин-1 (ИЛ-1), стимулирующий в T-хелпере синтез и секрецию цитокинов, включая ИЛ-2, а также синтез и перенос на плазматическую мембрану T-хелпера рецепторов для ИЛ-2 (ИЛ-2 также стимулирует пролиферацию T-хелперов). Отбор B-лимфоцитов происходит при взаимодействии антигена с вариабельными участками антител (иммуноглобулинов) на поверхности этих клеток (правая часть рисунка). Эпитоп этого антигена в комплексе с молекулой MHC-II распознаёт рецептор T-хелпера, после чего T-лимфоцит секретирует цитокины, стимулирующие пролиферацию B-лимфоцитов и их дифференцировку в плазматические клетки, синтезирующие антитела к данному антигену. Также показаны некоторые мембранные белки (CD40/CD40L и CD28/B7), участвующие в проведении костимуляторных сигналов, необходимых для полноценной активации взаимодействующих клеток (они описаны подробнее в главе 7)
◊ T-хелперы при взаимодействии с АПК специфически распознают антигены и начинают вырабатывать определённый набор цитокинов соответственно типу инфекционного агента: Th2 при взаимодействии с B-клетками индуцируют гуморальный иммунный ответ (см. рис. 1-4), а Th1 — при взаимодействии с макрофагами и цитотоксическими Т-лимфоцитами (ЦТЛ) — клеточный иммунный ответ. Th17 продуцируют ИЛ17 — мощный индуктор тканевого воспаления, привлекающий и активирующий гранулоциты и макрофаги.
◊ Регуляторные T-клетки (Т-регуляторы) контролируют интенсивность иммунного ответа, подавляя активность других субпопуляций Т-лимфоцитов.
— CD8+ Т-лимфоциты. Субпопуляция T-клеток, экспрессирующих мембранные молекулы CD8. Эти клетки выступают в роли ЦТЛ. Они лизируют клетки-мишени, несущие чужеродные или видоизменённые собственные антигены — аутоантигены: например, клетки опухоли, трансплантата, инфицированные вирусом клетки, несущие поверхностные вирусные антигены. Эффекторные функции ЦТЛ реализуются через индукцию образования в клетках-мишенях пор (под действием особых белков — перфоринов) и секрецию в поры специализированных сериновых протеаз — гранзимов. Вызванное этим нарушение осмотического баланса с внеклеточной средой приводит к гибели клетки (рис. 1-5). Под влиянием гранзимов индуцируются процессы запрограммированной гибели клетки — апоптоза.
• Т-клетки памяти — долгоживущие рециркулирующие малые лимфоциты, формируемые при первичном иммунном ответе. Они «запоминают» особенности детерминант антигенов и при повторном распознавании того же антигена развивают быстрый и усиленный ответ. Т-клетки памяти отличаются от наивных и эффекторных Т-лимфоцитов высоким уровнем экспрессии мембранных маркёров активации, меньшей потребностью в провоспалительных медиаторах и корецепторных сигналах для развития вторичного иммунного ответа.
• B-лимфоциты отвечают за гуморальный иммунный ответ. На мембране B-лимфоцитов присутствует рецептор для антигена — мономер IgM. Продолжительность жизни большинства B-лимфоцитов (если они не активируются антигеном!) не превышает 10 сут.

Рис. 1-5. Уничтожение клетки-мишени цитотоксическим T-лимфоцитом (Т-киллером). При сближении цитотоксического T-лимфоцита с клеткоймишенью после специфичного взаимодействия мембранных молекул клетокпартнёров T-лимфоцит убивает клетку-мишень
— Эффекторные B-лимфоциты. Активированные B-лимфоциты размножаются и дифференцируются в плазматические клетки (см. рис. 5-9), вырабатывающие антитела (иммуноглобулины, специфичные к конкретному антигену). При этом плазматические клетки теряют экспрессию специфических рецепторов для антигена.
— B-лимфоциты иммунной памяти — долгоживущие рециркулирующие малые лимфоциты. Они не превращаются в плазматические клетки, но сохраняют иммунную «память» об антигене, с которым когда-то контактировали, за счёт продолжающейся экспрессии рецептора для антигена. Клетки памяти активируются
при повторном распознавании того же антигена. В этом случае B-лимфоциты памяти, при обязательном участии T-хелперов и ряда других факторов, превращаются в плазматические клетки, обеспечивая быстрый синтез большого количества специфичных антител, взаимодействующих с чужеродным антигеном, и развитие эффективного иммунного ответа. • NK-клетки (от англ. Natural Killer — естественный киллер) — лимфоциты, лишённые характерных для T- и B-клеток поверхностных CD-маркёров, а также антигенраспознающих рецепторов — TCR (T Cell Receptor) или BCR (B Cell Receptor). Эти клетки играют важную роль в механизмах врождённого иммунитета (см. главу 3), уничтожают трансформированные, инфицированные вирусами и чужеродные клетки.
Источник
