Вакцинацией бцж формируется иммунитет пассивный специфический
Профилактика инфекций посредством вакцинации доказала свою эффективность, является на протяжении двух столетий неотъемлемой частью при формировании защитного иммунитета у населения. Иммунология начала зарождаться в 18 веке, когда Э. Дженнер установил, что доярки, взаимодействующие с зараженными оспой коровами, не болеют впоследствии черной оспой, поражавшей людей того времени. Не зная ничего об иммунитете, его механизмах, доктор создал вакцину, позволившую снизить уровень заболеваемости.

Последователем Дженнера считают Луи Пастера, который определил наличие микроорганизмов, являющихся возбудителями инфекций, получил вакцину против бешенства. Постепенно ученные создали препараты от коклюша, кори, полиомиелита и других, ранее опасных для жизни, здоровья человечества болезней. В 21 веке иммунопрофилактика остается главным инструментом создания специфического иммунитета среди граждан.
Что такое вакцина
Иммунный препарат в состав, которого входят ослабленные, либо убитые вирусные компоненты возбудителей получил название вакцина. Она служит для выработки в организме человека антител, противостоящих антигенам (чужеродным структурам) на протяжении длительного временного периода, отвечающих за устойчивый иммунный барьер.
Разработаны средства (сыворотки) действующие не более нескольких месяцев, отвечающие за выработку пассивного иммунитета. Они вводятся сразу же после инфицирования, позволяют спасти человека от смерти, серьезных патологий. Вакцинация – механизм, обеспечивающий организм специфическими антителами, которые он получает не болея.
Вакцина до прохождения сертификации проходит длительный экспериментальный путь. К использованию допускают препараты со следующими характеристиками:
- Безопасность — после введения вакцины отсутствуют тяжелые осложнения у граждан.
- Протективность – длительное стимулирование защитного потенциала против введенного возбудителя, сохранение иммунологической памяти.
- Иммуногенность – способность к индукции активного иммунитета с долгосрочным эффектом вне зависимости от специфичности антигена.
- Иммунная активность – направленная стимуляция выработки нейтрализующих антител, эффекторных Т-лимфоцитов.
- Вакцина должна быть: биологически стабильной, неизменчивой при транспортировке, хранении, обладать низкой реактогенностью, доступной стоимостью, удобной при применении.
Перечисленные свойства вакцин позволяют свести к минимуму проявление местных реакций и осложнений. В чем заключается разница между понятиями:
- поствакцинальные реакции или местные – кратковременный ответ организма, возникающий на введение вакцины. Он проявляется в виде припухлости, отечности или покраснения в месте инъекции, общих недомоганий – подъема температуры, головной боли. Продолжительность периода составляет в среднем 3 суток, коррекция состояний носит симптоматический характер;
- осложнения после вакцины – возникают отсрочено, принимают патологические формы. К ним относят: аллергические реакции, процессы нагноения, спровоцированные нарушением правил асептики, обострение хронических болезней, наслоение инфекций, полученных в поствакцинальный период.
Разновидности вакцин
Иммунологи разделяю вакцины на типы, отличающиеся способом получения, механизмом действия, компонентным составом и рядом других признаков. Выделяют:
Аттенуированные – препараты производят из живых, но сильно ослабленных вирусов, либо патогенных штаммов микроорганизмов измененных генетически, либо из родственных штаммов (дивергентные суспензии), которые не в состоянии вызвать заражение человека. Корпускулярные вакцины характеризуются сниженной вирулентностью (уменьшенной способностью антигена заражать) при сохранении иммуногенных свойств, то есть способности вызывать иммунный ответ и формировать устойчивый иммунитет.
Примерами живых вакцин служат средства, используемые при иммунизации против чумы, гриппа, кори, краснухи, эпидемического паротита, бруцеллеза, туляремии, натуральной оспы, сибирской язвы. После некоторых прививок, например БЦЖ, требуется ревакцинация для сохранения иммунитета на протяжении жизненного периода.
Инактивированные – состоят из «мертвых» микробных частиц, выращиваемых в других культурах, например, на куриных эмбрионах, затем, убитых под воздействием формальдегида и очищенных от белковых примесей. К обозначенной категории вакцин относятся:
- корпускулярные – добывают из целостных штаммов (цельновирионные), либо из бактерий вируса (цельноклеточные). Примером первых являются противогриппозные суспензии, от клещевого энцефалита, вторых – лиофилизированные массы против лептоспироза, коклюша, брюшного тифа, холеры. Вакцины не вызывают инфицирование организма, но тем не менее содержат протективные антигены, могут спровоцировать аллергии и сенсибилизацию. Преимуществом корпускулярных составов в их стабильности, безопасности, высокой реактогенности;
- химические – изготавливают из бактериальных единиц, имеющих определенную химическую структуру. Отличительной особенностью считают минимальное наличие балластных частиц. К ним причисляют вакцины от дизентерии, пневмококка, брюшного тифа;
- конъюгированные – содержат комплекс из токсинов и бактериальных полисахаридов. Подобные комбинации усиливают индуцирование иммуногеном иммунитета. Например, сочетание вакцины анатоксина дифтерийного и Ar Haemophilus influenzae;
- сплит или субвирионные расщепленные – состоят из внутренних и поверхностных антигенов. Вакцины хорошо очищены, поэтому переносятся без выраженных побочных проявлений. Примером служат некоторые средства против гриппа;
- субъединичные – образованы из молекул инфекционных частиц, то есть имеют изолированные антигены микробов. Например, Гриппол, Инфлювак. Отдельно обозначают анатоксин – состав, выработанный из обезвреженных токсинов бактерий, который сохранил анти- и иммуногенность. Анатоксины способствуют формированию напряженного иммунитета длительностью до 5 лет и больше;
- рекомбинантные генно-инженерные – получают при содействии рекомбинантных ДНК, переносимых из вредоносного микроорганизма. Например, вакцина от ВГВ.
Сравнительный анализ вакцин
Таблица №1
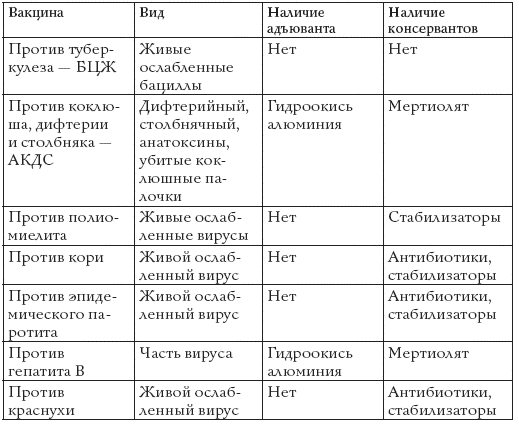
Особенности поствакцинального иммунитета
После тех или иных прививок, у человека вырабатывается иммунитет специфичный по отношению к введенным инфекционным возбудителям, формируется невосприимчивость к ним. Основными характеристиками иммунитета, возникшего от вакцины, считаются:
- выработка антител к специфичным антигенам инфекционного заболевания;
- формирование иммунитета через 2 – 3 недели;
- поддержание способности клеток длительно сохранять информацию, отвечать реакцией при выявлении гомогенного антигена;
- пониженная невосприимчивость к инфицированию при сравнении с иммунитетом, образованным после перенесенного заболевания.
Иммунитет, приобретенный человеком посредством прививок, не наследуется, при грудном кормлении не передается. В своем становлении он проходит 3 этапа:
- Скрытый. На протяжении первых 3 дней формирование протекает латентно, без видимых изменений в иммунном статусе.
- Период роста. Длится в зависимости от препарата, особенностей организма от 3 до 30 дней. Характеризуется увеличением количества антител по отношению к возбудителю, полученному при инъекции.
- Снижения иммунитета. Постепенное уменьшение ответа от прививок штаммов.
Получить полноценный ответ на Т-зависимые антигены, возможно при соблюдении ряда условий: применять следует протективные, правильно дозированные вакцины, обеспечивающие продолжительный контакт с иммунной системой. Длительность взаимодействия обеспечивают путем создания «депо», введением суспензии по схеме с соблюдением указанных интервалов, своевременной ревакцинацией. Устойчивость организма к инфекциям обеспечивается отсутствием стрессов, ведением подвижного образа жизни, сбалансированные питанием.
Вакцинацию откладывают при высоких показателях температуры, хронических заболеваниях в обостренной фазе, воспалительных процессах, иммуннодефиците, гемобластозе. Следует оценить риски вакцинации при планировании и в период беременности, аллергических состояниях при введении предыдущих вакцин.
Глобализация применения вакцин
Каждый гражданин должен понимать, что предотвратить распространение инфекции можно лишь профилактическими мероприятиями, которые отражены в календаре прививок отдельно взятого государства. В документе указана информация о перечне вакцин, эпидемиологически оправданных для конкретной территории, сроках их постановки.
ВОЗ создала расширенную программу иммунизации (РПИ) в 1974 году, направленную на предупреждение возникновения инфекций, сокращение их распространения.
Благодаря РПИ выделяют несколько значимых этапов, позволивших сократить возникновение очагов ряда заболеваний:
- 1974 – 1990 гг. – активная иммунизация против кори, столбняка, полиомиелита, туберкулеза, коклюша;
- 1990 – 2000 гг. – ликвидация краснухи беременных, полиомиелита, столбняка новорожденных. Снижение инфицирования корью, свинкой, коклюшем, параллельная разработка, применение суспензий, сывороток против японского энцефалита, желтой лихорадки;
- 2000 – 2025 гг. – реализуется введение ассоциированных препаратов, планируется ликвидация дифтерии, краснухи, кори, гемофильной инфекции, паротита.
Масштабный охват вызывает некоторые опасения со стороны населения, среди молодых родителей, опасающихся мельчайших признаков нездоровья ребенка. Следует помнить, что средства, формирующие иммунитет, защитят от специфичных заболеваний, предотвратят осложнения, патологические изменения, смерть при инфицировании в ситуациях отказа от прививки. Даже здоровый образ жизни не способен обезопасить организм от воздействия вирусов, бактерий.
В случаях заражения после прививки, например при ненадлежащем хранении средства, нарушениях введения препарата, болезнь протекает легко и без последствий, благодаря наличию иммунитета. Плановая вакцинация экономически оправдана, так как лечение в случае инфицирования потребует больше средств, чем стоимость вакцины.
Видео: сроки формирования БЦЖ
Источник
Степень активации при двукратном введении была выше, чем при однократном, и при внутрибрюшинном введении выше, чем при подкожном. Выраженная стимуляция получена при использовании доз в диапазоне от 5-106 до 1-108 бактериальных клеток на мышь. Цитотоксичность КПЭ индуцируется БЦЖ уже через час после введения, сильно возрастая к 3-му дню, достигает максимального значения на 4-5-й день и постепенно возвращается к исходному уровню на 22-е сутки. По мнению D. Е. Tracey, цитотоксичность КПЭ, по крайней мере на фазе пика (4-6-й день) после введения БЦЖ, обусловлена не макрофагами, активность которых развивается позднее, не Т-лимфоцитами и К-клетками, а ЕКК, которые в этих условиях усиленно нарабатываются и скапливаются в брюшной полости. При неспецифической терапии опухолей у людей с помощью БЦЖ или C. parvum также повышается активность ЕКК. Позднее D. Е. Tracey пришел к выводу, что индукция ЕКК под влиянием БЦЖ происходит при обязательном участии макрофагов, осуществляемом, возможно, с помощью растворимых факторов, выделяемых макрофагами. Повышение антителозависимой цитоксичности клеток селезенки мышей, обработанных БЦЖ и С. parvum, также происходит при участии макрофагов, так как элиминация последних из суспензии спленоцитов ведет к ее отмене. Вероятно, цитолитическое действие клеток перитонеального экссудата является результатом синергического влияния ЕКК и макрофагов.
Иммуномодулирующее действие БЦЖ далеко не исчерпывается описанными феноменами. Важная роль принадлежит индукции супрессорных клеток, выявляемых в различных тест-системах.
Спустя 1-2 недели после внутривенного или внутрибрюшинного введения БЦЖ мышам разных линий, у них угнетается пролиферативный ответ клеток селезенки на ФГА, КонА и ЛПС, снижается индукция кожной ПЧЗТ, а клетки селезенки приобретают способность супрессировать реакцию смешанной культуры лимфоцитов, генерацию in vitro Т-лимфоцитов, цитотоксичных для опухолевых клеток-мишеней и образование АОК к ЭБ.
С наибольшей вероятностью на роль клеток-супрессоров претендуют активированные БЦЖ-лимфоциты-супрессоры. По-видимому, механизм реализации индуцированной БЦЖ супрессии в отношении отдельных иммунологических реакций может быть различным. В экспериментах G. R. KHmpel прилипающие клетки селезенки мышей линии C57BL/6, которым за 20 суток до опыта ввели БЦЖ (108 живых клеток), in vitro подавляли образование лимфоцитов, способных лизировать клетки мастоцитомы Р815, и продукцию АОК по отношению к ЭБ. Супернатант же культуры супрессирующих клеток угнетал только образование АОК.
Сложность переплетения иммуностимулирующих и иммуносупрессивных эффектов определяет неоднозначность влияния БЦЖ на противоопухолевый иммунитет как в экспериментальных условиях, так и в клинике. На ряде моделей показано тормозящее влияние БЦЖ на прививаемость и развитие экспериментальных опухолей. Противоположные результаты получены в работах Г. Т. Жалгабаевой, Л. В. Агибаловой, J. L. Bernheim и некоторых других исследователей. Противоопухолевая эффективность БЦЖ зависит от вида вакцины, дозы и режимов введения, а в эксперименте — от вида и даже, как указывает А. И. Валетов, от линии животных.
Эксперименты В. И. Каледина, выполненные на мышах с трансплантацией карциномы Кребс-2, демонстрируют значение режима и места введения БЦЖ относительно опухолевых клеток. Предварительное введение малых доз вакцины тормозит опухолевый рост. Совместная инокуляция БЦЖ и опухолевых клеток угнетает, а контралатеральное введение их стимулирует рост опухоли. Выявленная закономерность указывает на значение наступающего под влиянием БЦЖ перераспределения клеток, ответственных за противоопухолевую резистентность. В связи с тем что оптимальный противоопухолевый эффект достигается при локализации БЦЖ непосредственно в области роста опухолевых клеток, В. И. Каледин и Ю. Н. Курунов полагают, что хорошие результаты можно ожидать от введения вакцины в район операции после хирургического удаления лимфогенно метастазирующих иммуногенных опухолей. С обсуждением различных аспектов механизма противоопухолевого и противолейкозного действия БЦЖ можно познакомиться в отечественных публикациях обзорного типа. Все авторы предупреждают о возможности эффекта усиления опухолевого роста в результате индукции БЦЖ блокирующих факторов.
БЦЖ с разной мерой успеха довольно широко используется в лечении онкологических больных в комплексе с цитостатическими препаратами.
Н. С. Кислят, используя вакцинацию БЦЖ в комбинации с химиопрепаратами в период ремиссии острого лейкоза у детей, достиг пролонгирования ремиссии и увеличения продолжительности жизни детей. При включении БЦЖ в комплексную терапию у больных лимфогранулематозом, хотя этим и не удается добиться увеличения продолжительности их жизни, отмечены возрастание длительности первой ремиссии, продолжительная динамика показателей кожного туберкулинового теста, увеличение числа лимфоцитов в периферической крови и спонтанного розеткообразования. Использование же БЦЖ у больных меланомой кожи существенного влияния на течение и исход заболевания не оказало, за исключением улучшения процентных показателей -2-летних ремиссий у больных в группах риска без очевидных метастазов. Однако, по предварительным данным R. Lieberman и Н. Н. Fudenberg, у части больных меланомой, леченных БЦЖ, в периферической крови повысились число Т-РОК и активность сывороточного лизоцима.
Страница 2 — 2 из 3
Источник
Содержание:
- Почему мы уделяем такое внимание прививке БЦЖ
- Почему именно эта прививка обычно бывает первой в жизни новорожденного?
- Когда формируется противотуберкулезный иммунитет?
- Каковы особенности ухода за местом введения вакцины
- Как происходит отбор новорожденных на вакцинацию
- Какие осложнения могут быть после вакцин?
- Немного о ревакцинации
- Это важно знать
- Что такое проба Манту?
- Что такое туберкулез?
Даже те, кто не особенно увлекался словесностью в школе, наверняка помнят, что в произведениях русской литературы XIX в. буквально свирепствовала болезнь под названием «чахотка». Так называли в те времена туберкулез (преимущественно туберкулез легких), тысячами уносивший человеческие жизни.
В 1882 г. немецкий микробиолог Роберт Кох нашел «злоумышленника» — бактерию, вызывающую туберкулез. В честь этого ученого она и была названа — «палочка Коха». (В современной медицине эти смертельно опасные для человека микроорганизмы называют микобактериями туберкулеза.) Однако, несмотря на то, что виновника уже «знали в лицо», человечество еще почти полвека было заложником этого рокового недуга.
Только в 1923 г. двое французских ученых — Кальметт и Герен — создали противотуберкулезную вакцину (отсюда и название культуры — Bacillum CalmetteGuerin, BCG; в русской транскрипции — БЦЖ). Задача у них была не из легких: нужно было создать такой штамм (т.е. разновидность) болезнетворной бактерии, который, во-первых, будет устойчив во внешней среде (иначе вакцину невозможно хранить), а во-вторых, способен вызывать заболевание ровно в той степени, которая позволит человеческому организму выработать иммунитет, но не нанесет ему при этом существенного вреда. В течение 10 лет они пересаживали культуру микобактерии туберкулеза со среды на среду — и наконец добились успеха.
Впервые вакцина БЦЖ была применена в том же 1923 году в Париже, в институте Пастера, и ее давали перорально (через рот). Первые вакцинные штаммы вызывали разные осложнения, и понадобилось еще много лет работы, чтобы вакцина получила повсеместное распространение. В нашу страну она была завезена еще в довоенный период, но применялась только в крупных городах.
Отечественные ученые создали сухую вакцину, которая долго сохранялась и могла быть транспортирована в любые уголки страны. Однако обязательное массовое применение вакцины в СССР началось лишь с 1962 года с соответствующим постановлением правительства.
Современная вакцина БЦЖ вводится внутрикожно, обеспечивая развитие локального (местного, ограниченного) туберкулезного процесса, неопасного для общего здоровья человека. В результате организм вырабатывает специфические защитные антитела против микобактерии туберкулеза.
Почему мы уделяем такое внимание прививке БЦЖ
Известно, что туберкулез — не только медицинская, но и во многом социальная проблема, и увеличение заболеваемости населения туберкулезом часто бывает связано с катаклизмами, происходящими в общественной жизни страны. Все мы знаем, какими трудными для нас были конец восьмидесятых — начало девяностых годов. Так вот, с 1989 года в нашей стране отмечается ежегодный подъем заболеваемости туберкулезом, причем в первую очередь туберкулез поражает детей с их неокрепшей иммунной системой. Кроме того, система раннего выявления туберкулеза в нашей стране разлажена. Вы вряд ли вспомните, когда последний раз проходили флюорографию. Если на некоторых государственных предприятиях она входит в обязательную диспансеризацию сотрудников, то в коммерческих структурах флюорография является даже экономически невыгодной. Больные туберкулезом нуждаются не только в лечении, но и в постоянном медицинском наблюдении. Если учесть, что очень большой процент среди них приходится на долю так называемых «асоциальных элементов», наблюдение за которыми невозможно, становится понятным, почему сегодня созданы прекрасные условия для распространения микобактерии. Очевидно, что увеличение заболеваемости взрослых сказывается и на аналогичном показателе у детей.
В настоящее время цифра детской заболеваемости составляет 17,8 на 100 000, а смертности от туберкулеза — 0,1 на 100000. Всемирная организация здравоохранения (ВОЗ) включила Россию в число стран, где рекомендована обязательная вакцинация против туберкулеза.
Иммунизация вакциной БЦЖ в раннем возрасте снижает заболеваемость в 15 раз и предупреждает развитие тяжелых форм туберкулеза, захватывающих многие органы и системы. Туберкулез — тяжелое заболевание, которое гораздо легче предотвратить, чем вылечить.
За последние годы наметился рост туберкулеза и в экономически развитых странах. Это связано с тем, что микобактерия приспосабливается, вырабатывает устойчивость к противотуберкулезным препаратам. Поэтому во всем мире отношение к вакцине БЦЖ, очень серьезное, так как она является эффективным способом профилактики заболеваемости туберкулезом.
Почему именно эта прививка обычно бывает первой в жизни новорожденного?
Доказано, что иммунная система ребенка готова к вакцинации уже с момента рождения, а туберкулез является одной из наиболее опасных инфекций, подстерегающих малыша после выписки из родильного дома. Обычно вакцинация проводится на 3-7 сутки, причем чем раньше она будет проведена, тем раньше иммунная система организма познакомится с возбудителем туберкулеза, тем эффективнее будет ее ответ в случае контакта с инфекционным агентом.
Мы настоятельно рекомендуем производить вакцинацию БЦЖ именно в условиях родильного дома, а не в поликлинике после выписки, так как, во-первых, в поликлиниках чаще встречаются нарушения техники проведения прививок, которые могут привести к осложнениям, а во-вторых, ребенок никогда не застрахован от встречи с микобактерией дома, на улице, в той же поликлинике — и при отсутствии у него иммунитета такая встреча может оказаться очень и очень опасной.
Когда формируется противотуберкулезный иммунитет?
Полноценный противотуберкулезный иммунитет формируется до года. Критерием успешной иммунизации является появление рубца на плече, в месте введения вакцины — следствия перенесенного локального кожного туберкулеза. Слишком маленький, незаметный рубчик говорит о недостаточной иммунизации.
Каковы особенности ухода за местом введения вакцины
Через 2-3 месяца на коже в месте инъекции формируется инфильтрат (уплотнение или утолщение ткани), напоминающий укус комара. В норме он должен быть не более 1 см в диаметре. Иногда инфильтрат покрыт корочкой. Корочку ни в коем случае нельзя удалять! Она может отпадать самостоятельно, отмокать во время водных процедур и затем появляться вновь. При купании ребенка следует избегать намыливания этой области мочалкой. К 6 месяцам, как правило, формируется нежный рубчик, который принимает свой окончательный вид к году.
Категорически запрещается смазывать место введения вакцины антисептическими растворами — бриллиантовой зеленью, йодом, спиртом, так как это может повредить развитию местного инфекционного процесса.
Как происходит отбор новорожденных на вакцинацию
Вакцинация БЦЖ абсолютно противопоказана:
- детям, в семьях которых отмечены случаи врожденного или приобретенного (вызванного ВИЧ-инфекцией) иммунодефицита;
- детям, у братьев или сестер которых наблюдались осложнения после противотуберкулезной вакцинации;
- детям с врожденными ферментопатиями1, тяжелыми наследственными заболеваниями (например, болезнью Дауна), тяжелыми перинатальными поражениями ЦНС (детский церебральный паралич).
Вакцинация БЦЖ откладывается до выздоровления:
- при любых инфекционных процессах;
- при гемолитической болезни новорожденных (т.е. заболевании, развившемся вследствие несовместимости крови матери и плода по резус-фактору или группе крови);
- при глубокой степени недоношенности.
Какие осложнения могут быть после вакцин?
Осложнения после этой прививки делятся на две категории:
- Тяжелые осложнения, связанные с генерализацией (распространением) инфекции. Вакцина БЦЖ — это, как уже отмечалось выше, живая культура. Поэтому она может вызывать специфические (т.е. связанные с развитием туберкулезного процесса) осложнения. Как правило, такие осложнения бывают связаны с неправильным отбором детей на прививку. Однако хотелось бы подчеркнуть, что риск подобных осложнений гораздо меньше, чем риск заболевания у невакцинированного ребенка.
- Более легкие осложнения, связанные в т.ч. с нарушением техники введения вакцины или некачественной вакциной.
- Изъязвление инфильтрата. Область уплотнения или утолщения ткани в месте инъекции (инфильтрат) увеличивается в диаметре (больше 1 мм), изъязвляется; язва безболезненная, с небольшим отделяемым.
- Образование подкожного инфильтрата. Инфильтрат образуется не в коже, а под кожей. Выглядит он как «шарик», прощупывающийся под гладкой, неизмененной кожей. Это осложнение связано с чрезмерно глубоким введением вакцины, и, если вовремя не обратиться к врачу, инфильтрат может прорваться внутрь, и инфекция попадет в кровеносное русло.
- Образование келоида. Это достаточно редкое осложнение, причем у новорожденных оно встречается реже, чем у более старших детей. Представляет собой общее наследственное заболевание, при котором любое повреждение кожи сопровождается чрезмерным разрастанием рубцовой ткани. В случае образования келоида после прививки рубец становится ярким, сквозь него просвечивают сосуды, иногда появляется зуд.
- Распространение инфекции на лимфоузлы. В этом случае определяются увеличенные безболезненные подмышечные лимфатические узлы, которые матери чаще всего замечают при купании ребенка. Такой лимфатический узел имеет размер грецкого ореха, а иногда — куриного яйца. Изредка инфекция прорывается через кожу, и образуется свищ, то есть канал, через который отходит отделяемое.
При появлении любого из вышеперечисленных осложнений, а также других необычных явлений следует немедленно обратиться к фтизиатру.
Немного о ревакцинации
Иммунитет, приобретенный после прививки БЦЖ, сохраняется в среднем 5 лет. Для поддержания приобретенного иммунитета повторные вакцинации (ревакцинации) проводятся в настоящее время в 7 и 14 лет — считается, что в этом возрасте дети наиболее уязвимы для заражения туберкулезом. Последние исследования показывают, что большее количество ревакцинаций нецелесообразно.
Это важно знать
Совершенно справедливо считается, что туберкулез — болезнь людей низкого достатка. Однако важно знать, что, в связи с неблагоприятной эпидемиологической ситуацией в нашей стране и в мире, с этой болезнью может встретиться любой человек, независимо от уровня его достатка! И действительно, в последнее время наблюдается рост заболеваемости туберкулезом среди обеспеченных слоев общества.
Теоретически родители вправе отказаться от проведения вакцинации БЦЖ своему ребенку. Однако, принимая такое решение, необходимо помнить, что от туберкулеза не застрахован никто, особенно беззащитный ребенок. Среди новорожденных для туберкулеза нет «благополучных» и «неблагополучных» детей. Исходя из этого, хотелось бы подчеркнуть важность и обязательность вакцинопрофилактики всех новорожденных детей независимо от социального положения.
Что такое проба Манту?
Проба Манту (туберкулинодиагностика — метод раннего выявления туберкулезной инфекции) была предложена французским ученым Шарлем Манту в 1908 г., т.е. еще до получения противотуберкулезной вакцины, и в течение вот же почти века широко используется во многих странах, в том числе и в нашей. Ее принцип состоит во внутрикожном ведении в человеческий организм малых доз туберкулина — аллергена, полученного из микобактерии туберкулеза, и наблюдения за местной реакцией. Если организм уже встречался с микобактерией, местная реакция на повторную встречу будет бурной (это называется сенсибилизацией организма), а проба — положительной. Иными словами, положительная реакция означает, что воспаление превышает естественную реакцию, вызываемую самим уколом. На третий день после инъекции измеряется диаметр образовавшейся в результате пробы Манту папулы (воспалительной «бляшки» или «пуговки»)-результаты измерения позволяют оценить напряженность иммунитета к туберкулезной палочке. При этом измеряется только размер самого уплотнения, покраснение вокруг уплотнения не является признаком иммунитета к туберкулезу или инфицированности.
Проба Манту — важное средство ранней диагностики туберкулеза, однако она не дает 100% гарантии: возможен как ложноположительный, так и ложноотрицательный результат. Во всех сомнительных случаях диагноз ставится врачом на основе совокупности диагностических признаков.
Первая проба Манту предстоит вашему ребенку в возрасте одного года, затем — каждый год. До момента оценки результатов важно не допускать контакта места пробы с водой и другими жидкостями, не разрешать ребенку расчесывать «пуговку». Не надо мазать место пробы зеленкой, перекисью, а также заклеивать ранку лейкопластырем — под ним кожа может потеть. Помните, что неправильный уход за местом введения туберкулина может повлиять на результат пробы, а это не нужно ни пациенту, ни врачу.
После оценки результатов, если образовался гнойничок или язвочка, ее можно обрабатывать как любую другую ранку, с применением всех традиционных средств.
Проба Манту — не прививка! Поэтому если ваш ребенок по каким-либо причинам освобожден от профилактических прививок, проба Манту должна быть произведена.
Что такое туберкулез?
Туберкулез — это инфекционно-аллергическое заболевание, возбудителем которого является микобактерия туберкулеза, или палочка Коха. Туберкулезная инфекция может поражать различные органы и ткани человека: легкие (чаще всего), глаза, кости, кожу, мочеполовую систему, кишечник и т.д. Инфекция передается в основном воздушно-капельным путем, попадая в органы дыхания от больного человека к здоровому, поэтому заразиться можно где угодно и совсем не обязательно в результате тесного контакта с больным. Микобактерии туберкулеза обладают значительной устойчивостью к различным физическим и химическим агентам, холоду, теплу, влаге и свету. В естественных условиях при отсутствии солнечного света они могут сохранять свою жизнеспособность в течение нескольких месяцев. В уличной пыли микобактерии сохраняются в течение 10 дней. На страницах книг они могут оставаться живыми в течение трех месяцев. В воде микобактерии сохраняются очень долго (до 150 дней).
При активной форме туберкулеза палочка Коха быстро размножается в легких больного и разрушает пораженный орган, отравляет организм человека продуктами своей жизнедеятельности, выделяя в него токсины. Идет процесс туберкулезной интоксикации, иначе говоря, отравления организма человека.
При отсутствии лечения в половине случаев развивается активный туберкулез, который чреват смертельным исходом в течение 1-2 лет.
В другой половине случае нелеченый туберкулез переходит в хроническую форму; причем хронически больной человек продолжает выделять возбудителей туберкулеза и заражать окружающих.
Палочка Коха не отличает богатых от бедных, однако малоимущие граждане, живущие в тесноте, сырости, без средств, необходимых для обеспечения нормального питания и приобретения лекарств, составляют «группу риска» в отношении заболеваемости туберкулезом. Если общество не создает условий для улучшения условий жизни малоимущих, риск распространяется на все слои общества. Туберкулез можно с полным правом назвать социальной болезнью.
Очень опасен туберкулез при беременности. Если беременность наступает на фоне активного туберкулеза легких, то болезнь обостряется. Течение беременности часто осложняется преждевременными родами, причиной чего является интоксикация и кислородная недостаточность, вызываемые инфекцией. У беременных, больных туберкулезом, чаще, чем у здоровых, наблюдаются ранние и поздние токсикозы, у них отмечается меньшая продолжительность родов по сравнению со здоровыми женщинами. При некоторых видах туберкулеза легких рекомендуется даже прерывание беременности (особенно на ранних сроках).
1Ферментопатия — это врожденная недостаточность функции какого-либо фермента или полное его отсутствие. В результате ферментопатии развивается соответствующее нарушение обмена веществ.
Валентина Аксенова
Главный фтизиопедиатр МЗ РФ,
руководитель детско-подросткового отделения
НИИ фтизиопульмонологии ММА им. И.М. Сеченова,
руководитель Российского центра осложнений БЦЖ,
профессор, д.м.н.
Источник
