Вид иммунитета у вакцинированного
Как устроен иммунитет: Объясняем по пунктам
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
Кто отвечает за работу различных видов иммунитета?
- Костный мозг. Это центральный орган иммуногенеза. В костном мозге образуются все клетки, участвующие в иммунных реакциях.
- Тимус (вилочковая железа). В тимусе происходит дозревание некоторых иммунных клеток (Т-лимфоцитов) после того, как они образовались в костном мозге.
- Селезенка. В селезенке также дозревают иммунные клетки (B-лимфоциты), кроме того, в ней активно происходит процесс фагоцитоза — когда специальные клетки иммунной системы ловят и переваривают проникших в организм микробов, фрагменты собственных погибших клеток и так далее.
- Лимфатические узлы. По своему строению они напоминают губку, через которую постоянно фильтруется лимфа. В порах этой губки есть очень много иммунных клеток, которые также ловят и переваривают микробов, проникших в организм. Кроме того, в лимфатических узлах находятся клетки памяти — это специальные клетки иммунной системы, которые хранят информацию о микробах, уже проникавших в организм ранее.
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
- Т-лимфоциты. Названы так, потому что после образования в костном мозге дозревают в вилочковой железе — тимусе. Разные подвиды Т-лимфоцитов отвечают за разные функции. Например, Т-киллеры могут убивать зараженные вирусами клетки, чтобы остановить развитие инфекции, Т-хелперы помогают иммунной системе распознавать конкретные виды микробов, а Т-супрессоры регулируют силу и продолжительность иммунной реакции.
- B-лимфоциты. Название их происходит от Bursa fabricii (сумка Фабрициуса) — особого органа у птиц, в котором впервые обнаружили эти клетки. В-лимфоциты умеют синтезировать антитела (иммуноглобулины). Это специальные белки, которые «прилипают» к микробам и вызывают их гибель. Также антитела могут нейтрализовывать некоторые токсины.
- Натуральные киллеры. Эти клетки находят и убивают раковые клетки и клетки, пораженные вирусами.
- Нейтрофилы и макрофаги умеют ловить и переваривать микробов — осуществлять фагоцитоз. Кроме того, макрофаги выполняют важнейшую роль в процессе презентации антигена, когда макрофаг знакомит другие клетки иммунной системы с кусочками переваренного микроба, что позволяет организму лучше бороться с инфекцией.
- Эозинофилы защищают наш организм от паразитов — обеспечивают антигельминтный иммунитет.
- Базофилы — выполняют главным образом сигнальную функцию, выделяя большое количество сигнальных веществ (цитокинов) и привлекая этим другие иммунные клетки в очаг воспаления.
Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
Источник
Профилактика инфекций посредством вакцинации доказала свою эффективность, является на протяжении двух столетий неотъемлемой частью при формировании защитного иммунитета у населения. Иммунология начала зарождаться в 18 веке, когда Э. Дженнер установил, что доярки, взаимодействующие с зараженными оспой коровами, не болеют впоследствии черной оспой, поражавшей людей того времени. Не зная ничего об иммунитете, его механизмах, доктор создал вакцину, позволившую снизить уровень заболеваемости.

Последователем Дженнера считают Луи Пастера, который определил наличие микроорганизмов, являющихся возбудителями инфекций, получил вакцину против бешенства. Постепенно ученные создали препараты от коклюша, кори, полиомиелита и других, ранее опасных для жизни, здоровья человечества болезней. В 21 веке иммунопрофилактика остается главным инструментом создания специфического иммунитета среди граждан.
Что такое вакцина
Иммунный препарат в состав, которого входят ослабленные, либо убитые вирусные компоненты возбудителей получил название вакцина. Она служит для выработки в организме человека антител, противостоящих антигенам (чужеродным структурам) на протяжении длительного временного периода, отвечающих за устойчивый иммунный барьер.
Разработаны средства (сыворотки) действующие не более нескольких месяцев, отвечающие за выработку пассивного иммунитета. Они вводятся сразу же после инфицирования, позволяют спасти человека от смерти, серьезных патологий. Вакцинация – механизм, обеспечивающий организм специфическими антителами, которые он получает не болея.
Вакцина до прохождения сертификации проходит длительный экспериментальный путь. К использованию допускают препараты со следующими характеристиками:
- Безопасность — после введения вакцины отсутствуют тяжелые осложнения у граждан.
- Протективность – длительное стимулирование защитного потенциала против введенного возбудителя, сохранение иммунологической памяти.
- Иммуногенность – способность к индукции активного иммунитета с долгосрочным эффектом вне зависимости от специфичности антигена.
- Иммунная активность – направленная стимуляция выработки нейтрализующих антител, эффекторных Т-лимфоцитов.
- Вакцина должна быть: биологически стабильной, неизменчивой при транспортировке, хранении, обладать низкой реактогенностью, доступной стоимостью, удобной при применении.
Перечисленные свойства вакцин позволяют свести к минимуму проявление местных реакций и осложнений. В чем заключается разница между понятиями:
- поствакцинальные реакции или местные – кратковременный ответ организма, возникающий на введение вакцины. Он проявляется в виде припухлости, отечности или покраснения в месте инъекции, общих недомоганий – подъема температуры, головной боли. Продолжительность периода составляет в среднем 3 суток, коррекция состояний носит симптоматический характер;
- осложнения после вакцины – возникают отсрочено, принимают патологические формы. К ним относят: аллергические реакции, процессы нагноения, спровоцированные нарушением правил асептики, обострение хронических болезней, наслоение инфекций, полученных в поствакцинальный период.
Разновидности вакцин
Иммунологи разделяю вакцины на типы, отличающиеся способом получения, механизмом действия, компонентным составом и рядом других признаков. Выделяют:
Аттенуированные – препараты производят из живых, но сильно ослабленных вирусов, либо патогенных штаммов микроорганизмов измененных генетически, либо из родственных штаммов (дивергентные суспензии), которые не в состоянии вызвать заражение человека. Корпускулярные вакцины характеризуются сниженной вирулентностью (уменьшенной способностью антигена заражать) при сохранении иммуногенных свойств, то есть способности вызывать иммунный ответ и формировать устойчивый иммунитет.
Примерами живых вакцин служат средства, используемые при иммунизации против чумы, гриппа, кори, краснухи, эпидемического паротита, бруцеллеза, туляремии, натуральной оспы, сибирской язвы. После некоторых прививок, например БЦЖ, требуется ревакцинация для сохранения иммунитета на протяжении жизненного периода.
Инактивированные – состоят из «мертвых» микробных частиц, выращиваемых в других культурах, например, на куриных эмбрионах, затем, убитых под воздействием формальдегида и очищенных от белковых примесей. К обозначенной категории вакцин относятся:
- корпускулярные – добывают из целостных штаммов (цельновирионные), либо из бактерий вируса (цельноклеточные). Примером первых являются противогриппозные суспензии, от клещевого энцефалита, вторых – лиофилизированные массы против лептоспироза, коклюша, брюшного тифа, холеры. Вакцины не вызывают инфицирование организма, но тем не менее содержат протективные антигены, могут спровоцировать аллергии и сенсибилизацию. Преимуществом корпускулярных составов в их стабильности, безопасности, высокой реактогенности;
- химические – изготавливают из бактериальных единиц, имеющих определенную химическую структуру. Отличительной особенностью считают минимальное наличие балластных частиц. К ним причисляют вакцины от дизентерии, пневмококка, брюшного тифа;
- конъюгированные – содержат комплекс из токсинов и бактериальных полисахаридов. Подобные комбинации усиливают индуцирование иммуногеном иммунитета. Например, сочетание вакцины анатоксина дифтерийного и Ar Haemophilus influenzae;
- сплит или субвирионные расщепленные – состоят из внутренних и поверхностных антигенов. Вакцины хорошо очищены, поэтому переносятся без выраженных побочных проявлений. Примером служат некоторые средства против гриппа;
- субъединичные – образованы из молекул инфекционных частиц, то есть имеют изолированные антигены микробов. Например, Гриппол, Инфлювак. Отдельно обозначают анатоксин – состав, выработанный из обезвреженных токсинов бактерий, который сохранил анти- и иммуногенность. Анатоксины способствуют формированию напряженного иммунитета длительностью до 5 лет и больше;
- рекомбинантные генно-инженерные – получают при содействии рекомбинантных ДНК, переносимых из вредоносного микроорганизма. Например, вакцина от ВГВ.
Сравнительный анализ вакцин
Таблица №1
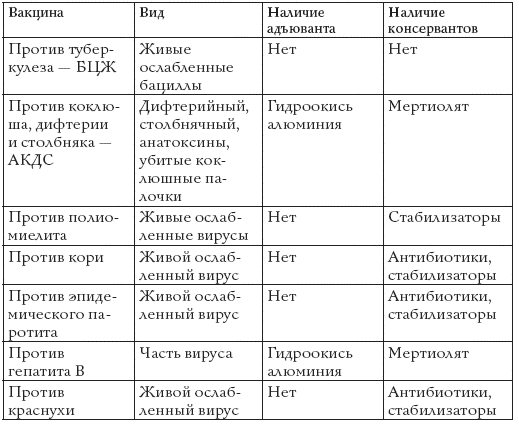
Особенности поствакцинального иммунитета
После тех или иных прививок, у человека вырабатывается иммунитет специфичный по отношению к введенным инфекционным возбудителям, формируется невосприимчивость к ним. Основными характеристиками иммунитета, возникшего от вакцины, считаются:
- выработка антител к специфичным антигенам инфекционного заболевания;
- формирование иммунитета через 2 – 3 недели;
- поддержание способности клеток длительно сохранять информацию, отвечать реакцией при выявлении гомогенного антигена;
- пониженная невосприимчивость к инфицированию при сравнении с иммунитетом, образованным после перенесенного заболевания.
Иммунитет, приобретенный человеком посредством прививок, не наследуется, при грудном кормлении не передается. В своем становлении он проходит 3 этапа:
- Скрытый. На протяжении первых 3 дней формирование протекает латентно, без видимых изменений в иммунном статусе.
- Период роста. Длится в зависимости от препарата, особенностей организма от 3 до 30 дней. Характеризуется увеличением количества антител по отношению к возбудителю, полученному при инъекции.
- Снижения иммунитета. Постепенное уменьшение ответа от прививок штаммов.
Получить полноценный ответ на Т-зависимые антигены, возможно при соблюдении ряда условий: применять следует протективные, правильно дозированные вакцины, обеспечивающие продолжительный контакт с иммунной системой. Длительность взаимодействия обеспечивают путем создания «депо», введением суспензии по схеме с соблюдением указанных интервалов, своевременной ревакцинацией. Устойчивость организма к инфекциям обеспечивается отсутствием стрессов, ведением подвижного образа жизни, сбалансированные питанием.
Вакцинацию откладывают при высоких показателях температуры, хронических заболеваниях в обостренной фазе, воспалительных процессах, иммуннодефиците, гемобластозе. Следует оценить риски вакцинации при планировании и в период беременности, аллергических состояниях при введении предыдущих вакцин.
Глобализация применения вакцин
Каждый гражданин должен понимать, что предотвратить распространение инфекции можно лишь профилактическими мероприятиями, которые отражены в календаре прививок отдельно взятого государства. В документе указана информация о перечне вакцин, эпидемиологически оправданных для конкретной территории, сроках их постановки.
ВОЗ создала расширенную программу иммунизации (РПИ) в 1974 году, направленную на предупреждение возникновения инфекций, сокращение их распространения.
Благодаря РПИ выделяют несколько значимых этапов, позволивших сократить возникновение очагов ряда заболеваний:
- 1974 – 1990 гг. – активная иммунизация против кори, столбняка, полиомиелита, туберкулеза, коклюша;
- 1990 – 2000 гг. – ликвидация краснухи беременных, полиомиелита, столбняка новорожденных. Снижение инфицирования корью, свинкой, коклюшем, параллельная разработка, применение суспензий, сывороток против японского энцефалита, желтой лихорадки;
- 2000 – 2025 гг. – реализуется введение ассоциированных препаратов, планируется ликвидация дифтерии, краснухи, кори, гемофильной инфекции, паротита.
Масштабный охват вызывает некоторые опасения со стороны населения, среди молодых родителей, опасающихся мельчайших признаков нездоровья ребенка. Следует помнить, что средства, формирующие иммунитет, защитят от специфичных заболеваний, предотвратят осложнения, патологические изменения, смерть при инфицировании в ситуациях отказа от прививки. Даже здоровый образ жизни не способен обезопасить организм от воздействия вирусов, бактерий.
В случаях заражения после прививки, например при ненадлежащем хранении средства, нарушениях введения препарата, болезнь протекает легко и без последствий, благодаря наличию иммунитета. Плановая вакцинация экономически оправдана, так как лечение в случае инфицирования потребует больше средств, чем стоимость вакцины.
Видео: сроки формирования БЦЖ
Источник
