Защитная функция крови виды иммунитета
Организм защищается от болезнетворных агентов с помощью неспецифических и специфических защитных механизмов. Одним из них являются барьеры, т.е. кожа и эпителий различных органов (ЖКТ, легких, почек и т.д.). Кроме этого, в крови и лимфе имеются неспецифические клеточные и гуморальные механизмы. Эти механизмы способны обезвреживают даже факторы, с которыми организм раньше не сталкивался. К неспецифическим защитным механизмам крови относятся неспецифический клеточный и гуморальный иммунитет. Неспецифический клеточный иммунитет обусловлен фагоцитарной активностью гранулоцитов, моноцитов, лимфоцитов и тромбоцитов. Неспецифический гуморальный иммунитет связан с наличием в крови и других жидкостях организма естественных антител и ряда белковых систем. Раньше считали, что естественные антитела образуются в организме без контакта с антигеном. Однако сейчас установлено, что они не синтезируются самопроизвольно. Они возникают в результате контакта организма с облигатной кишечной микрофлорой, т.е. иммунной реакции. Имеется и несколько защитных белковых комплексов.
1. Лизоцим. Белок, обладающий ферментативной активностью и подавляющий развитие бактерии и вирусов. Он содержится в гранулах гранулоцитов и макрофагах легких. При их разрушении выделяется в окружающую среду. Лизоцим имеется в слезной жидкости, слизи носа и кишечника.
2. Пропердин. Комплекс белковоподобных веществ. Участвует в лизисе бактерий.
3. Система комплемента. Комплекс 1 1 белков плазмы, активирующийся при иммунологических реакциях. Совместно с пропердином участвует в лизисе бактерий.
4. Интерферон. Белок, вырабатываемый многими клетками при поступлении в них вирусов. Начинает выделяться в кровь до появления иммунных антител. Препятствует выработке рибосомами пораженных клеток вирусного белка.
5. Лейкины. Выделяются лейкоцитами.
6. Плакины. Продукт тромбоцитов. Те и другие разрушают микроорганизмы. Специфические защитные механизмы включают специфический клеточный и гуморальный иммунитет. Специфический клеточный иммунитет обеспечивают Т-лимфоциты. Лимфоциты, образующиеся из стволовых лимфоидных клеток костного мозга, поступают в тимус и превращаются в иммунокомпетентные Т-лимфоциты. Затем эти лимфоциты переходят в кровь. При контакте с антигеном часть Т-лимфоцитов пролиферирует. Одна часть образовавшихся дочерних клеток связывается с антигеном (бактериями) и разрушает его. Для этой реакции антиген-антитело необходимо участие Т-хелперов. Другая часть дочерних клеток преобразуется в Т-клетки иммунологической памяти, которые запоминают структуру антигена. Они смеют большую продолжительность жизни. При повторном контакте Т-клеток памяти с этим антигеном они узнают его. Начинается их интенсивная пролиферация, с образованием большого количества Т-киллеров, а также Т-супрессоров. Т-супрессоры подавляют выработку антител В-лимфоцитами в этот момент. Этот вторичный клеточный иммунный ответ развивается примерно через 48 часов и называется иммунным ответом замедленного типа Так как раньше него возникает вторичный гуморальный иммунный ответ. Примером такой иммунной реакции является покраснение и отек кожи в результате контакта с некоторыми веществами, например краской урсолом.
Специфический гуморальный иммунитет обеспечивается В-лимфоцитами. Они превращаются в иммунокомпетентные клетки в лимфатических узлах тонкого кишечника, миндалинах, аппендиксе. Затем В-лимфоциты выходят в кровь и разносятся ею в селезенку и лимфатические узлы лимфатического русла. При первом контакте с антигеном они пролиферируют. Это явление называется начальной активацией или сенсибилизацией. Одна часть образующихся дочерних клеток превращается в клетки памяти и покидает центры размножения. Другая часть лимфоцитов оседает в лимфатических узлах, превращаясь в плазматические клетки. Эти клетки вырабатывают гуморальные антитела,
поступающие в кровь. Выработку иммуноглобулинов стимулируют Т-хелперы. Многие иммуноглобулины очень длительно сохраняются в крови. При повторном контакте антител с антигеном развивается быстрая и сильная иммунная реакция. Поэтому их называют иммунными реакциями немедленного типа. Они наблюдаются при гемотрансфузионном шоке, аллергии, бронхиальной астме и т.д.
В медицине, для формирования специфического иммунитета, используется вакцинация. При пересадке органов наоборот с помощью иммунодепрессантов определенные звенья иммунитета подавляются. Это предотвращает отторжение трансплантата.
ФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ
Кровообращение это процесс движения крови по сосудистому руслу, обеспечивающий выполнение ею своих функций. Физиологическую систему кровообращения составляют сердце и сосуды. Сердце обеспечивает энергетические потребности системы, а сосуды являются кровеносным руслом. В минуту сердце перекачивает около 5 литров крови, за год 260 тонн, а в течение жизни около 200.000 тонн крови. Суммарная длина сосудов около 100.000 км.
Первое научное исследование системы произвел У.Гарвей. В 1623 году он опубликовал работу «Анатомическое исследование о движении сердца и крови у животных». В 1653- году монах М.Серве описал малый круг кровообращения, а 1628г. Мальпиги под микроскопом обнаружил капилляры. Большой круг кровообращения начинается аортой, отходящей от левого желудочка. По мере удаления от сердца она делится на артерии большого, среднего и малого калибра, артериолы, прекапилляры, капилляры. Капилляры соединяются в посткапиллярные венулы, затем вены. Заканчивается большой круг полыми венами, впадающими в правое предсердие. Малый круг кровообращения начинается легочной артерией, отходящей от правого желудочка. Она также разветвляется на артерии, артериолы и капилляры, пронизывающие легкие. Капилляры объединяются в венулы и легочные вены. Последние впадают в левое предсердие. Сердце — это полый мышечный орган. Его вес составляет 200—00 грамм или 1/200 массы тела. Стенка сердца образована тремя слоями: эндокардом, миокардом и эпикардом. Наибольшую толщину 10-15 мм она имеет* в области левого желудочка. Толщина стенки правого — 5-8 мм, а предсердий 2-3 мм. Миокард состоит из мышечных клеток 3-х типов: сократительных и атипических. Большую часть составляют сократительные кардиомиоциты. Сердце разделено перегородками на 4 камеры: 2 предсердия и 2 желудочка. Предсердия соединяются с желудочками посредством атриовентрикулярных отверстий. В них находятся створчатые атриовентрикулярные клапаны. Правый клапан трехстворчатый (трикуспидальный), а левый двухстворчатый (митральный). К створкам клапанов присочиняются сухожильные нити. Другим концом эти нити соединены сосочковыми (папиллярными) мышцами. В начале систолы желудочков эти мышцы сокращаются и нити натягиваются. Благодаря этому не происходит выворота створок клапанов в полость предсердий и обратного движения крови регургитации. В местах выхода аорты, и лёгочной артерии из желудочков расположены аортальный и пульмональный клапаны. Они имеют вид карманов а форме полумесяцев. Поэтому их называют полулунными. Функцией клапанного аппарата сердца является обеспечение одностороннего тока крови по кругам кровообращения. В клинике функция клапанного аппарата исследуется такими косвенными методами, как аускультация, фонокардиографня, рентгенография, эхокардиография позволяет визуально наблюдать за деятельностью клапанов.
Источник
Состав крови
Кровеносная, она же сердечно-сосудистая система обеспечивает циркуляцию крови и лимфы в организме человека. Среди всех органов тела только поверхность глаз может получать кислород непосредственно из воздуха. Все остальные органы и ткани, даже кожа, получают кислород с током крови.
Кровь относится к соединительной ткани, клетки в ней занимают гораздо меньший объем, чем межклеточное вещество. Кровь состоит из жидкости с растворенными веществами (плазмы) и форменных элементов: лейкоцитов, эритроцитов и тромбоцитов. Плазма крови образует внутреннюю среду организма: жидкость из крови «выдавливается» в ткани и становится тканевой жидкостью, избыток тканевой жидкости попадает в лимфатические сосуды, становясь лимфой. Лимфа в итоге попадает в кровоток, возвращая жидкость в кровь.
Плазма крови содержит 0,9% хлорида натрия (поваренная соль), поэтому для внутривенных вливаний используют водный 0,9% раствор NaCl («физиологический», или изотонический раствор). Другие соли и органические вещества в сумме занимают около 9% массы плазмы. Большую роль играют белки плазмы, особенно альбумины.
Для поддержания постоянной кислотности в плазме присутствуют буферные системы. Водородный показатель крови человека (pH) в среднем равен 7,4. При его смещении в кислотную или основную сторону происходят химические реакции в буферных системах, которые уравновешивают изменения кислотности.
Поддерживать постоянство внутренней среды (гемостаз) необходимо для нормальной жизни клеток. Клеточная мембрана проницаема для молекул воды, поэтому если снаружи концентрация раствора повышается (гипертонический раствор), вода стремится выйти из клетки по закону осморегуляции. Клетка при этом скукоживается, становится неправильной формы, многие ее органеллы перестают правильно работать.
Если же концентрация соли в окружающем растворе слишком мала (гипотонический раствор), вода стремится внутри клетки, чтобы «разбавить» ее содержимое. В этом случае клетки разбухают, мембрана может не выдержать и лопнуть. Таким образом, изменение солености крови может привести к необратимым изменениям в организме.
Клетки составляют около 45% объема крови. Выделяют «белую» кровь – лейкоциты и «красную» кровь – эритроциты. Эритроциты имеют небольшой размер и двояковогнутую дисковидную форму. Такая форма дает большую площадь поверхности при минимальном объеме, что повышает эффективность газообмена. Эритроциты человека не имеют ядра, они теряют его в процессе созревания.
Эритроциты
В 1 мл крови содержится 4-6 млн эритроцитов. Их главная функция – перенос кислорода, за это отвечает крупный белок – гемоглобин. Одна молекула гемоглобина состоит из четырех полипептидных цепей (глобина) и железосодержащих групп (гема). Каждая молекула гемоглобина может перенести четыре молекулы кислорода, причем способность связывать и отдавать кислород зависит от условий среды: в более щелочной среде (легких) гемоглобин лучше связывает кислород, в то время как в более кислой среде (тканях), он лучше отдает его.
Механизм действия гемоглобина
Помимо кислорода с гемоглобином могут связываться другие газы, самым опасным из которых является угарный (СО). Он образуется при неполном сгорании органики в условиях нехватки кислорода и не имеет цвета и запаха. Сродство гемоглобина к угарному газу гораздо выше, чем к кислороду, поэтому, однажды связавшись с гемоглобином, угарный газ будет еще долго циркулировать в крови. При этом свободных сайтов связывания кислорода станет меньше и ткани начнут страдать от его нехватки. Тяжелое отравление угарным газом требует немедленной специализированной помощи.
Лейкоциты
Лейкоциты являются основой клеточного иммунитета, это сферические клетки с достаточно крупным ядром. 1 мл крови содержит 4-11 тысяч лейкоцитов. Из всех клеток организма они наиболее уязвимы к действию радиации.
В зависимости от свойств лейкоциты делятся на несколько типов: содержащие гранулы, или гранулоциты (эозинофилы, нейтрофилы, базофилы) и не содержащие – агранулоциты.
Тромбоциты
Также кровь содержит тромбоциты, которые представляют собой отшнуровавшиеся куски гигантской клетки. Сами тромбоциты клетками не являются, они выглядят как мелкие пластинки неправильной формы и содержат только цитоплазму с гранулами. В гранулах находятся ферменты свертывающей системы, которые активируются при повреждении сосуда: образуется сгусток крови (тромб), который закупоривает поврежденный участок. 1 мл крови содержит 200-500 тысяч тромбоцитов.
Начало всем форменным элементам крови дают стволовые клетки красного костного мозга. Клетки крови постоянно обновляются, но у разных типов клеток обновление происходит с разной периодичностью. Эритроциты могут циркулировать 120-130 суток, в то время как лейкоциты и тромбоциты обычно живут не дольше 5-7 суток.
Иммунитет
Иммунная система защищает организм от воздействия бактерий, вирусов, грибов и паразитов, вредных веществ. В случае сбоя в работе иммунитета могут возникать аутоиммунные заболевания, в организме человека есть несколько механизмов, чтобы их предотвратить.
Органы, участвующие в формировании иммунитета
Основными органами иммунной системы являются селезенка, тимус (вилочковая железа) и костный мозг, где появляются и начинают созревать иммунные клетки. Клетки иммунитета циркулируют с кровью, располагаются в лимфоузлах и тканях, особенно много их в местах контакта с внешней средой (кожа, ЖКТ, дыхательные пути). Некоторые органы защищены от иммунного ответа барьерами, они называются иммунологически привилегированными органами. Это мозг, камеры глаза, семенники, плацента и плод и т.д. При травмах иммунологически привилегированных органов, когда нарушается целостность барьера, могут возникнуть аутоиммунные реакции.
Макрофаги
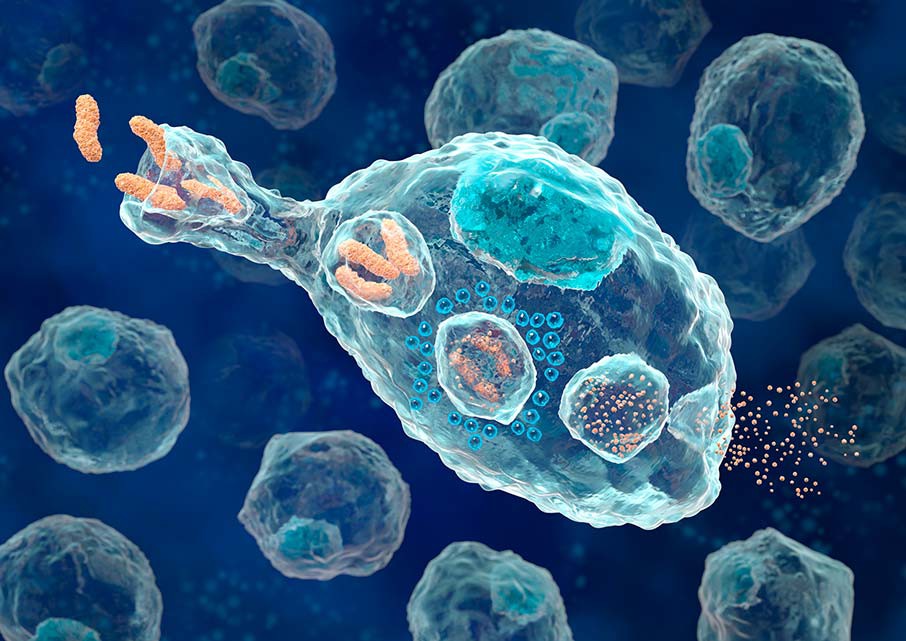
Другие клетки неспецифического иммунитета, которые первыми отвечают на воздействие, – макрофаги. Это крупные клетки, которые способны к активному передвижению и фагоцитозу, они пожирают бактерии и инородные тела. Самостоятельно распознавать чужеродные белки макрофаги не способны, их действие не избирательно. «Ориентируют» макрофагов на уничтожение конкретных клеток антитела.
Макрофаг, фагоцитирующий бактерии.
Другими клетками иммунитета являются нейтрофилы и эозинофилы. Они, как и макрофаги, являются фагоцитами (то есть способны к фагоцитозу). Кроме того, в их цитоплазме есть гранулы с едкими веществами, которые высвобождаются при активации клетки. Запускается каскад химических реакций, в ходе которых образуются активные формы кислорода, это называется кислородным взрывом. Нейтрофилы и эозинофилы, а также окружающие здоровые клетки тоже погибают в результате кислородного взрыва, их остатки фагоцитируют макрофаги. Эозинофилы играют основную роль в развитии аллергий.
Нейтрофил, эозинофил, базофил
Фагоциты способны к направленному движению (хемотаксису), их можно обнаружить во многих тканях и органах, даже на поверхности кожи. Благодаря их постоянной активности большая часть атакующих агентов не вызывает инфекции, то есть системного ответа организма. Инфекция возникает в том случае, если иммунитет ослаблен (переутомление, переохлаждение, голодание и т.д.) или если инфекционный агент не был вовремя распознан фагоцитами.
Различают два вида иммунитета: клеточный и гуморальный. Гуморальный иммунитет – это система комплемента и циркулирующие с плазмой крупные молекулы – антитела. Белки системы комплемента «помечают» чужеродные агенты, вызывая направленное движение клеток иммунитета. Также система комплемента может формировать поры в мембране бактерий, что будет вести к их разрушению.
Антитела
Каждое антитело имеет на конце вариабельные домены (участки), комплементарные к чужеродному белку и специфические для конкретного возбудителя. Они прикрепляются к комплементарным участкам белков, «помечая» их для других клеток иммунного ответа, например, для фагоцитов. Также антитела могут слипаться между собой, что вызывает агглютинацию возбудителя. Особенно эффективны антитела против бактерий.
На рисунке изображены молекулы антител. Каждая состоит из двух пар цепей, синим цветом нарисованы тяжелые цепи, коричневым – легкие.
Клеточный иммунитет состоит из Т и В-лимофцитов. Т-лимофоциты могут быть двух видов: Т-хелперы и Т-киллеры. Т-киллеры клетки-убийцы, они запускают процессы апоптоза, то есть запрограммированной гибели клеток, их самоуничтожения. Это необходимо, если клетки организма заражены вирусами или бактериями или если при делении в геноме появились мутации (то есть Т-киллеры борются также с раковыми клетками).
В-лимфоциты синтезируют антитела и таким образом управляют гуморальным иммунитетом. При миграции В-клеток из крови в ткань они дифференцируются в плазматические клетки.
Лимфоциты действуют избирательно, они «настроены» на уничтожение возбудителя с конкретными антигенами. Чтобы правильно «настроить» лимфоциты, нужны антиген-презентирующие клетки (АПК). АПК фагоцитируют чужеродных агентов и выставляют на своей поверхности участки их молекул в комплексе с МНС II (главный комплекс гистосовместимости II). Т-хелперы способны распознавать чужие молекулы на поверхности АПК и активировать иммунный ответ.
Специфический иммунитет очень эффективен, но требует времени на развертывание. От попадания возбудителя в кровь до выработки антител может пройти несколько дней.
К неспецифическому иммунитету относят в основном фагоциты, которые пытаются поглотить или разрушить любое инородное тело или подозрительную клетку, которую встречают.
Немаловажную роль в иммунной защите организма играет воспаление. Это сложный стадийный процесс, который имеет следующие признаки: отек, местное повышение температуры, покраснение, боль и утрата функции органа. Благодаря отеку затрудняется распространение возбудителей по организму, место проникновения ограничивается. При повышении температуры повышается активность некоторых белков гуморального иммунитета, в то время как активность бактерий и скорость их размножения снижаются. Воспалительный процесс особенно эффективен против паразитов.
N-киллеры (натуральные киллеры), как и Т-киллеры могут запускать процессы клеточной гибели. Однако они, в отличии от Т-клеток, не требуют специальной подготовки – презентации антигена и активации. N-киллеры хорошо борются с опухолями.
Интерфероны – белки крови, которые составляют основу противовирусного гуморального иммунитета. Вирусы проникают в клетки организма, после чего здоровые клетки перестают синтезировать необходимые белки и начинают воспроизводить белки и генетическую информацию вирусов. Чтобы остановить распространение вирусных частиц и выиграть время на формирование специфического иммунитета, интерфероны замедляют или даже останавливают синтез белка в зараженных клетках.
Неспецифический иммунитет не требует времени на развертывание, его действие начинается уже в первые минуты после воздействия. Однако и точность неспецифического иммунитета низкая, при развитии иммунного ответа могут страдать здоровые клетки.
Синтез клеток специфического иммунитета (лимфоцитов) включает в себя элемент случайности, только так можно достигнуть неимоверного разнообразия иммунных клеток. Чтобы в кровоток не выходили клетки, которые способны атаковать собственный организм, они проходят строгий отбор в органах иммунной системы, где происходит созревание лимфоцитов (тимус, лимфоузлы). Если в результате отбора оказывается, что юный лимфоцит распознает клетки своего организма в качестве «врагов», в нем запускается процесс апоптоза, самоуничтожения.
Группы крови. Гемотрансфузия.
На поверхности эритроцитов могут находиться белки-агглютиногены А и В. В зависимости от того, какие агглютиногены есть в организме, выделяют: I группу крови (без агглютиногенов), II (только А), III (только В) и IV (оба агглютиногена).
При гемотрансфузии (переливании крови) необходимо учитывать группу, чтобы избежать возникновения иммунного конфликта. Если человеку с I группой крови перелить любую другую, клетки его иммунитета распознают чужеродные белки-агглютиногены и выработают антитела. В результате все чужие эритроциты «слипнутся» (агглютинируют), что может быть очень опасно для организма хозяина. Поэтому людям с I группой крови можно переливать только кровь такой же группы.
Если же перелить кому-нибудь эритроциты I группы крови, не имеющие белков-агглютиногенов, реакции иммунитета не последует. Можно сказать, что обладатели I группы самые «щедрые», потому что могут поделиться своей кровью со всеми. Также их называют универсальными донорами.
Обратная ситуация с IV группой: в крови таких людей нет антител ни к агглютиногену А, ни к агглютиногену В, поэтому им можно перелить кровь любой группы. Однако при попадании эритроцита группы IV в организм с другой группой произойдет агглютинация, поэтому обладателей IV группы крови можно назвать самыми «жадными» или универсальными реципиентами. Соответственно, II группу крови нельзя перелить обладателю III и наоборот.
Помимо агглютиногенов А и В существует много других белков, которые могут привести к возникновению иммунного конфликта. Международное общество трансфузиологов в настоящее время признает всего 36 систем деления крови на группы. Наиболее часто применяют систему АВО, в которой также учитывают резус-фактор. Впервые этот белок был описан у макак-резусов, за что и получил свое название.
Большая часть людей резус-положительна (Rh+), то есть имеет на эритроцитах белок-резус. Им можно переливать кровь с любым резусом. Людям же с резус-отрицательной кровью (Rh-) можно переливать только резус-отрицательную кровь.
Резус-фактор может стать причиной резус-конфликта между матерью и плодом. Если у резус-отрицательной матери будет резус-положительный ребенок, то при попадании крови плода в кровоток матери сформируются антитела к Rh+ белку. Чаще всего смешение крови происходит при родах и не несет опасности для ребенка. Если же антитела каким-то образом появились до родов, они могут проникнуть через плаценту и вызвать агглютинацию эритроцитов плода, что приведет к его гибели. Такая опасность часто возникает при повторной беременности резус-отрицательных женщин.
Распространенность групп крови варьирует в разных популяциях. На картинке приведена частота встречаемость разных групп по системе АВО в мире.
Распространенность групп крови
Источник
