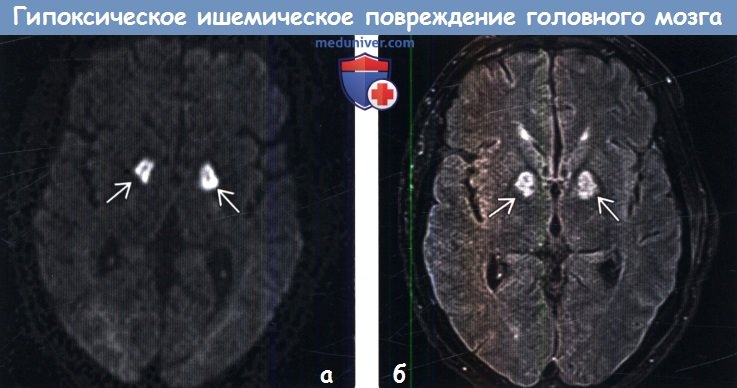
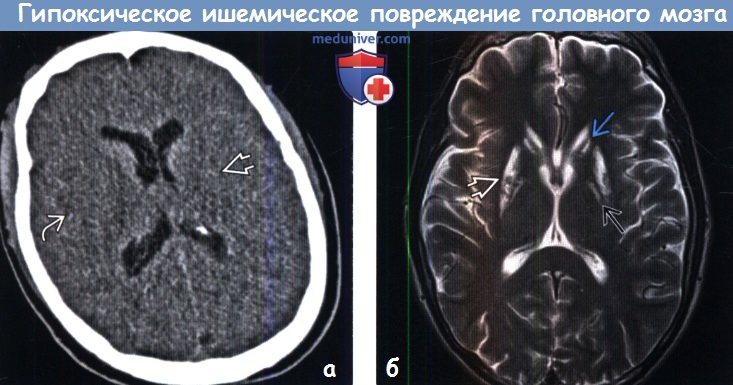
Аноксическое поражение головного мозга на мрт
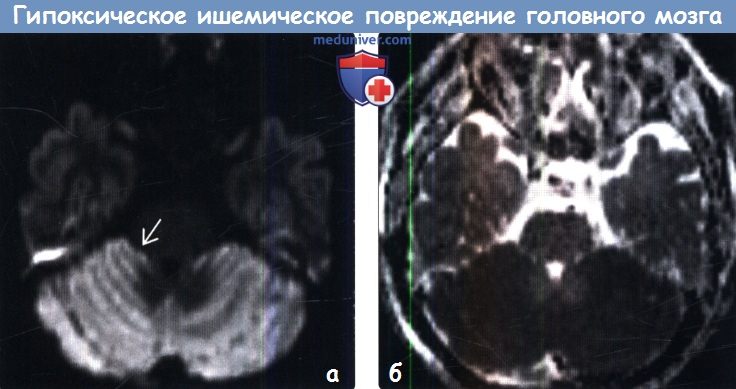
Диагностика гипоксического ишемического повреждения головного мозга у взрослых по МРТа) Терминология: б) Визуализация: 1. Общие характеристики гипоксического ишемического повреждения головного мозга у взрослых: 2. КТ при гипоксическом ишемическом повреждении головного мозга у взрослых:
3. МРТ при гипоксическом ишемическом повреждении головного мозга у взрослых: 4. Рекомендации по визуализации:
в) Дифференциальная диагностика: 1. Ишемия-инфаркт мозговой ткани в острой стадии: 2. Травматический отек головного мозга: 3. Токсическая/метаболическая энцефалопатия: 4. Гипертензивная энцефалопатия, СЗОЭ: 5. Болезнь Крейтцфельдта-Якоба (БКЯ): 6. Синдром MELAS: г) Патология: 1. Стадирование и классификация гипоксического ишемического повреждения головного мозга у взрослых: д) Клиническая картина гипоксического ишемического повреждения головного мозга у взрослых: 1. Проявления: 2. Течение и прогноз: 3. Лечение: е) Диагностическая памятка: ж) Список литературы:
— Также рекомендуем «Гипотензивный инфаркт головного мозга на МРТ» Редактор: Искандер Милевски. Дата публикации: 20.3.2019 |
Неврология
09.05.2019
Аноксическое поражение головного мозга происходит по причине острого кислородного голодания, длящегося 60-240 секунд, или более длительный период.
Прекращение оксигенации провоцирует гибель церебральных нейронов уже через 3-5 минут. В поврежденных мозговых структурах возникают ишемические очаги и небольшие кровоизлияния, провоцирующие отек.
Нарастающий отек ведет к сдавливанию тканей, отмиранию нервных клеток, нарушению работы внутренних органов. Без своевременной терапии часто заканчивается смертельным исходом.
Что это такое и почему возникает?
 Аноксия обусловлена недостаточной оксигенацией церебральных нейронов. В условиях гипоксии органеллы нейронов не способны выполнять свои функции, что приводит структурным изменениям и гибели клеток. Массовая гибель нейроцитов способствует образованию некротических очагов в ЦНС.
Аноксия обусловлена недостаточной оксигенацией церебральных нейронов. В условиях гипоксии органеллы нейронов не способны выполнять свои функции, что приводит структурным изменениям и гибели клеток. Массовая гибель нейроцитов способствует образованию некротических очагов в ЦНС.
К причинам патологии у детей и у взрослых относят:
- тромбоэмболию легочной артерии или артериол головного мозга;
- удушение;
- утопление;
- расстройства дыхания;
- остановка сердцебиения;
- токсические повреждения ЦНС;
- воздействие электротока;
- инфекционные поражения мозговых структур и т.д.
Аноксическое состояние плода или младенца в перинатальный период провоцируют:
- Патологии беременности – болезни внутренних органов матери, гестозы, маточные кровотечения, интоксикации и пр.
- Родовые аномалии – преждевременная отслойка детского места, плацентарное предлежание, обвитие пуповиной, преждевременные роды, перенашивание плода, недостаточность родовой деятельности.
- Послеродовые патологические состояния – апноэ новорожденного, гемолитическая болезнь, синдром аспирации мекония, инфекции.
Указанные факторы способствуют ишемическому повреждению нервной ткани. Рефлекторная реакция кровеносных сосудов подразумевает увеличение проницаемости сосудистых стенок, что с одной стороны препятствует адекватному кровоснабжению, а другой, становится причиной развития отека мозга. Чем дольше длится это состояние, тем глубже тканевые повреждения.
Снижение оксигенации нервной ткани приводит к метаболическим нарушениям с образованием ацидных соединений, оказывающих раздражающее действие на центры дыхания и пищеварения в ЦНС.
Классификация
В зависимости от морфологических изменений различают следующие формы аноксического поражения:
- аноксическая (связанная с прекращением или недостаточностью дыхания);
- анемическая (развивается вследствие недостаточного кровоснабжения мозговых тканей);
- застойная (связанная с гемодинамическими нарушениями);
- метаболическая (возникает при серьезных нарушениях обменных процессов).
Церебральное аноксическое поражение бывает острым (отличается внезапным и стремительным развитием) или хроническим (когда происходит постепенное снижение оксигенации).
По длительности отсутствия поступления кислорода аноксия бывает:
- легкой – отсутствие кислорода ограничивается полутора минутами;
- умеренной – оксигенация отсутствует до трех минут;
- тяжелой – гипоксия сохраняется до четырех минут и более.
По международной классификации аноксическое поражение головного мозга мкб 10 зарегистрировано под кодами G 93.1 и P21.9.
Симптомы
 Симптоматика определяется этиологическими факторами и длительностью отсутствия кислородного снабжения тканей.
Симптоматика определяется этиологическими факторами и длительностью отсутствия кислородного снабжения тканей.
При острой форме патологии наблюдается:
- помрачение или потеря сознания;
- цианоз кожи и слизистых оболочек;
- нарушение дыхания и сердечной деятельности;
- тремор конечностей и головы;
- судороги.
Если поступление кислорода не было восстановление, у человека развивается агония или кома, которая заканчивается летальным исходом. Если человек выходит из коматозного состояния после длительной аноксии, у него может развиться апаллический синдром.
Хроническая форма характеризуется:
- эпилепсией;
- тремором рук и головы;
- изменением чувствительности кожных покровов;
- нарушением зрительной функции и слуха;
- головокружениями и краниалгиями;
- парезами или параличами конечностей;
- повышенной чувствительностью к световым и звуковым раздражителям.
При тяжелых и умеренных проявлениях недуга у пациентов наблюдается потеря памяти. Долгосрочные последствия включают парезы и параличи групп мышц или конечностей, когнитивную дисфункцию, снижение концентрации внимания, шаткость походки, приступы эпилепсии.
Диагностика
Для постановки диагноза врач собирает анамнез больного, осматривает его, назначает проведение анализов и направляет на обследование при помощи специальных методов.
Для выявления степени повреждения мозговых структур применяют:
- КТ или МРТ – методы, позволяющие при помощи рентгеновских лучей или магнитных волн получить подробное изображение церебральных тканей, наличие участков некроза и других поражений.
- Электроэнцефалограмма – необходима для измерения электрической активности различных зон головного мозга.
- ОЭКТ – эмиссионная томография дающая возможность получить трехмерное изображение мозга.
Результаты обследований помогают врачу оценить степень аноксическго поражения головного мозга у детей и у взрослых, сделать прогноз течения заболевания, а также назначить оптимальные терапевтические схемы.
Лечение
Терапевтические мероприятия по устранению недуга рассчитаны на несколько этапов. В первую очередь необходимо устранить факторы, препятствующие нормальной оксигенации центральной нервной системы. В зависимости от причины это может быть:
- устранение инородного тела или жидкости из дыхательных путей;
- восстановление сердечной деятельности и дыхания;
- выведение токсических веществ из организма;
- прекращение воздействия электротока и т.д.
После устранения причины аноксии необходимо восстановить жизненно-важные функции – дыхание, кровообращение, сердечный ритм. После этого лечение назначается в зависимости от повреждений, спровоцированных отсутствием кислородного снабжения мозговых структур.
Реабилитация
Реабилитационные мероприятия проводятся с целью восстановления утерянных функций и навыков. При серьезных расстройствах важно, чтобы близкие больного принимали непосредственное участие в реабилитации.
Двигательные расстройства подразумевают посещение физиотерапевтических процедур. Показана электротерапия, дарсонвализация, магнитотерапия, электростатический массаж, акупунктура, бальнеотерапия. Такие мероприятия позволяют улучшить нервную проводимость, укрепить мускулатуру, наладить двигательную активность.
При выраженной гипоксии назначают оксигенобаротерапию в специальных барокамерах. Такой вид физиотерапии улучшает оксигенацию тканей и восстанавливает гемодинамику в мозговых структурах. Если состояние больного удовлетворительное, показана лечебная физкультура и массаж.
Проблемы с речью требуют вмешательства логопеда, а при нестабильном эмоциональном состоянии с больным должен работать психотерапевт или психолог.
Пациенты с тяжелой степенью аноксии не способны самостоятельно себя обслужить. Таким людям требуются занятия с трудотерапевтом, который поможет восстановить навыки, необходимые в повседневной жизни – прием пищи, одевание, личная гигиена.
Прием лекарств
Лекарственные средства применяют при острой аноксии для восстановления жизненно-важных функций и устранения церебрального отека. Применяют препараты, стимулирующие дыхание, сердечную деятельность, кровообращение. При интоксикациях используют антидоты ядовитых веществ, сорбенты и инфузионные растворы. Для снятия отека показано введение диуретиков, выводящих из организма лишнюю жидкость.
После устранения острых симптомов проводят симптоматическую терапию, а также применяют лекарственные средства, улучшающие церебральную микроциркуляцию.
При краниалгиях применяют анальгезирующие препараты (ибупрофен, анальгин, парацетамол). В случае появления судорог назначают Клоназепам. Если аноксия осложняется эпилептическими пароксизмами, показаны средства, снижающие их частоту и интенсивность. Для укрепления нервной системы рекомендуется принимать препараты витаминов группы В, магния, аминокислоту глицин.
Профилактика
Учитывая, что аноксическое поражение головного мозга у новорожденных результат внутриутробных патологий или родовых травм, беременным женщинам важно своевременно проходить ультразвуковую диагностику и скриниговые тесты.
Следует отказаться от вредных привычек и работы с токсическими веществами еще на этапе планирования беременности.
Снизить риски аноксии головного мозга помогут следующие рекомендации:
- во время приема пищи не разговаривайте и тщательно пережевывайте еду;
- не нарушайте правила поведения на воде;
- не оставляйте без присмотра маленьких детей, не позволяйте им играть мелкими предметами, которые легко вдохнуть;
- откажитесь от курения, употребления наркотиков, злоупотребления алкогольными напитками;
- избегайте контакта с ядовитыми веществами;
- осуществляйте регулярную проверку печного и газового оборудования во избежание утечек угарного газа;
- соблюдайте осторожность при использовании или ремонте электроприборов, проводки, выключателей и других потенциально опасных устройств.