Что такое комплимент иммунитета

Система комплемента, состоящая примерно из 30 белков, как циркулирующих, так и экспрессированных на мембране, является важной эффекторной ветвью как врожденного, так и опосредованного антителами приобретенного иммунного ответов. Термин «комлемент» появился в связи с тем, что этот чувствительный к повышению температуры материал сыворотки крови был обнаружен по свойству «дополнять» способность антител уничтожать бактерии. Известно, что комплемент играет главную роль в защите от многих инфекционных микроорганизмов.
Наиболее важными составляющими его защитной функции являются: 1) выработка опсонинов — молекул, увеличивающих способность макрофагов и нейтрофилов к фагоцитозу; 2) выработка анафилатоксинов — пептидов, индуцирующих местные и системные воспалительные реакции; 3) непосредственный киллинг микроорганизмов.
Известны и другие важные функции комплемента, такие как усиление антигенспецифических иммунных ответов и поддержание гомеостаза (стабильности внутри организма) путем удаления иммунных комплексов и мертвых или умирающих клеток. Мы знаем также, что нарушение контроля над активацией комплемента может привести к повреждению клеток и тканей организма.
Компоненты комплемента синтезируются в печени, а также клетками, участвующими в воспалительной реакции. Концентрация всех белков комплемента в циркулирующей крови составляет примерно 3 мг/мл. (Для сравнения: концентрация IgG в крови составляет примерно 12 мг/мл) Концентрации некоторых компонентов комплемента высоки (например, около 1 мг/мл для С3), в то время как другие компоненты (такие как фактор D и С2) присутствуют в следовых количествах.
Пути активации комплемента
Начальные этапы активации комплемента заключаются в последовательной каскадной активации одного за другим его компонентов. На этой стадии активация одного компонента индуцирует действие фермента, которое приводит к активации следующего по очереди компонента. Поскольку одна активная молекула фермента способна расщеплять множество молекул субстрата, этот каскад реакций усиливает относительно слабый начальный сигнал. Эти каскадные свойства системы комплемента аналогичны наблюдаемым в других сывороточных каскадах, направленных на образование сгустка и выработку кининов, сосудистых медиаторов воспаления.
После активации отдельные компоненты расщепляются на фрагменты, обозначаемые строчными буквами. Меньший из расщепленных фрагментов обычно обозначается буквой «а», больший — «b». Исторически сложилось, однако, что больший из расщепленных фрагментов С2 обычно относят к С2а, а меньший — к С2b. (Однако в некоторых текстах и статьях фрагменты компонентов комплемента С2 обозначаются обратным способом.) Дальнейшие фрагменты расщепления также обозначаются малыми буквами, например C3d.
Известны три пути активации комплемента: классический, лектиновый и альтернативный.
Начало каждого из путей активации характеризуется собственными компонентами и процессами распознавания, однако на более поздних стадиях во всех трех случаях используются одни и те же компоненты. Свойства каждого пути активации и веществ, их активирующих, обсуждаются далее.
Классический путь
Классический путь активации так называется потому, что он был определен первым. Белковые компоненты классического пути обозначаются С1, С2, С9. (Номера расставлены в том порядке, в котором компоненты были открыты, а не в том, в котором они активируются.) Комплексы антиген — антитело являются основными активаторами классического пути. Таким образом, последний является главным эффекторным путем активации гуморального адаптивного иммунного ответа.
Другими активаторами являются некоторые вирусы, погибшие клетки и внутриклеточные мембраны (например, митохондрий), агрегаты иммуноглобулинов и β-амилоид, обнаруживаемый при болезни Альцгеймера в бляшках. С-реактивный белок является белком острой фазы — компонентом воспалительной реакции; он прикрепляется к полисахариду фосфорилхолину, экспрессированному на поверхности многих бактерий (например, Streptococcus pneumoniae), и тоже активирует классический путь.
Классический путь инициируется, когда С1 прикрепляется к антителу в комплексе антиген — антитело, например антителу, связанному с антигеном, экспрессированным на поверхности бактерии (рис. 13.1). Компонент С1 представляет собой комплекс из трех различных белков: Clq (содержащего шесть одинаковых субкомпонентов), связанного с двумя молекулами (причем каждой по две) — Clr и Cls. При активации Cl его глобулярные участки — субкомпоненты Clq — связываются с Clq-специфичным участком на Fc-фрагментах или одного IgM, или двух близко расположенных молекул IgG, связанных с антигеном (связывание IgG показано на рис. 13.1).
Таким образом, антитела IgM и IgG являются эффективными активаторами комплемента. Иммуноглобулины человека, обладающие способностью связываться с Cl и активировать его, в порядке уменьшения этой способности располагаются: IgM > > IgG3 > IgG 1 » IgG2. Иммуноглобулины IgG4, IgD, IgA и IgE не взаимодействуют с Clq не закрепляют и не активируют его, т.е. не активируют комплемент по классическому пути.
После связывания С1 с комплексом антиген—антитело Cls приобретает ферментативную активность. Эта активная форма известна как Cls-эстераза. Она расщепляет следующий компонент классического пути — С4 — на две части: С4а и С4b. Меньшая часть — С4а — остается в растворенном состоянии, а С4b ковалентно связывается с поверхностью бактерии или другой активирующей субстанцией.
Часть С4b, прикрепленная к поверхности клетки, затем связывает С2, который расщепляется Cls. При расщеплении С2 получают фрагмент С2b, который остается в растворенном состоянии, и С2а. В свою очередь С2а прикрепляется к С4b на поверхности клетки с образованием комплекса С4b2а. Этот комплекс называется С3-конвертазой классического пути, поскольку, как мы увидим позднее, этот фермент расщепляет следующий компонент — С3.
Лектиновый путь
Лектиновый путь активируется концевыми остатками маннозы в белках и полисахаридах, находящихся на поверхности бактерии. Эти остатки не обнаруживаются на поверхности клеток млекопитающих, поэтому лектиновый путь может рассматриваться в качестве средства распознавания своего и чужого. Поскольку этот путь активации не требует присутствия антител, он является частью системы врожденной иммунной защиты.
На рис. 13.1 показано, как бактериальные маннозные остатки связываются с циркулирующим комплексом маннозосвязывающего лектина (МСЛ; по структуре схожий с Clq классического пути) и двумя ассоциированными протеазами, называемыми маннозассоциированными сериновыми протеазами (МАСП-1 и -2). Это связывание активирует МАСП-1 для последующего расщепления компонентов классического пути комплемента — С4 и С2 с формированием С4b2а, С3-конвертазы классического пути на поверхности бактерий. А МАСП-2 обладает способностью напрямую расщеплять С3. Таким образом, лектиновый путь после фазы активации С3 аналогичен классическому.
Альтернативный путь
Альтернативный путь активации комплемента запускается почти любой чужеродной субстанцией. К наиболее изученным веществам относятся липополисахариды (ЛПС, также известные как эндотоксины клеточной стенки грамотрицательных бактерий), клеточные стенки некоторых дрожжей и белок, находящийся в яде кобры (фактор яда кобры). Некоторые агенты, активирующие классический путь, — вирусы, агрегаты иммуноглобулинов и мертвые клетки, запускают также и альтернативный путь.
Активация происходит в отсутствие специфических антител. Таким образом, альтернативный путь активации комплемента является эффекторной ветвью системы врожденной иммунной защиты. Некоторые компоненты альтернативного пути характерны только для него (сывороточные факторы В и D и пропердин, известный также как фактор Р), в то время как другие (С3, С3b, С5, С6, С7, С8 и С9) являются общими с классическим путем.
Компонент С3b появляется в крови в небольших количествах после спонтанного расщепления реактивной тиоловой группы в С3. Этот «предсу-ществующий» С3b способен связываться с гидроксильными группами белков и углеводов, экспрессированных на клеточных поверхностях (см. рис. 13.1). Накопление С3b на поверхности клетки инициирует альтернативный путь.
Оно может происходить как на чужеродной, так и на собственной клетке организма; таким образом, с точки зрения альтернативного пути он всегда запущен. Однако, как указано более детально далее, собственные клетки организма регулируют течение реакций альтернативного пути, в то время как чужеродные не обладают такими регуляторными способностями и не могут предотвратить развитие последующих событий альтернативного пути.

Рис. 13.1. Запуск классического, лектинового и альтернативного путей. Демонстрация активации каждого пути и формирования С3-конвертазы
На следующей стадии альтернативного пути сывороточный белок, фактор B, соединяется с С3b на поверхности клетки с формированием комплекса С3bВ. Затем фактор D расщепляет фактор В, который находится на поверхности клетки в комплексе С3bВ, в результате чего образуется фрагмент Ва, который высвобождается в окружающую жидкость, и Вb, остающийся связанным с С3b Этот С3bВb является С3-конвертазой альтернативного пути, которая расщепляет С3 на С3а и С3b.
Обычно С3bВb быстро растворяется, но может стабилизироваться при соединении с пропердином (см. рис. 13.1). В результате стабилизированный пропердином С3bВb способен связываться и расщеплять большое количество С3 за очень короткое время. Накопление на клеточной поверхности этих быстро образованных в большом количестве С3b приводит к почти «взрывному» запуску альтернативного пути. Таким образом, связывание пропердина с С3bВb создает петлю усиления альтернативного пути. Cпособность пропердина активировать петлю усиления контролируется противоположным действием регуляторных белков. Следовательно, активация альтернативного пути не происходит постоянно.
Активация С3 и С5
Расщепление С3 является основной фазой для всех трех путей активации. На рис. 13.2 показано, что С3-конвертазы при классическом и альтернативном путях (С4b2а и С3bВb соответственно) расщепляют С3 на два фрагмента. Более мелкий С3а является растворимым белком анафилатоксином: он активирует клетки, участвующие в реакции воспаления. Больший фрагмент, С3b, продолжает процесс активации каскада комплемента, связываясь с клеточными поверхностями вокруг места активации. Как показано далее, С3b также участвует в защите организма, воспалении и иммунной регуляции.

Рис. 13.2. Расщепление компонента С3 С3-конвертазой и компонента С5 С5-конвертазой при классическом и лектиновом (наверху) и альтернативном (внизу) путях. Во всех случаях С3 расщепляется на С3b, который откладывается на клеточной поверхности, и СЗа, высвобождаемый в жидкую среду. Таким же образом С5 расщепляется на С5b, который откладывается на клеточной поверхности, и С5а, высвобождаемый в жидкую среду
Связывание С3b с С3-конвертазами как при классическом, так и альтернативном путях инициирует связывание и расщепление следующего компонента — С5 (см. рис. 13.2). По этой причине С3-конвертазы, связанные с С3b, относятся к С5-конвертазам (С4b2а3b при классическом пути; С3bВb3b при альтернативном). При расщеплении С5 образуются два фрагмента. Фрагмент С5а высвобождается в растворимой форме и является активным анафилатоксином. Фрагмент С5b связывается с клеточной поверхностью и формирует ядро для связи с терминальными компонентами комплемента.
Терминальный путь
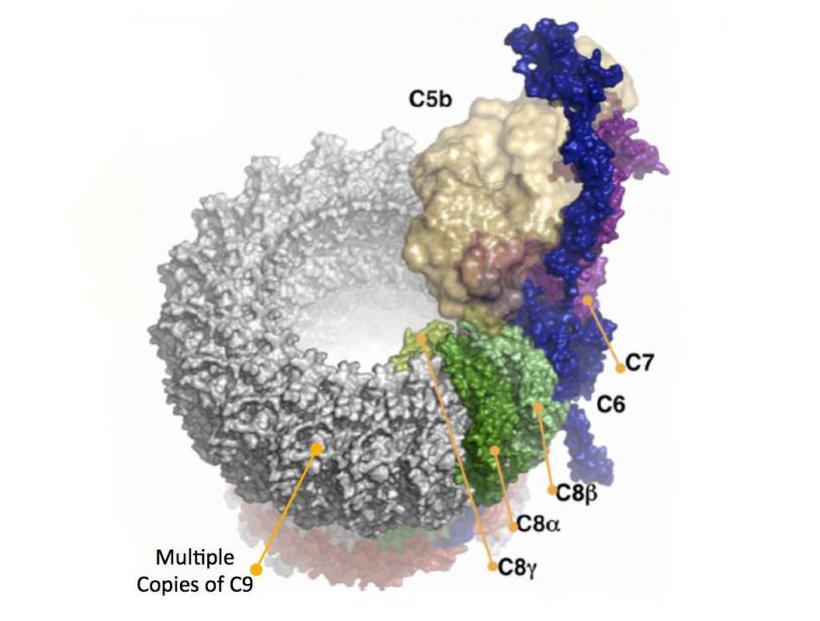
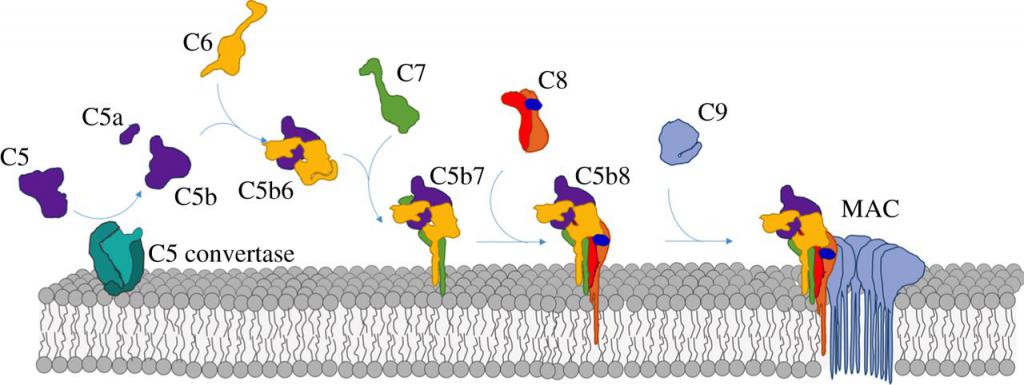
Терминальные компоненты каскада комплемента — С5b, С6, С7, С8 и С9 — являются общими для всех путей активации. Они связываются друг с другом и формируют мембраноатакующий комплекс (МАК), который вызывает лизис клетки (рис. 13.3).

Рис. 13.3 Формирование мембраноатакующего комплекса. Компоненты комплемента поздней фазы — С5b-С9 — последовательно соединяются и формируют на поверхности клетки комплекс. Многочисленные С9-компоненты прикрепляются к этому комплексу и полимеризуются с образованием поли-С9, создавая канал, который пронизывает клеточную мембрану
Первой фазой формирования МАК является прикрепление С6 к С5b на поверхности клетки. Затем С7 связывается с С5b и С6 и проникает в наружную мембрану клетки. Последующее связывание С8 с С5b67 приводит к образованию комплекса, глубже проникающего в мембрану клетки. На мембране клетки C5b—С8 действует как рецептор для С9 — молекулы типа перфорина, который связывается с С8.
Дополнительные молекулы С9 взаимодействуют в комплексе с молекулой С9, образуя полимеризованные С9 (поли-С9). Эти поли-С9 формируют трансмембранный канал, нарушающий осмотическое равновесие в клетке: через него проникают ионы и поступает вода. Клетка набухает, мембрана становится проницаемой для макромолекул, которые затем покидают клетку. В результате происходит лизис клетки.
Р.Койко, Д.Саншайн, Э.Бенджамини
Опубликовал Константин Моканов
Комплемент — важнейший элемент иммунной системы позвоночных животных и человека, играющий ключевую роль в гуморальном механизме защиты организма от патогенов. Термин впервые ввел Эрлих для обозначения компонента кровяной сыворотки, без которого ее бактерицидные свойства пропадали. Впоследствии было выяснено, что этот функциональный фактор представляет собой набор белков и гликопротеидов, которые при взаимодействии друг с другом и с чужеродной клеткой вызывают ее лизис.
Комплемент в буквальном смысле переводится как «дополнение». Изначально он считался всего лишь еще одним элементом, обеспечивающим бактерицидные свойства живой сыворотки. Современные представления об этом факторе значительно шире. Установлено, что комплемент представляет собой сложнейшую, тонко регулируемую систему, взаимодействующую как с гуморальными, так и с клеточными факторами иммунного ответа и оказывающую мощное влияние на развитие воспалительной реакции.
Общая характеристика
В иммунологии системой комплемента называют проявляющую бактерицидные свойства группу взаимодействующих друг с другом белков сыворотки крови позвоночных, представляющую собой врожденный механизм гуморальной защиты организма от патогенов, способный действовать как самостоятельно, так и в комплексе с иммуноглобулинами. В последнем случае комплемент становится одним из рычагов специфического (или приобретенного) ответа, поскольку антитела сами по себе не могут уничтожать чужеродные клетки, а действуют опосредованно.
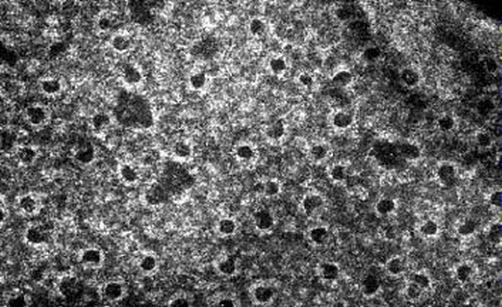
Эффект лизирования достигается за счет образования пор в мембране чужеродной клетки. Таких отверстий может быть множество. Перфорирующий мембрану комплекс системы комплемента называется МАК. В результате ее действия поверхность чужеродной клетки становится дырчатой, что приводит к выходу цитоплазмы наружу.
На долю комплемента приходится около 10% всех белков сыворотки. Его компоненты всегда присутствуют в крови, не оказывая никакого действия до момента активации. Все эффекты комплемента являются результатом последовательных реакций — либо расщепляющих входящие в его состав белки, либо приводящих к образованию их функциональных комплексов.
Каждый этап такого каскада подвержен строгой обратной регуляции, которая в случае необходимости может остановить процесс. Активированные компоненты комплемента проявляют большой комплекс иммунологических свойств. При этом эффекты могут оказывать на организм как положительное, так и негативное воздействия.
Основные функции и эффекты комплемента
Действие активированной системы комплемента включает:
- Лизис чужеродных клеток бактериальной и небактериальной природы. Осуществляется за счет образования специального комплекса, который встраивается в мембрану и проделывает в ней дыру (перфорирует).
- Активацию удаления иммунных комплексов.
- Опсонизацию. Присоединяясь к поверхностям мишеней, компоненты комплемента делают их привлекательными для фагоцитов и макрофагов.
- Активация и хемотаксическое привлечение лейкоцитов в очаг воспаления.
- Образование анафилотоксинов.
- Облегчение взаимодействия антигенпрезентирующих и В-клеток с антигенами.
Таким образом, комплемент оказывает комплексное стимулирующее воздействие на всю иммунную систему. Однако чрезмерная активность этого механизма может негативно повлиять на состояние организма. К отрицательным эффектам системы комплемента относят:
- Ухудшение протекания аутоиммунных заболеваний.
- Септические процессы (при условии массовой активации).
- Отрицательное влияние на ткани в очаге некроза.
Дефекты системы комплемента могут приводить к аутоиммунным реакциям, т.е. к повреждению здоровых тканей организма собственной иммунной системой. Именно поэтому имеет место такой строгий многоступенчатый контроль активации данного механизма.
Белки комплемента
Функционально белки системы комплемента подразделяются на компоненты:
- Классического пути (C1-C4).
- Альтернативного пути (факторы D, B, C3b и пропердин).
- Мембраноатакующего комплекса (C5-C9).
- Регуляторной фракции.
Номера С-белков соответствуют последовательности их обнаружения, но не отражают очередность их активации.

К регуляторным белкам системы комплемента относят:
- Фактор H.
- C4-связывающий белок.
- ФУД.
- Мембранный кофакторный белок.
- Рецепторы комплемента первого и второго типа.
C3 является ключевым функциональным элементом, поскольку именно после его распада образуется фрагмент (C3b), который присоединяется к мембране клетки-мишени, начиная процесс формирования литического комплекса и запуская так называемую петлю усиления (механизм положительной обратной связи).
Активация системы комплемента
Активация комплемента представляет собой каскадную реакцию, в которой каждый фермент катализирует активацию последующего. Этот процесс может происходить как с участием компонентов приобретенного иммунитета (иммуноглобуллинов), так и без них.
Есть несколько способов активации комплемента, которые отличаются последовательностью реакций и набором участвующих в ней белков. Однако все эти каскады приводят к одному итогу — образованию конвертазы, расщепляющей белок C3 на C3a и C3b.
Существуют три пути активации системы комплемента:
- Классический.
- Альтернативный.
- Лектиновый.
Среди них только первый связан с системой приобретенного иммунного ответа, а остальные имеют неспецифический характер действия.
Во всех путях активации можно выделить 2 этапа:
- Пусковой (или собственно активационный) — включает весь каскад реакций до момента образования C3/C5-конвертазы.
- Цитолитический — обозначает формирование мембраноатакующего комплекса (МКФ).
Вторая часть процесса во всех стадиях схожа и задействует белки C5, C6, C7, C8, C9. При этом только C5 подвергается гидролизу, а остальные просто присоединяются, образуя гидрофобный комплекс, способный встроиться и перфорировать мембрану.
Первый этап основан на последовательном запуске ферментативной активности белков C1, C2, C3 и C4 путем гидролитического расщепления на большие (тяжелые) и малые (легкие) фрагменты. Образовавшиеся единицы обозначаются малыми буквами а и b. Одни из них осуществляют переход к цитолитическому этапу, а другие выполняют роль гуморальных факторов иммунного ответа.
Классический путь
Классический путь активации комплемента начинается со взаимодействия ферментного комплекса C1 с группой антиген — антитело. C1 представляет собой фракцию из 5 молекул:
- C1q (1).
- C1r (2).
- C1s (2).
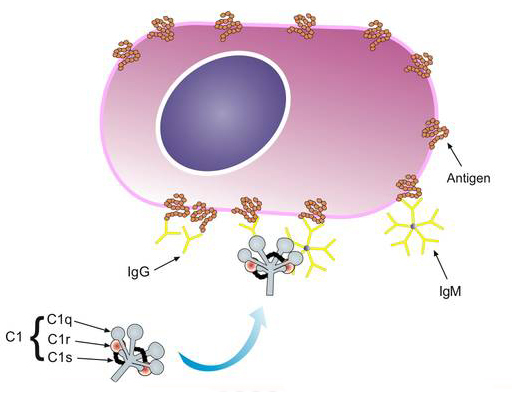
На первой ступени каскада с иммуноглобулином связывается C1q. Это вызывает конформационную перестройку всего комплекса C1, что приводит к его автокаталитической самоактивации и образованию действующего фермента C1qrs, расщепляющего белок C4 на C4a и C4b. При этом все остается прикрепленным к иммуноглобулину и, следовательно, к мембране патогена.
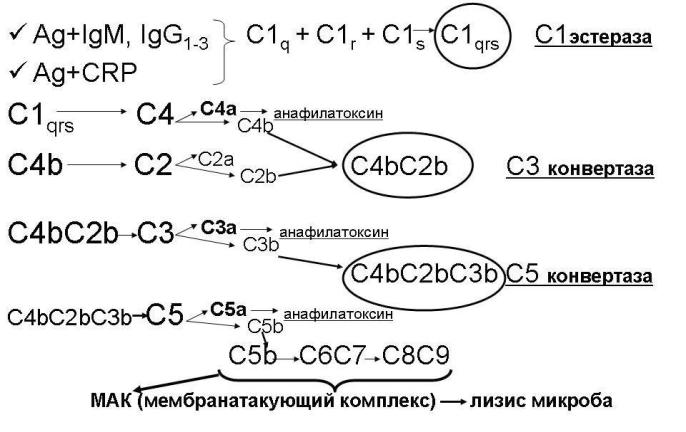
После осуществления протеолитического эффекта группа антиген — C1qrs присоединяет к себе фрагмент C4b. Такой комплекс становится подходящим для связывания с C2, которая под действием C1s тут же расщепляется на C2a и C2b. В результате создается C3-конвертаза C1qrs4b2a, действие которой формирует C5-конвертазу, запускающую образование МАК.
Альтернативный путь
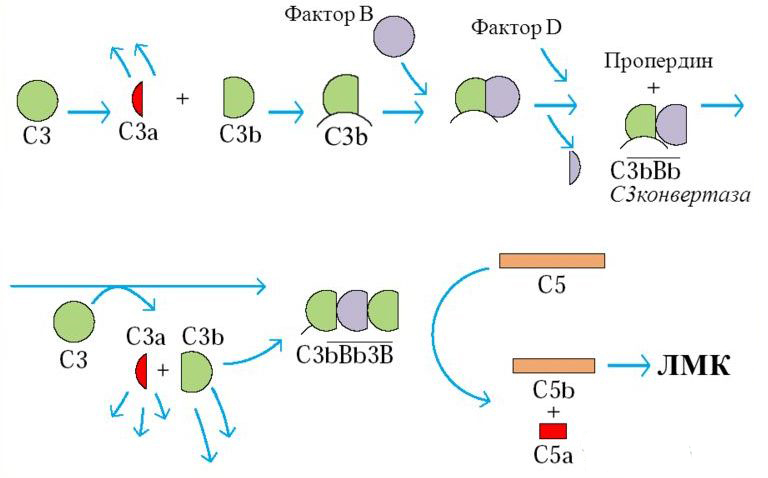
Такая активация иначе называется холостой, поскольку гидролиз C3 происходит самопроизвольно (без участия посредников), что приводит к периодическому беспричинному образования C3-конвертазы. Альтернативный путь осуществляется тогда, когда специфический иммунитет к возбудителю еще не сформировался. При этом каскад состоит из следующих реакций:
- Холостой гидролиз C3 с образованием фрагмента C3i.
- C3i связывается с фактором В, формируя комплекс C3iB.
- Связанный фактор В становится доступен для расщепления D-белком.
- Фрагмент Ba удаляется и остается комплекс C3iBb, который и является C3-конвертазой.
Суть холостой активации заключается в том, что в жидкой фазе C3-конвертаза нестабильна и быстро гидролизуется. Однако при столкновении с мембраной возбудителя стабилизируется и запускает цитолитическую стадию с формированием МАК.
Лектиновый путь
Лектиновый путь очень похож на классический. Основное отличие заключается в первой ступени активации, которая осуществляется не через взаимодействие с иммуноглобулином, а через связывание C1q с концевыми маннановыми группами, присутствующими на поверхности бактериальных клеток. Дальнейшая активация осуществляется полностью идентично классическому пути.
