Дендритные клетки врожденный иммунитет
Дендритные клетки – часть иммунной системы организма. Их сооткрывателем и открывателем ряда их ключевых функций был Ральф Штейнман [1,2], за что в 2011 году он получил Нобелевскую премию. По воле случая получилось так, что доктор Штейнман был единственным, кому Нобелевская премия досталась посмертно (сама по себе премия присуждается живым людям). Казус заключался в том, что смерть господина Штейнмана и объявление о присуждении ему премии произошли в один день (в пятницу), но о смерти было объявлено только в понедельник. Комитет Нобелевской премии решил, что технически на момент объявления победителя доктор Штейнман был жив, и ситуацию не стали «переигрывать».
Дендритные клетки (Dendritic cells, DCs) получили свое название за внешнюю схожесть с дендритами нейронов. Они являются частью врожденного иммунитета и играют важную роль в активации адаптивного иммунитета.
Цель заметки – раскрыть базовые принципы активации Т-клеток дендритными клетками и познакомить читателя с необходимой терминологией.
Содержание заметки:
- Врожденная и адаптивная иммунная система;
- Общие принципы функционирования врожденной иммунной системы;
- Pathogen-associated molecular patterns (PAMPs) и pattern recognition receptors (PRRs);
- Небольшой фокус на дендритных клетках и интерфероне I типа.
- Коротко о разных видах клеток адаптивной иммунной системы;
- Дендритные клетки и их функции:
- Antigen presenting cells и активация Т-клеток;
- MHC-белки и пептидные «сигнатуры» микробов;
- Разница MHC I и MHC II;
- Активация дендритных клеток молекулярными паттернами микробов;
- CCR7 (рецептор хемокина 7) и миграция в дендритных клеток в лимфоузлы;
- Циркуляция наивных Т-клеток и попадание их в лимфоузлы;
- Презентация антигена дендритными клетками и принцип «двойного рукопожатия»;
- Активация, экспансия и деактивация Т-клеток.
Рассказ не хочется ограничивать исключительно нюансами функций DCs. Хочется, чтобы эта информация накладывалась на какую-то базу о работе иммунной системы. При этом попытки охватить все и сразу не будет. Комплиментарная система, подробности создания и работы антигенов, активация B-клеток и многого-много другого в заметке не будет.
Врожденная иммунная система
Innate immune system (врожденный иммунитет) – мгновенно реагирует на заранее определенное и небольшое количество патогенных паттернов;
Adaptive immune system (адаптивный иммунитет) с задержкой реагирует, но на любое антитело. В последствии запоминая антитело, и в последующие разы реактивно на него реагируя.
Основной клеточный состав врожденной иммунной системы:
- Циркулирующие в крови клетки:
- Нейтрофилы, фагоцитируют бактерии, но быстро погибают (в течение часа), секретируют цитокины итд;
- Моноциты, преобразовываются в макрофаги при попадании в ткани;
- Дозорные клетки (sentinel cells):
- Маркофаги, фагоцитоз микробов и мертвых клеток (в основном нейтрофилов), секретируют цитокины, несколько месяцев жизни итд;
- Тучные клетки (mast cells), секретируют цитокины, гистамины итд;
- Дендритные клетки, запускают антивирусный ответ, активируют Т клетки итд.
Дозорные клетки находятся в тканях и реагируют на микробы после пересечения последними эпителиальных барьеров кожи и кишечника.
Циркулирующие клетки иммунной системы находятся в крови. И при воспалении попадают в нужные ткани.
Примерный порядок активации врожденного иммунитета:
- Микробы пересекают эпителиальные барьеры;
- Рецепторы дозорных клеток опознают «непрошенных гостей»;
- Дозорные клетки секретируют провоспалительные цитокины;
- Цитокины связывают на рецепторах эндотелия;
- Что активирует молекулы адгезии внутри сосудов;
- Различные молекулы адгезии с разной аффинитивностью связываются с соответствующими лигандами на поверхности циркулирующих иммунных клеток:
- Например, e-selectin связывается с низкой аффинитивностью с лингадом e-selectin на нейтрофилах, что затормаживает их движение;
- I-CAM связывается с высокой аффинтивностью с LFA-1 белком иммунной клетки, что останавливает иммунную клетку;
- После полной остановки иммунные клетки просачиваются с воспаленную ткань и начинают все доступными им способами уничтожать микробы;
- Первыми приходят нейтрофилы, фагоцитируют бактерии и через пару часов погибают сами; За ними приходят моноциты, превращаются в макрофаги и «подъедают» остатки трупов как микробов, так и нейтрофилов.
Остается вопрос: как дозорные клетки врожденного иммунитета опознают микробы?
PAMPs (Pathogen-associated molecular patterns) – паттерны молекулярных патогенов;
PPRs (Pattern recognition receptors) – рецепторы, опознающие паттеры.PAMPs:
- Вирусные (находятся внутри клетки):
- ДНК;
- Односпиральные РНК;
- Двуспиральные РНК
- Бактериальные (в большей степени на поверхности клетки):
- Паттерны Грам-отрицательные паттерны:
- Липополисахариды (LPS) клеточной стенки;
- Флагеллины («жгутики» для перемещения);
- Паттерны Грам-положительных бактерий:
- Флагеллины;
- Тейхоивые кислоты;
- Пептидогликаны
- Паттерны Грам-отрицательные паттерны:
Бактерии уничтожаются при помощи фагоцитоза и разрушения их клеточной стенки.
Цепочка будет такой: бактерия связывается с PPRs на поверхности клетки (так называемые TLRs toll like receptors) → димеризация рецепторов и запуск цепочки внутриклеточных сигналов ˧ деактивация ингибитора Nf-Kb → выраженность транскрипторного фактора Nf-Kb → клеточные изменения, в частности секреция цитокинов TNFα и IL-1.
Плазмоцитоидные дендритные клетки и антивирусный ответ
С вирусами ситуация чуть интересней, и тут к нам возвращаются дендритные клетки.
Дендритные клетки реагируют на вирусные PAMPs секретированием интерферонов 1 типа. INF type 1 приводят клетки (например, эпителия) в противо-вирусное состояние. Которое заключается в большей подверженности апоптозу зараженными клетками, выраженности белков/ферментов, которые мешают вирусу размножаться и которые могут наносить урон ДНК/РНК вируса.
Сами клетки в противовирусном состоянии также способны секретировать INF type 1.
Дендритные клетки
Необходимые вводные закончились, пора приступить к antigen presenting cells. К антиген презентующим клеткам относятся дендритные клетки, макрофаги и B-клетки.
В дальнейшем речь будет идти о том, как DCs активируют Т-клетки адаптивной иммунной системы.
Т-клетки, MHC I и MHCII
Т клетки своими рецепторами могут воспринимать только пептиды, представленные им на MHC белках антиген презентующих клеток.
MHC II
- Отвечает за бактерии;
- Дендритные клетки интернализируют бактерии, уничтожают их в лизосомах, в итоге мы получаем пептидную «сигнатуру» бактерии;
- MHC с пептидом отправляется к мембране;
- MHC II связываются с рецепторами CD4+ клеток (T helpers, которые активируют B-клетки и клетки врожденной иммунной системы;
- MHC II есть у антиген презентующих клеток.
MHC I
- Отвечает за вирусы (тему опухолей пропустим);
- Вирусный белок проходит юбиквинацию и становится доступных протеазам;
- Протеаза «расщепляет» вирусный белок до пептидов;
- Вирусный пептид с помощью транспортера TAP попадает в эндоплазматический ретикулум, откуда с MHC I комплексом попадает на мембрану;
- MHC I активирует CD8+ клетки (цитотоксичные T клетки, которые уничтожают зараженные вирусы;
- MHC I есть у большинства клеток, что объясняется особенностью вирусов.
Дендритные клетки. Активация и миграция в лимфоузлы
Для активации дендритных клеток должно произойти 2 события:
- MHC белок с пептидом микроба на поверхности клетки (значит он был так или иначе интернализирован и расщеплен до пептидов);
- PAMP рецепторы дендритных клеток должны быть активированными микробами;
При выполнении двух этих условий дендритные клетки выражают CD80/CD86 (подробнее чуть позже) и CCR7 (хемокин рецептор 7), выраженность которого приводит к тому, что DCs мигрируют в лимфососуды и по ним попадают во вторичные лимфо-органы. В частности, в лифмоузлы, где в межмембранном пространстве встречаются с Т-клетками.
Дендритные клетки активируют Т клетки
Т-лимфоциты путешествуют по крови по попадают с мемфоликулярное пространоство лимфоузлов при помощи кровотока и так называемых High endothelial venules (HEV).
Дело в том, что Т-клеток, аффинитивных определенному антигену, очень немного. Поэтому они путешествуют по организму, заходя ненадолго в лимфоузлы, куда активированные дендритные клетки попадают из тканей.
Для активации Т-клеток должно пройти 2 сигнала:
Сигнал 1. Антиген должен связаться с рецептором Т-клетки (нужна Т клетка с необходимой аффинитивностью рецептора;
Сигнал 2. Костимулирующие молекулы должны соединиться. Это B7-1 (CD80) и B7-2 (СD86) на стороне DCs и CD-28 на стороне Т-клеток.
Сигнал 1 без сигнала 2 приведет к апоптозу или анергии (угасание активной иммунной функции) Т-клетки.
После активация Т клетки проходят clonal expansion, активно делятся, их становятся десятки тысяч в случае с CD4+ и даже сотни тысяч в случае CD8+. Плюс Т-клетки после активации приобретают некоторые полезные фукнции.
Я опущу вопрос активации B-клеток Т-клетками, вопрос более глубокой функции T helpers и T killers. Остановлюсь только на активации Т клеток. В ткани они попадают примерно также, как циркулирующие в кроки клетки врожденной иммунной системы (см выше).
Деактивация Т-клеток
Любое воспаление (особенно цитотоксичное) чревато последствиями для организма. И этот процесс на уметь «тормозить».
В лимфоузлах это за это отвечает белок CTLA4 на Т-клетках, который связывается вместо CD28 с B7-1/B7-2. Это приводит к тому, что во время активации у нас будет только сигнал 1 и Т клетка будет неактивной.
Ткани (и опухоли) выражают PD-1 лиганд (PD-1, programmed death), который связывается с PD-1 белком Т-клеток, что приводит к их exhaustion (истощению), то есть деактивации.
Моноклональные антитела, подавляющие функции CTLA-4 и PD-1, одно из последних слов в борьбе с раковыми заболеваниями.
Выводы:
- Дендритные клетки активируются двумя сигналами:
- MHC белком на мембране, на котором будет пептидный антиген;
- PAMPs микробов связывается с рецепторами DCs;
- Активированные дендритные клетки выражают CCR7, что позволяет им мигрировать через лимфо-сосуды в лимфоузлы и «искать» в междфоликулярном пространстве нужную Т-клетку;
- Активация Т-клеток включает в себя 2 сигнала:
- Сигнал 1 MHC с пептидом (антигеном) связываются с нужным TCR (T cell receptor);
- Сигнал 2, костимуляция CD86/CD80 DCs с CD28 Т-клеток;
- При наличии только сигнала 1 Т-клетки подвергаются апоптозу или анергии;
- После активации начинается экспансия и дифференциация Т-клеток, которая является одним из компонентов ответа иммунной системы.
Источники:
- The road to the discovery of dendritic cells, a tribute to Ralph Steinman;
- Ralph Steinman (1943–2011). Immunologist and cheerleader for dendritic-cell biology;
- Торможение лейкоцитов молекулами адгезии [видео];
P.S. Это было писать скучно, в виду пересказа без моего вклада, но необходимо для ряда последующих заметок.
Словарь по итогам заметки:
- Врожденная иммунная система:
- Дозорные клетки (тучные, макрофаги, дендритные – это только основные, есть и другие);
- Циркулирующие клетки (моноциты, нейтрофилы);
- Также врожденная иммунная система включает в себя барьеры (эпителий, муцин), белки и молекулы (комплименты, агглутинины);
- Адаптивная иммунная система: B-клетки, T-помощники, цитотоксичные Т-клетки;
- Дендритные клетки:
- MHC I,
- MHC II
- CCR7
- B7-1 (CD80)
- B7-2 (CD86)
- Т-клетки:
- CD28
- CTLA4
- PD-1
- Клональная селекция;
- Клональная экспансия
- Антиген-презентующие клетки (DCs, макрофаги, B-клетки);
- Анергия
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 4 мая 2020;
проверки требует 1 правка.
Дендритная клетка под микроскопом
Дендритные клетки (англ. Dendritic cells, DC) — это гетерогенная популяция антигенпредставляющих клеток костно-мозгового происхождения. Морфологически дендритные клетки — крупные клетки (15-20 мкм) круглой, овальной или полигональной формы с эксцентрически расположенным ядром, многочисленными разветвлёнными отростками мембраны.[1] Термин «дендритные клетки» ввёл в 1973 году Ральф Стайнман из Рокфеллеровского университета[2].
Характеристика[править | править код]
Дендритные клетки экспрессируют набор поверхностных молекул, характерный для других антигенпредставляющих клеток:
- патоген-распознающие рецепторы, в том числе рецепторы для компонентов клеточной стенки и нуклеиновых кислот микроорганизмов, рецепторы к компонентам комплемента (CD205, CD206, CD14), Толл-подобные рецепторы;
- молекулы II класса гистосовместимости (ГКС);
- костимуляторные молекулы CD40, B7.1 (CD80), B7.2 (CD86), ICOS-L;
- коингибиторные молекулы B7-DC (CD274), B7-H1 (CD274) и др.;
- молекулы межклеточной адгезии (ICAM-1), CD11b, CD11c;
- комплекс хемокиновых рецепторов (CD193, CD197 и многие другие).
К молекулам, которые представлены преимущественно на дендритных клетках, относят:
- молекулы LAMP-семейства CD208 (DC-LAMP), BAD-LAMP;
- высокоспецифичный маркер зрелых ДК — молекулу CD83;
- ГКС-подобные молекулы CD1a, CD1c, участвующие в презентации липидных антигенов ;
- молекулы CD209 (DC-SIGN), CD207 (лангерин).
У человека выделяют две основные субпопуляции дендритных клеток
- миелоидные дендритные клетки (myeloid DC — mDC) — названы так потому, что происходят из общего миелоидного гемопоэтического предшественника. Локализованы в различных органах и тканях, где захватывают чужеродные антигены путём пино- и фагоцитоза, после чего экспрессируют антигенную детерминанту в комплексе с молекулами MHC II класса. Затем дендритные клетки мигрируют в регионарные лимфоузлы, где стимулируют пролиферацию и дифференцировку антигенспецифических Т-лимфоцитов, тем самым инициируя и стимулируя иммунный ответ. Специфическими маркерами миелоидных дендритных клеток крови являются молекулы BDCA-1 (CD1c) и BDCA-3 (CD141).
Миелоидные ДК не экспрессируют популяционные маркеры других клеток иммунной системы, таких как CD14 (моноциты, макрофаги и нейтрофилы), CD3 (Т-лимфоциты), CD19, CD20 (B-лимфоциты), CD56, CD57 (естественные киллеры), CD16, CD66b (гранулоциты). В ответ на стимуляцию индукторами созревания, миелоидные дендритные клетки продуцируют преимущественно цитокины Th1 спектра, включая ИЛ-6, ИЛ-12, фактор некроза опухоли и интерферон-гамма.
- плазмоцитоидные дендритные клетки (plasmacytoid DC — pDC), эти клетки — лимфоидного происхождения и морфологически напоминают плазматические клетки. pDCs экспрессируют TLR-9, лигандами которого являются CpG-олигонуклеотиды бактериальной ДНК. ПДК секретируют в больших количествах интерфероны I типа (α и β), являясь основными интерферон-продуцирующими клетками крови, а также ИЛ-4 и ИЛ-10, которые переключают дифференцировку нулевых Т-хелперов в Т-хелперы 2 типа. К маркерам плазмацитоидных дендритных клеток относят молекулы BDCA-2 (CD303), BDCA-4 (CD304).
Функции дендритных клеток[править | править код]
Основной функцией дендритных клеток является презентация антигенов Т-клеткам. Дендритные клетки также выполняют важные иммунорегуляторные функции, такие как контроль за дифференцировкой Т-лимфоцитов, регуляция активации и супрессии иммунного ответа. Важной особенностью дендритных клеток является способность захватывать из окружающей среды различные антигены при помощи пиноцитоза и рецептор-опосредованного эндоцитоза. Больше всего дендритных клеток находится в тканях, которые соприкасаются с внешней средой, например в толще эпителиального слоя слизистой оболочки кишечника, в подслизистой респираторного, желудочно-кишечного и урогенитального трактов.
Дендритные клетки поглощают антигены, процессируют и представляют на своей поверхности в комплексе с MHC I или MHC II классов. Только в таком виде Т-клетки способны распознать антиген и вслед за этим активироваться и развить иммунный ответ.
В зависимости от типа патогена дендритные клетки способны направлять дифференцировку наивных Т-хелперов (Th0) в сторону Т-хелперов 1 типа, Т-хелперов 2 типа, регуляторных Т-клеток или же Т-хелперов 17.
Применение в медицине[править | править код]
В последнее десятилетие дендритные клетки вызывают повышенный интерес исследователей благодаря лёгкости их получения из клеток кожи (фибробластов), а также из моноцитов периферической крови или стволовых клеток костного мозга и способности эффективно представлять антиген Т-лимфоцитам. К настоящему времени проведено множество исследований по модуляции иммунного ответа у больных хроническими инфекционными и онкологическими заболеваниями с использованием праймированных антигеном дендритных клеток. Результаты большинства исследований обнадеживающие, показана безопасность применения ДК, активация иммунной системы в ответ на проводимую терапию и неплохой клинический эффект. Так, например, убедительные доказательства безопасности и эффективности лечения рака простаты при помощи ДК, показанные на 512 пациентах, позволило Управлению по контролю за качеством пищевых продуктов и лекарственных препаратов США в 2010 г. одобрить использование ДК для лечения пациентов с данным заболеванием [3].
См. также[править | править код]
- Иммунная система
Примечания[править | править код]
Литература[править | править код]
- Ueno H, Klechevsky E, Morita R, Aspord C, Cao T, Matsui T, Di Pucchio T, Connolly J, Fay JW, Pascual V, Palucka AK, Banchereau J. Dendritic cell subsets in health and disease. Immunol Rev. 2007 Oct;219:118-42.
Ссылки[править | править код]
- Dendritic cell subsets in health and disease. // Immunol Rev. 2007 Oct;219:118-42.
Клеточные элементы врожденного иммунитета. Дендритные клетки
Впервые дендритные клетки были описаны Лангергансом в 1868 г., в связи с чем впоследствии они стали известны как клетки Лангерганса. Однако сам автор считал их чувствительными нейронами. Фундамент современных представлений о ДК, как клетках иммунной системы, заложили американские ученые Штайман и Кон, и коллеги в 1970-е гг., открывшие и охарактеризовавшие ДК в лимфоидных органах мышей.
В 1985 г. показана принадлежность клеток Лангерганса к ДК. 1990-е гг. характеризуются определением характеристики различных линий ДК и путей их дифференцировки, установлением роли ДК в регуляции клеточного, гуморального адаптивного ответа, началом изучения роли ДК в патогенезе инфекционных и онкологических заболеваний человека.
Подобно другим клеткам иммунной системы, предшественниками ДК являются гематопоэтические стволовые клетки костного мозга. FLT-3 лиганд и GM-CSF являются ключевыми ростовыми и дифференциро-вочными факторами in vivo.
В процессе гематопоэза стволовые клетки, несущие молекулы CD34′, дают начало двум типам прекурсорных ДК (пpe-DCs) — моноцитов (пре-DC1) и плазмацитоидных клеток (пpe-DC2), из которых формируются зрелые ДК. Данные предшественники составляют около 1% всех мононуклеарных клеток периферической и пуповинной крови, а также лимфоидных органов.

Показано, что у мыши и человека ДК образуются преимущественно в красном костном мозге из предшественников миелоидного ряда или в тимусе из предшественников лимфоидного ряда.
Миелоидные дендритные клетки формируются из СD14+-моноцитов и CD11c-клеток СD14+’-моноциты дифференцируются в незрелые ДК и макрофаги, а CD11с+-клетки дают начало эпидермальным клеткам Лангерганса, интерстициальным ДК, локализующимся в дерме большинства органов, включая сердце и легкие. ДК, происходящие из СD14′-моноцитов, отличаются очень высокой способностью к захвату антигена и индукции дифференцировки В-лимфоцитов в IgM-продуцирующие клетки.
В настоящее время в крови выявлено как минимум 4 вида миелоидных пре-ДК (в порядке убывания численности): 1)CD14++CD16-Cd11c+HLA-DR); 2)CD147 CD16CD11cHLA-DR’-клетки, ранее считавшиеся активированной субпопуляцией моноцитов; 3) CD14CD16CDIc’CD11cHLA-DR-клетки по свойствам наиболее близкие к незрелым ДК; 4) CD14 CD16 BDCA-3CD11cHLA-DR-клетки. Описаны также два пути дифференцировки макрофагов в ДК: 1) в присутствии GM-CSF и IL-4; 2) при миграции активированных макрофагов через стенку афферентных лимфатических сосудов. Возможно и обратное превращение незрелых ДК в макрофаги под действием IL-10 и M-CSF.
Таким образом, предполагается, что в тканях существует динамическое равновесие между миелоидными ДК (АПК) и макрофагами (клетками-эффекторами), которое определяется потребностями иммунной системы и регулируется цитокиновым микроокружением.
— Также рекомендуем «Лимфоидные или плазмацитоидные дендритные клетки. Функции дендритных клеток»
Оглавление темы «Дендритные клетки и естественные киллеры иммунитета»:
- Анатоксин стафилококковый очищенный (АСО). Укрепление иммунитета стафилококковым анатоксином
- Ликопид как иммуномодулятор. Механизмы стимуляции иммунитета ликопидом
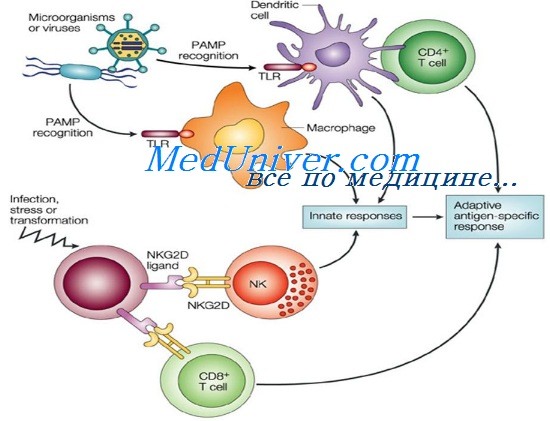
- Клеточные элементы врожденного иммунитета. Дендритные клетки
- Лимфоидные или плазмацитоидные дендритные клетки. Функции дендритных клеток
- Миелоидные дендритные клетки. Фолликулярные, опухоль-ассоциированные дендритные клетки
- Влияние иммуномодуляторов на дендритные клетки. Морфология дендритных клеток
- Фагоцитарная активность дендритных клеток. Иммунофенотип дендритных клеток
- Действие иммуномодуляторов на активацию дендритных клеток. Созревание дендритных клеток
- Естественные киллеры (NK). Функции естественных киллеров
- Естественные киллеры Т-лимфоциты. Взаимодействие естественных киллеров и дендритных клеток
