Иммунитет и его патологии

ИММУНИТЕ́Т животных и человека (от лат. immunitas – освобождение, избавление), способность организма поддерживать свою целостность и биологическую индивидуальность путём распознавания и удаления чужеродных веществ и клеток. Учение об И. родилось из необходимости преодолеть инфекц. болезни, эпидемии которых (чума, холера, оспа и др.) до кон. 19 в. уносили большое число жизней людей. В связи с этим под термином «И.» долгое время понимали невосприимчивость организма к инфекц. заболеваниям. Дальнейшие исследования показали, что И. – это также устойчивость организма к пересаживаемым органам и тканям, к изменившимся собств. клеткам, включая раковые, а также к чужеродным веществам животного и растит. происхождения. В поддержании И. участвуют защитные механизмы врождённого (неспецифического) и приобретённого (специфического, или адаптивного) иммунитета.
Формы врождённого и приобретённого иммунитета и их взаимосвязь
Врождённый И. присущ всем многоклеточным животным, осуществляется специализир. клетками, развивающимися вне зависимости от поступления в организм чужеродных и потенциально опасных агентов; его неспецифич. защитные механизмы реализуются после кратковременной активации специализир. клеток. Приобретённый И. характерен для хрящевых и костных рыб, земноводных, пресмыкающихся, птиц и млекопитающих, его основой является иммунный ответ – цепь реакций иммунной системы, которая включается чужеродными агентами (антигенами) и приводит к формированию клеток и молекул, удаляющих эти агенты или продукты их разрушения из организма. В отличие от врождённого И., реакции которого универсальны в отношении разл. чужеродных агентов, иммунный ответ приобретённого И. специфичен (направлен против агентов, включивших этот иммунный ответ). Обе формы И. тесно взаимосвязаны: иммунный ответ развивается лишь при условии предварит. активации врождённого И., а продукты приобретённого И. повышают эффективность врождённого И. Реакции И. осуществляются спец. клетками – иммуноцитами. У высших животных, напр., это лейкоциты, которые созревают в кроветворных органах и некоторое время циркулируют в крови, а затем заселяют ткани. Реакции врождённого И. обеспечивают миелоидные клетки (нейтрофильные и эозинофильные гранулоциты, моноциты и их тканевые формы – макрофаги, дендритные и тучные клетки) и частично – лимфоидные дендритные клетки. Реакции приобретённого И. реализуются Т- и В-лимфоцитами.
Процесс распознавания чужеродных агентов в организме: рецепторы врождённого и приобретённого иммунитета
Распознавание чужеродных молекул в организме осуществляется с помощью спец. белковых рецепторов. Рецепторы врождённого И. имеют сродство к небольшому числу молекул, характерных для болезнетворных микроорганизмов (патогенов), но отсутствующих в организме данного вида. Такие молекулы (бактериальные липополисахариды, гликолипиды, пептидогликаны, нуклеиновые кислоты бактерий и вирусов и др.) называют молекулярными «образами», связанными с патогенами (PAMP – от pathogen-associated molecular patterns); они сигнализируют о потенциальной опасности со стороны патогенов. Распознавание РАМР осуществляют неск. типов рецепторов (т. н. Toll- и NOD-рецепторы, лектиновые рецепторы), которые представлены небольшим числом вариантов (ок. 10) и располагаются на поверхности или внутри клеток системы врождённого И.; такое распознавание надёжно, поскольку детерминируется генами зародышевой линии. Связывание РАМР с рецепторами приводит к активации клеток системы врождённого иммунитета.
Гл. особенность распознавания рецепторов в рамках приобретённого И. состоит в том, что каждый рецептор распознаёт конкретную чужеродную молекулу, называемую антигеном, точнее фрагмент антигена – его эпитоп, или антигенную детерминанту. При этом разные лимфоциты несут на своей поверхности рецепторы к разным эпитопам. Т. о., каждая клетка способна распознать только один эпитоп (или группу структурно сходных эпитопов) и лишь популяция лимфоцитов в целом способна обеспечить распознавание всего разнообразия чужеродных молекул, для чего требуется 105–107 вариантов рецепторов. В геноме животных содержится неск. сотен вариантов генов, кодирующих антигенраспознающие рецепторы лимфоцитов. Их вариабельность сильно возрастает при дифференцировке лимфоцитов в процессе перестройки соответствующих генов. Последняя происходит в каждой клетке автономно, в результате чего каждый лимфоцит и его потомство (клон) располагают индивидуальным по специфичности рецептором. Существует три типа антигенраспознающих рецепторов – два варианта (белковые димеры αβ и γδ , родственные иммуноглобулинам) в субпопуляциях Т-лимфоцитов и один (мембранный иммуноглобулин) в популяции В-лимфоцитов. Рецепторы В-лимфоцитов распознают эпитопы нативных молекул антигена, а Т-лимфоцитов – эпитопы, предварительно выщепленные из целой молекулы и включённые в состав молекулы главного комплекса гистосовместимости. Такую обработку антигена осуществляют антигенпредставляющие клетки. Для активации Т-лимфоцитов при этом требуется дополнит. стимуляция (костимуляция) с помощью молекул, образующихся при активации врождённого И. В отсутствии костимуляции формируется анергия (неотвечаемость) Т-лимфоцитов. При стимуляции В-лимфоцитов источником костимулирующих сигналов служит Т-лимфоцит (в частности, Т-хелпер, или клетка-помощник). Активация лимфоцитов – условие их последующей пролиферации (для обеспечения количества клеток, достаточного для осуществления защиты) и дифференцировки в эффекторные (исполнительные) клетки, которые обеспечивают реакции приобретённого иммунитета.
Механизмы удаления чужеродных агентов из организма при врождённом и приобретённом иммунитете
Удаление чужеродных агентов из организма осуществляется с использованием комплекса механизмов, бо́льшая часть которых формируется в рамках врождённого И. Эффекторные механизмы И. разделяют на клеточные и гуморальные. Клеточные механизмы врождённого И. приводят к цитолизу (разрушению клеток). Из трёх вариантов последнего (внутриклеточный, внеклеточный и контактный) наиболее эффективен внутриклеточный цитолиз, реализуемый в процессе фагоцитоза: чужеродная клетка захватывается фагоцитами (нейтрофилами, макрофагами и др. клетками) и, оказавшись внутри фаголизосомы, сначала убивается активными формами кислорода, оксидом азота и бактерицидными пептидами, а затем расщепляется ферментами. Внеклеточному цитолизу бактерицидными факторами, секретируемыми лейкоцитами (в т. ч. эозинофилами), подвергаются, напр., клетки многоклеточных паразитов, контактному цитолизу – инфицированные вирусом или опухолевые клетки с помощью т. н. NK-клеток (от англ. natural killer – естественный истребитель). В зоне контакта последних с клетками-мишенями формируется микрополость, в которую NK-клетка секретирует вещества, одни из которых формируют поры в мембране клетки-мишени, а другие, проникнув через эти поры, включают процесс апоптоза – активной формы гибели клетки. Гуморальными факторами врождённого И., способствующими удалению чужеродных агентов, являются бактерицидные пептиды (дефензины, кателицидины), белки острой фазы воспаления, компоненты системы комплемента, цитокины. Активируемые компоненты комплемента вызывают опсонизацию – облегчение фагоцитоза микроорганизмов или их лизис в результате формирования поры в мембране. Белки острой фазы (в т. ч. С-реактивный белок) опсонизируют чужеродные клетки и активируют комплемент. Цитокины обеспечивают формирование воспалит. реакции, в рамках которой реализуется врождённый И.; относящиеся к ним интерфероны оказывают противовирусное и противоопухолевое действие.
Осн. эффекторными факторами приобретённого И. служат цитотоксические Т-лимфоциты, цитокины, секретируемые Т-хелперами, и антитела. Цитотоксические Т-лимфоциты образуются в процессе клеточного иммунного ответа. Они реализуют своё действие с помощью механизма контактного цитолиза или апоптоза клеток-мишеней. Мишенью цитотоксических Т-лимфоцитов являются лишь те клетки, которые экспрессируют антигенные эпитопы, распознаваемые Т-лимфоцитами, т. е. их действие более прицельно, чем действие естеств. киллеров. Участие Т-хелперов в реализации эффекторной фазы иммунного ответа связано с секрецией цитокинов, прежде всего интерферона. При его действии на макрофаги (особенно в сочетании с фактором некроза опухоли) резко повышается бактерицидная активность последних и разрушаются даже те патогены (микобактерии, простейшие), которые не могут быть убиты без участия цитокинов. Т. о., гуморальные продукты Т-хелперов усиливают внутриклеточный цитолиз, осуществляемый в рамках врождённого И. Антитела, секретируемые плазматич. клетками, которые дифференцируются из В-лимфоцитов, представляют собой растворимую форму их антигенраспознающих рецепторов. Обладая способностью связываться с антигенами как в растворимой, так и в мембраносвязанной формах, они могут блокировать антигены и несущие их патогены. Результатом блокады может быть утрата микробными клетками подвижности, способности к адгезии, предотвращение инфицирования клеток вирусами. При связывании токсинов или ферментов антитела нейтрализуют их активность. Однако бо́льшая часть эффектов антител обусловлена привлечением эффекторных клеток и молекул. При взаимодействии с антигеном (см. Антиген – антитело реакция) демаскируются участки молекулы антитела, распознаваемые компонентами комплемента (C1q) и Fc-рецепторами эффекторных клеток – фагоцитов и естеств. киллеров. Связывание C1q приводит к активации комплемента с опсонизацией и/или лизисом чужеродной клетки. Связывание с Fc-рецептором макрофага или иного фагоцита облегчает фагоцитоз (опсонизацию). Распознавание антител, фиксированных на клетках-мишенях, Fc-рецепторами естеств. киллеров облегчает осуществление контактного цитолиза. Т. о., бóльшая часть проявлений эффекторной активности антител, как и клеточных факторов приобретённого И., состоит в повышении эффективности реакций врождённого И. и придании им специфичности в отношении конкретных антигенов.
В ходе иммунного ответа формируется иммунологическая память, не свойственная врождённому И. Её субстратом служат Т- и В-лимфоциты иммунологич. памяти, которые дифференцируются при первичном иммунном ответе, не принимая в нём участия, и затем длительно сохраняются в организме. Реакция этих клеток на антиген при его повторном поступлении (вторичный иммунный ответ) осуществляется более быстро и эффективно, чем реакция лимфоцитов при первом контакте с антигеном. На этом основано создание искусственного И. к возбудителям заболеваний путём вакцинации: ослабленный, убитый патоген или выделенные из него антигены вызывают формирование клеток памяти без развития инфекц. процесса, что повышает эффективность иммунной защиты при поступлении в организм активного патогена, несущего те же антигенные молекулы. Аналогичные подходы используют для создания И. к опухолевым клеткам с помощью онковакцин.
Патология иммунитета
может быть обусловлена его ослаблением (иммунодефициты) или извращённым проявлением (аутоиммунитет, аллергия). Иммунодефициты могут проявляться как самостоят. заболевания, обусловленные дефектом генов (первичные иммунодефициты), или как синдромы, сопутствующие др. заболеваниям или действию повреждающих факторов (вторичные иммунодефициты). Аутоиммунные болезни являются следствием развития иммунного ответа на собств. антигены организма. Основой аллергии служит неадекватно усиленная реакция И. на определённые антигены (аллергены); её причиной является выброс активных субстанций из тучных клеток при взаимодействии аллергена с IgE-антителами, фиксированными на поверхности этих клеток. К патологии И. могут быть отнесены также иммунологич. осложнения беременности (реакция на антигены плода). Особое место занимает реакция организма на трансплантаты чужеродных тканей, а также реакция иммуноцитов, содержащихся в трансплантате, на антигены организма (реакция трансплантат-против-хозяина). Необходимость предупреждения и лечения извращённых проявлений И. породила задачу ослабления И. путём «ингибирующей» вакцинации (аллерговакцины, вакцины против аутоиммунитета), что дополнило традиц. способы усиления И. против воздействия патогенных факторов (см. Иммунизация). Поиски путей направленной иммунокоррекции в значит. степени определяют прикладную значимость изучения И. и обусловливают обществ. интерес к иммунологич. проблемам. Наука об иммунитете называется иммунологией. См. также Иммунопатология.
Источник
![]()

Что такое иммунитет?
Иммунитет – это защитная система организма от негативного воздействия чужеродных агентов. Основа функционирования иммунного аппарата – это различение «своих» и «не своих» структур. Иммунная система призвана сохранять генетическую целостность организма.
Виды иммунитета
Иммунитет делится на два вида: врожденный и приобретенный.
Врожденный иммунитет – это система наследственных защитных биомеханизмов, обусловленная анатомо-физиологическими и видовыми особенностями организма. Человек не болеет зоонозными заболеваниями, так как невосприимчивость определенного биологического вида к инфекциям закреплена генетически.
Приобретенный – вырабатывается индивидуально для каждого человека в течение жизни при контакте с многочисленными антигенами. Для него характерна специфичность, он не передается по наследству.
Приобретенный бывает естественным, который образуется при встрече с инфекцией и искусственным, когда при помощи вакцинации защищают организм человека от заболеваний.
Искусственный иммунитет делят на активный, когда организм сам синтезирует антитела, и пассивный, когда в организм вводят уже готовые антитела против той или иной инфекции.
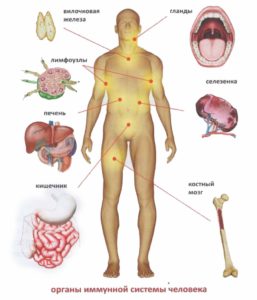 Органы иммунной системы
Органы иммунной системы
- костный мозг;
- вилочковая железа (тимус);
- селезенка;
- миндалины лимфоидного кольца, гланды;
- лимфатические узлы
- кишечник (Пейеровы бляшки)
- печень
В костном мозге синтезируются В-лимфоциты и лейкоциты.
В тимусе вырабатываются Т-лимфоциты и ряд гормонов, влияющих на работу вилочковой железы.
В селезенке происходит очищение крови от поврежденных эритроцитов и гетерогенных элементов. Кроме того, селезенка служит резервным хранилищем иммунных клеток.
Миндалины лимфоидного кольца, расположенного у входа в носоглотку, препятствуют проникновению в организм чужеродных агентов – патогенных микроорганизмов.
В тонком кишечнике имеются Пейеровы бляшки – скопления лимфоидной ткани, которые блокируют болезнетворные микробы.
Лимфатические узлы распределены по ходу лимфатических сосудов. Все вредные вещества: продукты клеточного обмена, токсины вместе с тканевой жидкостью оказываются в лимфоузлах, где обезвреживаются. Только тогда очищенная лимфа поступает в общий кровоток.
Механизмы работы иммунной системы
Гетерогенные (чужие) микроструктуры при проникновении в организм вызывают иммунный ответ – клеточный или гуморальный. За клеточный иммунитет ответственны Т-лимфоциты, которые формируются в тимусе.
В-лимфоциты, продуцируемые костным мозгом, отвечают за образование гуморальных иммунно-компетентных веществ.
При попытке внедрения в организм инородного антигена, на его пути первыми становятся неспецифические механизмы защиты: кожные покровы и слизистые оболочки. Помимо механического препятствия, они выделяют энзимы (секрет потовых и сальных желез, слюна, слизь носовой полости, соляная кислота и пептические ферменты желудка), которые обладают губительным действием на микроорганизмы.
Если первая линия защиты не справляется (при массивной микробной атаке, высоком уровне вирулентности патогена), антиген попадает в организм. Тогда включается в работу клеточный иммунитет: лейкоциты, фагоциты, макрофаги. Эти клетки захватывают патогены, растворяют клеточные мембраны микробов, переваривают, вырабатывают вещества, способствующие полному их уничтожению.
Параллельно с неспецифическим иммунитетом начинает функционировать гуморальный отдел иммунитета. Клетки иммунной системы опознают чужака, запоминают его генетическую структуру и начинают синтез антител против конкретного микроба. Сведения о геноме антигена сохраняются в иммунной «памяти», а в случае повторной встречи организма с тем же микробом, образование антител происходит гораздо быстрее.
Симптомы ослабления иммунитета

Снижение иммунитета характеризуется появлением массы жалоб у пациента – от плохого самочувствия до серьезных патологий, требующих немедленной медицинской помощи.
Все симптомы, свидетельствующие о неполадках в иммунной системе, можно разделить на четыре группы:
Инфекционный синдром
- Характеризуется увеличением числа инфекционных респираторных заболеваний; у взрослых более 4 эпизодов, у детей – от 6 случаев за год. ОРЗ и ОРВИ нередко протекают с осложнениями в виде пневмоний, отитов, синуситов.
- Частые проявления герпетической инфекции, которая является маркером сниженного иммунитета.
- Склонность к гнойничковым поражениям кожи: фурункулез, пиодермия.
- Наличие хронических инфекций: рецидивирующие тонзиллиты, пиелонефриты.
- Длительный субфебрилитет.
Инфекционные заболевания отличаются затяжным течением, тенденцией к хронизации процесса, устойчивости к проводимой терапии.
Аллергический синдром
Аллергия – это неадекватный ответ организма на воздействие какого-либо антигена. При этом нормальная иммунная реакция заменяется на патологическую, которая и является основой развития многочисленных аллергических заболеваний: бронхиальная астма, атопический дерматит и другие.
Аутоиммунный синдром
Это состояния, при которых иммунная система воспринимает собственные клетки за чужеродные и начинает против них вырабатывать антитела, тем самым разрушая орган, на который направлена ее агрессия. К таким болезням относится: аутоиммунный тиреоидит, ревматоидный артрит, дерматомиозит.
Желудочно-кишечный синдром
В него включают заболевания пищеварительного тракта: гастриты, энтериты, колиты, дисбактериозы.
Факторы и причины снижения иммунитета
 Факторы, связанные с образом жизни:
Факторы, связанные с образом жизни:
- Несбалансированное питание: дефицит витаминов, минералов, белков.
- Вредные привычки: табакокурение, алкоголизм, наркомания.
- Гиподинамия или чрезмерные физические нагрузки.
- Длительные психотравмирующие ситуации.
- Воздействие ионизирующего излучения.
- Профессиональные вредности.
Причины, обусловленные болезнями:
- Тяжелые соматические и инфекционные заболевания, ведущие к истощению организма.
- Патологии и травмы органов, принимающих участие в формировании иммунитета.
- Хирургические вмешательства.
- Кровотечения.
- Дисбактериоз.
- Химио- и радиотерапия при лечении онкологии.
- Почечные и печеночные патологии.
Задачи иммунитета
Главная задача иммунной системы – это иммунный надзор, который обеспечивает нормальное функционирование организма, предохраняет его от инфекционных и неинфекционных заболеваний.
Иммунная система реализует свои задачи при помощи следующих действий:
- Распознавание антигена.
- Активизация механизмов различных звеньев иммунитета для нейтрализации антигена.
- Регуляция и координация разных систем, поддерживающих постоянство внутренней среды, при проникновении в организм чужеродных агентов.
Последствия иммунодефицита
Иммунодефицит – это состояние, которое характеризуется снижением функциональной активности звеньев иммунитета – гуморального и клеточного – неспособностью иммунной системы распознать и уничтожить попавшую в организм гетерогенную субстанцию.
По этиологии иммунодефицитные состояния бывают:
- Физиологические: беременные, новорожденные, старики.
- Первичные (врожденные), обусловленные генетическим мутациями. Патология проявляется уже с раннего возраста развитием инфекционных заболеваний, протекающих с осложнениями. Присоединяются аутоиммунные, аллергические и онкологические болезни. При тотальном повреждении нескольких видом иммунокомпетентных клеток, прогноз неблагоприятный.
- Вторичные (приобретенные) формируются под воздействием повреждающих внешних или внутренних факторов. Примером вторичного иммунодефицита служит ВИЧ-инфекция. При вторичных иммунодефицитах страдают звенья клеточного, гуморального иммунитета, представители неспецифической защиты, а также их сочетания. Этот вид встречается гораздо чаще первичного и характеризуется благоприятным течением: при адекватном лечении иммунный статус восстанавливается полностью.
Причины, вызывающие вторичный иммунодефицит:
- Туберкулез.
- Истощение организма.
- Массивные кровопотери.
- Обширные травмы.
- Ожоговая болезнь.
- ВИЧ-инфекция.
- Уремия.
- Паразитарные инвазии.
- Онкологические патологии.
- Прием цитостатиков и иммунодепрессантов.
- Радиоактивные излучения.
Как укрепить иммунитет при помощи витаминов, лекарственных растений, антиоксидантов компании НСП
 Продукты компании НСП – это концентрированные органические биологически активные вещества, полученные из натурального сырья растительного, животного, морского, минерального происхождения.
Продукты компании НСП – это концентрированные органические биологически активные вещества, полученные из натурального сырья растительного, животного, морского, минерального происхождения.
Специалистами компании НСП разработан проект – комплекс натуральных средств «Сильный иммунитет», который укрепит иммунитет, уменьшит вероятность респираторных заболеваний, предотвратит нежелательные осложнения.
Продолжительность предварительного курса восстановления – 3 месяца; он складывается из нескольких этапов:
- Сдерживание вредного воздействия окружающей среды.
- Оздоровление ЖКТ, дезинтоксикация, нормализация кишечной микрофлоры.
 Реабилитация кишечника проводится препаратами из набора «Здоровье ЖКТ как Основа» (подробнее о применение):
Реабилитация кишечника проводится препаратами из набора «Здоровье ЖКТ как Основа» (подробнее о применение):
- Pau D’ Arco NSP (По Д’ Aрко НСП) — по 2-3 капс. бросить в стакан горячей воды, дать остыть по состояния теплового чая, потом добавить 1 ч.л. Chlorophyll Liquid (Хлорофилл Жидкий),выпить за 30-40 минут до завтрака, обеда и ужина. (1 этап ЖКТ)
- HP Fighter (Эйч Пи Файтер) — по 1 капсуле за 20-30 минут до завтрака, обеда и ужина, запивая 1 воды с 1 ч.л. Chlorophyll Liquid (Хлорофилл Жидкий). (2 этап ЖКТ)
- Caprylic Combination (Комплекс с каприловой кислотой) — по 2 капс. 3 раза в день во время еды. (3 этап ЖКТ)
- Bifidophilus Flora Force NSP (Бифидофилус Флора Форс НСП) – по 1 капс. 2 р/ день. (4 этап ЖКТ)
- Burdock (Репейник)– по 1 капс. 2 р/ день. (4 этап ЖКТ)
- Chlorophyll Liquid (Хлорофилл Жидкий) – растворить чайную ложку препарата в 200 мл воды; пить 2 р/ день. (4 этап ЖКТ)
- Loclo (Локло) – 20 мл средства на стакан воды. За час необходимо выпить еще до полулитра жидкости. (4 этап ЖКТ)
Препараты надо принимать по схеме комплексно, так как они усиливают действие друг друга, оказывая влияние на разные звенья иммунитета.
Продукты, входящие в базовый набор «Сильный Иммунитет«:
- Кошачий Коготь действует как органический иммуноактиватор.
- Защитная формула НСП – комплексный подбор витаминов, минералов, антиокислителей.
- Пастилки с цинком осуществляют санацию носоглотки, укрепляют эпителий слизистой.
- Пчелиная пыльца стимулирует физиологические процессы в органах и тканях, в составе содержит набор минералов, витаминов, белков и ненасыщенных жирных кислот.
- СиСи–Эй – композиция лечебных трав повышает иммунитет, обеспечивает защиту от патогенных микроорганизмов.
- Колострум – уникальный биогенный препарат на основе молозива, содержащий антитела против множества инфекционных болезней.
- Красный Клевер – природный стимулятор функциональной активности лимфатической системы.
- Замброза содержит соки фруктов и ягод, способных защитить клетки от свободных радикалов, разрушающих защитные силы организма.
Схема приема биологически активных препаратов, повышающих иммунитет
Источник
