Иммунитет после перенесенной чумы
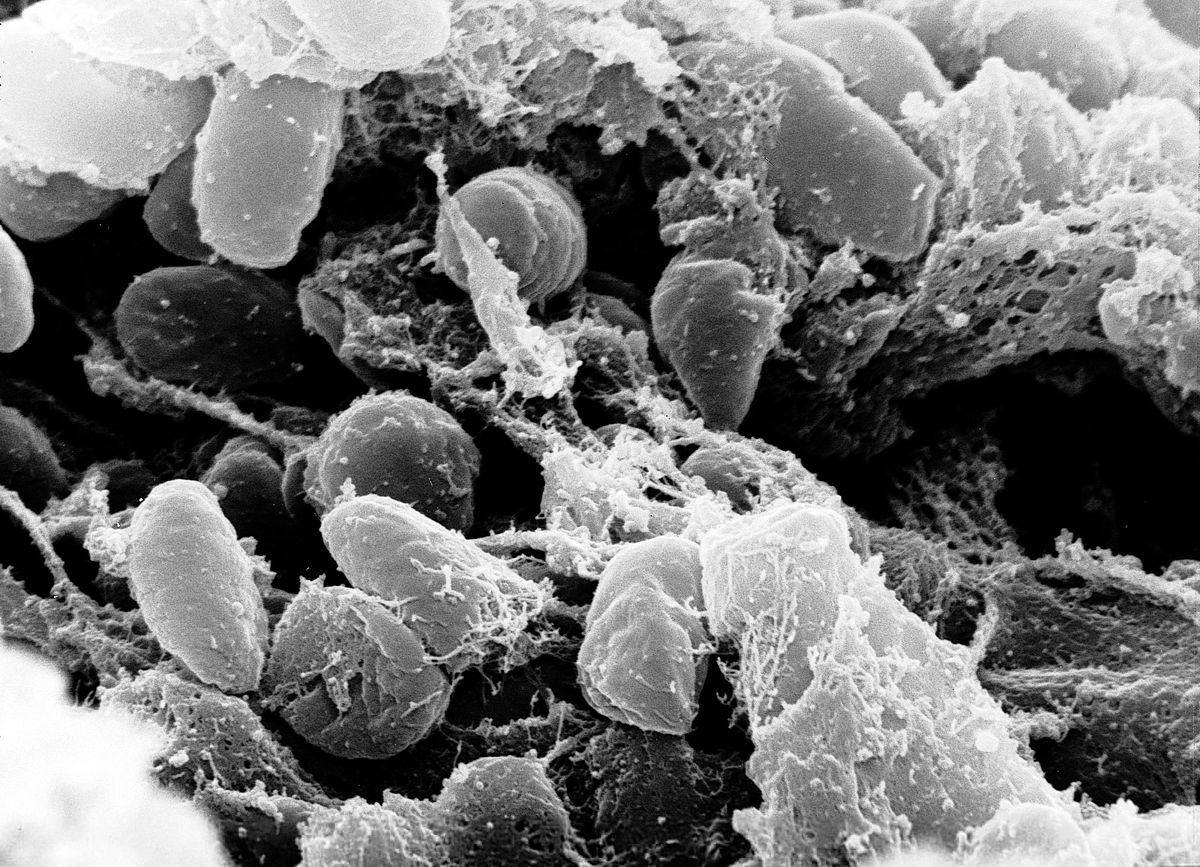
Клиника чумы у животных и человека
Краткая клиническая характеристика чумы у животных. Среди основных источников инфекции — грызунов — чума протекает либо в виде бубонов с острым течением, либо с более медленным, хроническим или латентным течением. Бактеремия наблюдается в большинстве случаев.
Как правило, летальность среди грызунов значительная, при возникновении эпизоотии они покидают свои стации и перемещаются на большие расстояния, способствуя диссеминации чумы по территории. У верблюда чума может протекать либо в виде бубонной, либо септической формы.
Основные клинические проявления чумы у человека. Инкубационный период — от нескольких часов до 1 — 2 суток, обычно не более 3—6 суток (при всех формах).
Чума протекает в виде трех основных клинико-патогенетических форм:
а) бубонной,
б) первично-септической и
в) легочной (первичной и вторичной).
Бубонная чума — наиболее часто встречающаяся форма, преобладают бедренные и паховые бубоны, которые развиваются в течение нескольких дней до размеров куриного яйца. В случае доброкачественного течения бубон нагнаивается, рассасывается или склерозируется. Опасны подмышечные бубоны, дающие септические осложнения.
Заболевание сопровождается высокой температурой, интоксикацией с поражением центральной нервной системы, падением кровяного давления. В 3—4% случаев отмечается первичный аффект на коже. Наиболее частым осложнением бубонной чумы является сепсис со вторичной пневмонией, менингитом. Чумная пневмония дает начало заражениям первично-легочной чумой. Летальность при нелеченной бубонной чуме от 30% до 50% случаев, своевременное лечение снижает этот показатель до 5—6%.
Первично-септическая форма чумы возникает при массивном заражении. Симптомы ее очень бурно развиваются — буйный бред, адинамия и прострация, геморрагическая сыпь, поражение гортани и миндалин. Смерть наступает в 100% случаев на 2—4-й день заболевания. Эта форма встречается очень редко.
Легочная форма чумы (первичная) является результатом аэрозольного заражения. Начало заболевания внезапное. Появляются озноб, боли в пояснице, конечностях, лицо красное, одутловатое, беспокойство, бред, Температура в течение нескольких часов достигает 40— 40,5°.
Отмечаются боли в груди, кашель и выделение вначале слизистой, а затем слизисто-гнойной и геморрагической мокроты во все возрастающих количествах, обычно жидкой консистенции. Перкуторно-аускультативные данные скудны, несмотря на очаги пневмонии. Больные погибают в течение 2—3 дней.
Вторичная легочная форма протекает аналогично первичной, но является осложнением бубонной чумы.
Наиболее эффективны для лечения чумы антибиотики стрептомицинового (стрептомицин, дигидрострептомицин, пасомицин) и тетрациклинового (окситетрациклин, хлортетрациклин) ряда, которые можно применять раздельно или в определенном сочетании. Вводят детоксицирующие средства (растворы глюкозы парентерально), сердечные и сосудистые медикаменты, витамины, кислород.
Картина эпидемии чумы
Иммунитет при чуме. После перенесенной чумы повторные заболевания отмечаются казуистически. Однако в этом надо усмотреть не только напряженность иммунитета, по и крайне редкую случайность повторного заражения человека.
Ведущий механизм иммунитета при чуме представляется как выработка антител и фракции I и антигена комплекса VW. Эти антигены обладают выраженной антифагоцитарной активностью, а образованные по отношению к ним сывороточные антитела (в конце первой и на второй неделе заболевания) облегчают путем опсонизации возбудителя фагоцитоз чумных палочек и внутриклеточную инактивацию микробов полиморфоядерными лейкоцитами.
На высоте иммунитета фагоцитоз носит завершенный характер, при его ослаблении — незавершенный. Последний отмечается при снижении титров антител к указанным антигенам. В то же время у лиц, выздоровевших от чумы, наблюдался относительно низкий уровень антитоксинов (фракция П), в противоположность антикапсульным антителам (фракция I), которые определялись в достаточно высоких титрах на протяжении нескольких месяцев.
Антитела к V-антигену (белковому) обладают протективным свойством, и в экспериментальных условиях защищали мышь при заражении чумными палочками; антитела к липопротеиновому W-антигену таким свойством не обладали.
Антитела к первой фракции и к токсину чумного микроба закономерно нарастают после иммунизации живой ослабленной противочумной вакциной из штамма EV. Однако наибольшее признание получила концепция о роли неспецифических факторов резистентности в формировании противочумного иммунитета, в частности фагоцитоза на уровне лимфатических узлов и местного воспалительного очага (преимущественно идет речь о бубонной чуме).
В целом иммунитет зависит от физиологической активности клеточных элементов мезодермальной ткани.
При чуме описан также феномен сенсибилизации Т-лимфоцитов (на основе иммунизации живой вакциной), наступающий закономерно и выявляемый при помощи кожной пробы с аллергеном-пестином.
Видео аудиокнига романа Чума Альбера Камю — психология и философия человека
При проблемах с просмотром скачайте видео со страницы Здесь
— Читать «Лабораторная диагностика чумы»
Оглавление темы «Зооантропонозы»:
- Клиника и диагностика кишечного иерсиниоза
- Орнитоз — история, география, возбудители
- Источник орнитоза и его резервуар
- Клиника орнитоза у птиц и человека
- Лабораторная диагностика орнитоза и его профилактика
- Чума — история, география, возбудитель
- Источник чумы и его резервуар
- Клиника чумы у животных и человека
- Лабораторная диагностика чумы
- Профилактика чумы и противоэпидемические меры
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 1 января 2020;
проверки требуют 4 правки.
Чумна́я па́лочка (лат. Yersinia pestis) — вид грамотрицательных бактерий из семейства Yersiniaceae порядка Enterobacterales.
Инфекционный агент бубонной чумы, также может вызывать чумную пневмонию и септическую чуму. Все три формы ответственны за высокий уровень смертности в эпидемиях, имевших место в истории человечества, например таких как «Юстинианова чума» (100 миллионов жертв) и «Чёрная смерть», на которой — смерть трети населения Европы за промежуток с 1347 по 1353 годы.
Роль Yersinia pestis в «Чёрной смерти» дискутируется. Некоторые утверждают, что «Чёрная смерть» распространилась слишком быстро, чтобы быть вызванной Yersinia pestis[2]. ДНК этой бактерии найдены в зубах умерших от «Чёрной смерти», тогда как тестирование средневековых останков людей, умерших по другим причинам, не дало положительной реакции на Yersinia pestis[3][4]. Это доказывает, что Yersinia pestis является как минимум сопутствующим фактором в некоторых (возможно, не во всех) европейских эпидемиях чумы. Возможно, что устроенный чумой отбор мог повлиять на патогенность бактерии, отсеяв индивидуумов, которые были наиболее ей подвержены. По последним исследованиям «Юстинианова чума» была вызвана сразу несколькими штаммами бактерии, а не одной разновидностью[5].
Род Yersinia — грамотрицательные, биполярные коккобациллы размером примерно 1.5 микрона. Обладают ферментативным метаболизмом. Y. pestis производит антифагоцитарную слизь. Подвижная в культуре бактерия становится неподвижной, попав в организм млекопитающего.
История[править | править код]
Бубонная чума. Изображение 1411 года
Y. pestis была открыта в 1894 году швейцарско-французским медиком и бактериологом Пастеровского института Александром Йерсеном во время эпидемии чумы в Гонконге. Йерсен был сторонником школы Пастера. Прошедший подготовку в Германии японский бактериолог Китасато Сибасабуро, практиковавший метод Коха, также в это время был привлечён к поискам агента, являющегося возбудителем чумы. Однако именно Йерсен фактически связал чуму с Y. pestis. Долгое время возбудителя чумы относили к роду Bacterium, позже — к роду Pasteurella. В 1967 году род бактерий, к которому относился возбудитель чумы, был переименован в честь Александра Йерсена.
В результате сравнения древних штаммов генов Yersinia pestis и её вероятного предка Yersinia pseudotuberculosis (псевдотуберкулезная палочка) было выявлено, что Yersinia pestis мутировала из сравнительно безвредного микроорганизма около 10 тысяч лет назад. Выяснилось, что обитающая в почве Y. pseudotuberculosis, вызывающая легкое заболевание желудочно-кишечного тракта, приобрела тогда несколько генов, позволивших ей проникать в легкие человека. Далее, в ключевом гене Pla произошла замена одной аминокислоты, в результате чего микроорганизм смог с повышенной силой разлагать белковые молекулы в легких и размножаться по всему организму через лимфатическую систему.
Исследователи подозревают, что ген Pla чумная палочка позаимствовала у другого микроба в результате горизонтального обмена генами[6][7]. Это подтверждают и исследования датских и британских ученых, которые провели исследования молекул ДНК, извлеченных из зубов 101 человека бронзового века, обнаруженных на территории Евразии (от Польши до Сибири). Следы бактерии Y. pestis нашли в ДНК семерых, возрастом до 5783 лет, при этом в шести из этих образцов отсутствовали «ген вирулентности» ymt и мутации в «гене активации» pla. В дальнейшем, на рубеже второго и первого тысячелетия до нашей эры, из-за демографических условий, выразившихся в увеличении плотности населения, возникла более летальная «бубонная» мутация бактерии[8][9].
Известны три биовара бактерии; полагают, что каждый соответствует одной из исторических пандемий чумы. Биовар antiqua считают ответственным за «Юстинианову чуму». Неизвестно, был ли этот биовар причиной более ранних, меньших эпидемий, или же эти случаи вообще не были эпидемиями чумы. Биовар medievalis полагают связанным с «Чёрной смертью». Биовар orientalis связывают с Третьей пандемией и большинством современных вспышек чумы.
В настоящее время только в России с 2001 по 2006 год зафиксировано 752 штамма возбудителя чумы[10].
Патогенность и иммунитет[править | править код]
Патогенность Yersinia pestis заключается в двух антифагоцитарных антигенах, называемых F1 и VW, оба существенны для вирулентности[11]. Эти антигены производятся бактерией при температуре 37 °C. Кроме этого, Y. pestis выживает и производит F1 и VW антигены внутри кровяных клеток, таких, например, как моноциты, исключением являются полиморфно-ядерные нейтрофильные гранулоциты[12].
Некоторое время назад в США инактивированная формалином вакцина была доступна для взрослых, находящихся под большим риском заражения, однако затем продажи были прекращены по указанию FDA, специального агентства министерства здравоохранения США, по причине низкой эффективности и вероятности серьёзного воспаления. Ведутся перспективные эксперименты в генной инженерии по созданию вакцины, основанной на антигенах F1 и VW, хотя бактерии не имеющие антигена F1 сохраняют достаточную вирулентность, а антигены V достаточно изменчивы, так что вакцинация, основанная на этих антигенах может не давать достаточно полной защиты[13].
В России доступна живая вакцина на основе невирулентного штамма чумы[14].
Вакцинация не защищает от легочной чумы. Во время эпидемии 1910—1911 года применение прочумных сывороток (лимфы Хавкина и сыворотки Йерсена) лишь продлевало течение болезни на несколько дней, но не спасло жизнь ни одному больному[15]. Впоследствии ученым окончательно стало ясно, что гуморальный иммунитет при аэрогенном инфицировании возбудителем чумы значения не имеет[16].
После перенесенного заболевания остается прочный продолжительный иммунитет.[17]
Геном[править | править код]
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM (из биовара Medievalis)[18], штамма CO92 (из биовара Orientalis, полученного из клинического изолятора в США)[19], штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755 парных оснований, в штамме CO92 — 4 653 728 парных оснований. Как и родственные Y. pseudotuberculosis и Y. enterocolitica, бактерия Y. pestis содержит плазмиды pCD1. Вдобавок, она также содержит плазмиды pPCP1 и pMT1, которых нет у других видов рода Yersinia. Перечисленные плазмиды и остров патогенности, названный HPI, кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина», вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов.
Древняя ДНК[править | править код]
В 2018 году в останках женщины из шведского местонахождения Frälsegården, умершей около 4900 лет назад (неолит) была обнаружена ДНК Yersinia pestis. Геном штамма из шведского захоронения выделился около 5700 лет назад, две ветви существующих сегодня штаммов Y. pestis выделились 5100 и 5300 лет назад[20].
ДНК Yersinia pestis найдена в останках двух человек из Самарской области, связанных со срубной культурой (около 3800 лет назад) и в останках человека из Капана (Армения), жившего в железном веке около 2900 лет назад[21].
Лечение[править | править код]
С 1947 года традиционным средством первого этапа лечения от Y. pestis были стрептомицин[22][23], хлорамфеникол или тетрациклин[24]. Также есть свидетельства положительного результата от использования доксициклина или гентамицина[25].
Надо заметить, что выделены штаммы, устойчивые к одному или двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
Примечания[править | править код]
- ↑ Genus Yersinia : [англ.] // LPSN[en]. (Проверено 9 декабря 2018).
- ↑ Ал Бухбиндер. Между чумой и эболой Архивная копия от 11 января 2018 на Wayback Machine — в статье, напечатанной в журнале «Знание—Сила» № 2 за 2002 год приводятся размышления, критикующие связь бактерии с чумой.
- ↑ Drancourt M., Aboudharam G., Signolidagger M., Dutourdagger O., Raoult D. Detection of 400-year-old Yersinia pestis DNA in human dental pulp: An approach to the diagnosis of ancient septicemia (англ.) // Proceedings of the National Academy of Sciences : journal. — National Academy of Sciences, 1998. — Vol. 95, no. 21. — P. 12637—12640.
- ↑ Drancourt M., Raoult D. Molecular insights into the history of plague (неопр.) // Microbes Infect.. — 2002. — Т. 4. — С. 105—109.
- ↑ Researchers discover bacterial diversity in Justinianic Plague. Дата обращения 6 июня 2019.
- ↑ Чума возникла благодаря случайной мутации. Lenta.ru. Дата обращения 23 октября 2015.
- ↑ Daniel L. Zimbler, Jay A. Schroeder, Justin L. Eddy & Wyndham W. Lathem. Early emergence of Yersinia pestis as a severe respiratory pathogen. nature.com. Дата обращения 13 февраля 2016.
- ↑ Древняя форма чумы оказалась неизвестным виновником катастроф бронзового века. Lenta.ru. Дата обращения 23 октября 2015.
- ↑ Simon Rasmussen. Early Divergent Strains of Yersinia pestis in Eurasia 5,000 Years Ago. cell.com. Дата обращения 13 февраля 2016.
- ↑ Приказ территориального управления Роспотребнадзора по МО от 02.05.2006 N 100 «Об организации и проведении мероприятий по профилактике чумы на территории Московской области»
- ↑ Collins F. M. Pasteurella, Yersinia, and Francisella. In: Barron’s Medical Microbiology (Barron S et al, eds.) (неопр.). — 4th ed.. — Univ of Texas Medical Branch, 1996.
- ↑ Salyers A. A., Whitt D. D. Bacterial Pathogenesis: A Molecular Approach (англ.). — 2nd ed.. — ASM Press (англ.)русск., 2002. — P. 207—212.
- ↑ Welkos S . et al. Determination of the virulence of the pigmentation-deficient and pigmentation-/plasminogen activator-deficient strains of Yersinia pestis in non-human primate and mouse models of pneumonic plague (англ.) // Vaccine (англ.)русск. : journal. — Elsevier, 2002. — Vol. 20. — P. 2206—2214.
- ↑ Вакцина чумная живая сухая (Vaccine plague).
- ↑ Супотницкий М. В., Супотницкая Н. С. Очерки истории чумы. Очерк XXXI. Эпидемия легочной чумы в Манжурии и забайкалье (1910—1911). — 2006.
- ↑ Супотницкий М. В., Супотницкая Н. С. Очерки истории чумы. Очерк XXXV. Эпидемии чумы в Маньчжурии в 1945—1947 гг. — перелом в лечении и в профилактике чумы. — 2006.
- ↑ «Профилактика чумы» Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека — федеральная служба Российской Федерации
- ↑ Deng W. et al. Genome Sequence of Yersinia pestis KIM (англ.) // American Society for Microbiology (англ.)русск.. — American Society for Microbiology (англ.)русск., 2002. — Vol. 184, no. 16. — P. 4601—4611.
- ↑ Parkhill J . et al. Genome sequence of Yersinia pestis, the causative agent of plague (англ.) // Nature : journal. — 2001. — Vol. 413. — P. 523—527.
- ↑ Nicolás Rascovan et al. Emergence and Spread of Basal Lineages of Yersinia pestis during the Neolithic Decline, 2018
- ↑ Derbise, A; Chenal-Francisque, V; Pouillot, F; Fayolle, C; Prévost, MC; Médigue, C; Hinnebusch, BJ; Carniel, E. A horizontally acquired filamentous phage contributes to the pathogenicity of the plague bacillus (англ.) // Mol Microbiol : journal. — 2007. — Vol. 63, no. 4. — P. 1145—1157. — doi:10.1111/j.1365-2958.2006.05570.x. — PMID 17238929.
- ↑ Wagle PM. Recent advances in the treatment of bubonic plague (неопр.) // Indian J Med Sci. — 1948. — Т. 2. — С. 489—494.
- ↑ Meyer KF. Modern therapy of plague (англ.) // JAMA. — 1950. — Vol. 144. — P. 982—985.
- ↑ Kilonzo B.S., Makundi R.H., Mbise TJ. A decade of plague epidemiology and control in the Western Usambara mountains, north-east Tanzania (англ.) // Acta Tropica : journal. — 1992. — Vol. 50. — P. 323—329.
- ↑ Mwengee W., Butler T., Mgema S., et al. Treatment of plague with gentamicin or doxycycline in a randomized clinical trial in Tanzania (англ.) // Clin Infect Dis : journal. — 2006. — Vol. 42. — P. 614—621.
Литература[править | править код]
- Козлов М. П. Чума (природная очаговость, эпизоотология, эпидемические проявления). — М.: Медицина, 1979. — 192 с.
- Кошель Елена Ивановна. Образование биопленки штаммами Yersinia pestis разных подвидов и их взаимодействие с членами почвенных биоценозов : Автореферат диссертации на соискание учёной степени кандидата биологических наук. — Саратов, 2014. — 22 с.
- Кутырев В. В.; Ерошенко Г. А.; Попов Н. В.; Видяева Н. А.; Коннов Н. П. Молекулярные механизмы взаимодействия возбудителя чумы с беспозвоночными животными // Молекулярная генетика, микробиология и вирусология. — 2009. — № 4. — С. 6—13 : 6 рис. — Библиогр.: с. 12—13 (39 назв.). — ISSN 0208-0613.
Ссылки[править | править код]
- Сложный паразитарный биоценоз: молекулярно-генетические основы взаимодействия возбудителя чумы с организмами хладнокровных и теплокровных животных.
- Молекулярные основы экологии возбудителя чумы.
Содержание
- Чума
- Характеристика возбудителя
- Классификация чумы
- Симптомы чумы
- Диагностика чумы
- Лечение чумы
- Прогноз при чуме
- Профилактика чумы
Чума – высококонтагиозная бактериальная инфекция с множественными путями передачи и эпидемическим распространением, протекающая с лихорадочно-интоксикационным синдромом, поражением лимфоузлов, легких и кожи. Клиническому течению различных форм чумы свойственна высокая лихорадка, тяжелая интоксикация, возбуждение, мучительная жажда, рвота, регионарный лимфаденит, геморрагическая сыпь, ДВС-синдром, а также свои специфические симптомы (некротические язвы, чумные бубоны, ИТШ, кровохарканье). Диагностика чумы осуществляется лабораторными методами (бакпосев, ИФА, РНГА, ПЦР). Лечение проводится в условиях строгой изоляции: показаны тетрациклиновые антибиотики, дезинтоксикация, патогенетическая и симптоматическая терапия.
Чума
Чума представляет собой острое инфекционное заболевание, передающееся преимущественно по трансмиссивному механизму, проявляющееся воспалением лимфоузлов, легких, других органов, имеющим серозно-геморрагический характер, либо протекающее в септической форме. Чума относится к группе особо опасных инфекций.
Чума относится к группе особо опасных инфекций. В прошлом пандемии «черной смерти», как называли чуму, уносили миллионы человеческих жизней. В истории описаны три глобальных вспышки чумы: в VI в. в Восточной Римской империи («юстинианова чума»); в XIV в. в Крыму, Средиземноморье и Западной Европе; в к. XIX в. в Гонконге. В настоящее время благодаря разработке эффективных противоэпидемических мероприятий и противочумной вакцины регистрируются лишь спорадические случаи инфекции в природных очагах. В России к эндемичным по чуме районам относятся Прикаспийская низменность, Ставрополье, Восточный Урал, Алтай и Забайкалье.
Характеристика возбудителя
Yersinia pestis представляет собой неподвижную факультативно-анаэробную грамотрицательную палочковидную бактерию из рода энтеробактерий. Чумная палочка может длительно сохранять жизнеспособность в отделяемом больных людей, трупах (в бубонном гное иерсинии живут до 20-30 дней, в трупах людей и павших животных – до 60 дней), переносит замораживание. К факторам внешней среды (солнечные лучи, атмосферный кислород, нагревание, изменение кислотности среды, дезинфекция) эта бактерия довольно чувствительна.
Резервуар и источник чумы – дикие грызуны (сурки, полевки, песчанки, пищухи). В различных природных очагах резервуаром могут служить разные виды грызунов, в городских условиях – преимущественно крысы. Резистентные к человеческой чуме собаки могут служить источником возбудителя для блох. В редких случаях (при легочной форме чумы, либо при непосредственном соприкосновении с бубонным гноем) источником инфекции может стать человек, блохи также могут получать возбудителя от больных септической формой чумы. Нередко заражение происходит непосредственно от чумных трупов.
Чума передается при помощи разнообразных механизмов, ведущее место среди которых занимает трансмиссивный. Переносчиками возбудителя чумы являются блохи и клещи некоторых видов. Блохи заражают животных, которые переносят возбудителя с миграцией, распространяя также блох. Люди заражаются при втирании в кожу при расчесах экскрементов блох. Насекомые сохраняют заразность около 7 недель (имеются данные о контагиозности блох на протяжении года).
Заражение чумой также может происходить контактным путем (через поврежденные кожные покровы при взаимодействии с мертвым животными, разделке туш, заготовке шкур и др.), алиментарно (при употреблении мяса больных животных в пищу).
Люди обладают абсолютной естественной восприимчивостью к инфекции, заболевание развивается при заражении любым путем и в любом возрасте. Постинфекционный иммунитет относительный, от повторного заражения не защищает, однако повторные случаи чумы обычно протекают в более легкой форме.
Классификация чумы
Чума классифицируется по клиническим формам в зависимости от преимущественной симптоматики. Различают локальные, генерализованные и внешнедиссеминированные формы. Локальная чума подразделяется на кожную, бубонную и кожно-бубонную, генерализованная чума бывает первично- и вторично-септической, внешнедиссеминированная форма подразделяется на первично- и вторично-легочную, а также – кишечную.
Симптомы чумы
Инкубационный период чумы в среднем занимает около 3-6 суток (максимально до 9 дней). При массовых эпидемиях или в случае генерализованных форм инкубационный период может укорачиваться до одного – двух дней. Начало заболевания острое, характеризуется быстрым развитием лихорадки, сопровождающейся потрясающим ознобом, выраженным интоксикационным синдромом.
Больные могут жаловаться на боль в мышцах, суставах, крестцовой области. Появляется рвота (часто – с кровью), жажда (мучительная). С первых же часов больные пребывают в возбужденном состоянии, могут отмечаться расстройства восприятия (бред, галлюцинации). Нарушается координация, теряется внятность речи. Заметно реже возникают вялость и апатия, больные ослабевают вплоть до невозможности подняться с постели.
Лицо больных одутловато, гиперемировано, склеры инъецированы. При тяжелом течении отмечаются геморрагические высыпания. Характерным признаком чумы является «меловой язык» — сухой, утолщенный, густо покрытый ярким белым налетом. Физикальное обследование показывает выраженную тахикардию, прогрессирующую артериальную гипотензию, одышку и олигурию (вплоть до анурии). В начальный период чумы эта симптоматическая картина отмечается при всех клинических формах чумы.
Кожная форма проявляется в виде карбункула в области внедрения возбудителя. Карбункул прогрессирует, проходя последовательно следующие стадии: сначала на гиперемированной, отечной коже образуется пустула (выражено болезненная, наполнена геморрагическим содержимым), которая после вскрытия оставляет язву с приподнятыми краями и желтоватым дном. Язва склонна увеличиваться. Вскоре в ее центра образуется некротический черный струп, быстро заполняющий все дно язвы. После отторжения струпа карбункул заживает, оставляя грубый рубец.
Бубонная форма является наиболее распространенной формой чумы. Бубонами называют специфически измененные лимфатические узлы. Таким образом, при этой форме инфекции преимущественным клиническим проявлением выступает регионарный в отношении области внедрения возбудителя гнойный лимфаденит. Бубоны, как правило, единичны, в некоторых случаях могут быть множественными. Первоначально в области лимфоузла отмечается болезненность, спустя 1-2 дня при пальпации обнаруживаются увеличенные болезненные лимфатические узлы, сначала плотные, при прогрессировании процесса размягчающиеся до тестообразной консистенции, сливаясь в единый спаянный с окружающими тканями конгломерат. Дальнейшее течение бубона может вести как к его самостоятельному рассасыванию, так и к формированию язвы, области склерозирования или некроза. Разгар заболевания продолжается с течение недели, затем наступает период реконвалесценции, и клиническая симптоматика постепенно стихает.
Кожно-бубонная форма характеризуется сочетанием кожных проявлений с лимфаденопатией. Локальные формы чумы могут прогрессировать во вторично-септическую и вторично-легочную форму. Клиническое течение этих форм не отличается от их первичных аналогов.
Первично-септическая форма развивается молниеносно, после укороченной инкубации (1-2 дня), характеризуется быстрым нарастанием тяжелой интоксикации, выраженным геморрагическим синдромом (многочисленными геморрагиями в кожных покровах, слизистых оболочках, конъюнктиве, кишечными и почечными кровотечениями), скорым развитием инфекционно-токсического шока. Септическая форма чумы без должной своевременной медицинской помощи заканчивается смертью.
Первично-лёгочная форма возникает в случае аэрогенного пути заражения, инкубационный период при этом также сокращается, может составлять несколько часов или продолжаться о двух дней. Начало острое, характерное для всех форм чумы – нарастающая интоксикация, лихорадка. Легочная симптоматика проявляется ко второму – третьему дню заболевания: отмечается сильный изнуряющий кашель, сначала с прозрачной стекловидной, позднее — с пенистой кровянистой мокротой, имеет место боль в груди, затруднение дыхания. Прогрессирующая интоксикация способствует развитию острой сердечно-сосудистой недостаточности. Исходом этого состояния может стать сопор и последующая кома.
Кишечная форма характеризуется интенсивными резкими болями в животе при тяжелой общей интоксикации и лихорадке, вскоре присоединяется частая рвота, диарея. Стул обильный, с примесями слизи и крови. Нередко – тенезмы (мучительные позывы к дефекации). Учитывая широкое распространение других кишечных инфекций, в настоящее время так и не решен вопрос: является ли кишечная чума самостоятельной формой заболевания, развившейся в результате попадания микроорганизмов в кишечник, или она связана с активизацией кишечной флоры.
Диагностика чумы
Ввиду особой опасности инфекции и крайне высокой восприимчивости к микроорганизму, выделение возбудителя производится в условиях специально оборудованных лабораторий. Забор материала производят из бубонов, карбункулов, язв, мокроты и слизи из ротоглотки. Возможно выделение возбудителя из крови. Специфическую бактериологическую диагностику производят для подтверждения клинического диагноза, либо, при продолжительной интенсивной лихорадке у больных, в эпидемиологическом очаге.
Серологическая диагностика чумы может производиться с помощью РНГА, ИФА, РНАТ, РНАГ и РТПГА. Возможно выделение ДНК чумной палочки с помощью ПЦР. Неспецифические методы диагностики — анализ крови, мочи (отмечается картина острого бактериального поражения), при легочной форме — рентгенография легких (отмечаются признаки пневмонии).
Лечение чумы
Лечение производится в специализированных инфекционных отделениях стационара, в условиях строгой изоляции. Этиотропная терапия проводится антибактериальными средствами в соответствии с клинической формой заболевания. Продолжительность курса занимает 7-10 дней.
При кожной форме назначают ко-тримоксазол, при бубонной – внутривенно хлорамфеникол со стрептомицином. Можно также применять антибиотики тетрациклинового ряда. Тетрациклином или доксициклином дополняется комплекс хлорамфеникола со стрептомицином при чумной пневмонии и сепсисе.
Неспецифическая терапия включает комплекс дезинтоксикационных мероприятий (внутривенная инфузия солевых р-ров, декстрана, альбумина, плазмы) в сочетании с форсированием диуреза, средства, способствующие улучшению микроциркуляции (пентоксифиллин). При необходимости назначаются сердечно-сосудистые, бронхолитические средства, жаропонижающие препараты.
Прогноз при чуме
В настоящее время в условиях современных стационаров при применении антибактериальных средств смертность от чумы довольно низка – не боле 5-10%. Ранняя медицинская помощь, предотвращение генерализации способствуют выздоровлению без выраженных последствий. В редких случаях развивается скоротечный чумной сепсис (молниеносная форма чумы), плохо поддающийся диагностированию и терапии, нередко заканчивающийся скорым летальным исходом.
Профилактика чумы
В настоящее время в развитых странах инфекция практически отсутствует, поэтому основные профилактические мероприятия направлены на исключение завоза возбудителя из эпидемиологически опасных регионов и санацию природных очагов. Специфическая профилактика заключается в вакцинации живой чумной вакциной, производится населению в районах с неблагоприятной эпидемиологической обстановкой (распространенность чумы среди грызунов, случаи заражения домашних животных) и лицам, отправляющимся в регионы с повышенной опасностью заражения.
Выявления больного чумой является показанием к принятию срочных мер по его изолированию. При вынужденных контактах с больными используют средства индивидуальной профилактики – противочумные костюмы. Контактные лица наблюдаются в течение 6 дней, в случае контакта с больным легочной формой чумы производится профилактическая антибиотикотерапия. Выписка больных из стационара производится не ранее 4 недель после клинического выздоровления и отрицательных тестов на бактериовыделительство (при легочной форме – после 6 недель).
