Иммунитет при грибковых инфекциях
Оглавление темы «Клеточные имунные реакции. Иммунная память. Иммунное реагирование при инфекциях. Иммунодефициты.»:
1. Клеточные имунные реакции. Индукция Т-клеточно-опосредованных реакций. Клеточный иммунитет.
2. Уничтожение клетки-мишени цитотоксическими Т лимфоцитами. Альтернативный механизм уничтожения клетки-мишени. Реакции ГЗТ. Реакции гиперчувствительности замедленного типа.
3. Иммунная память. Бустер эффект. Вакцинопрофилактика.
4. Иммунное реагирование при инфекциях. Иммунный ответ при вирусных инфекциях. Гуморальные иммунные реакции при вирусемии ( вирусных инфекциях ).
5. Клеточные иммунные реакции при вирусных инфекциях. Иммунный ответ при бактериальных инфекциях.
6. Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
7. Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.
8. Толерантность иммунитета. Устойчивость иммунной системы. Механизмы поддержания толерантности иммунитета.
9. Естественная толерантность иммунитета. Искусственная толерантность иммунной системы. Иммунный паралич. Расщеплённая толерантность иммунитета. Нарушения толерантности иммунной системы. Аутоимунные заболевания.
10. Иммунодепрессивное состояние. Иммунодефициты. Врождённые иммунодефициты. Гиперкортицизм ( синдром Кушинга ). Двусторонняя гиперплазия коры надпочечников ( болезнь Иценко-Кушинга ) при иммунодефицитах. Ионизирующая радиация и иммунодефицит.
Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
Грибковые клетки и их продукты — сильные иммуногены. Их распознавание иммунной системой проявляется в виде клеточных и гуморальных реакций. Многие грибковые Аг проявляют сенсибилизирующее действие, поэтому аллергический компонент — важное звено патогенеза микозов. Однако при микозах сенсибилизация не строго специфична, не отражает уровня иммунного реагирования и нередко не имеет прогностическое значение. Патогенные грибы содержат большой набор Аг.
Гуморальные реакции иммунитета при грибковых инфекциях
Большинство грибковых поражений сопровождается образованием высоких титров AT. Вид AT и нарастание концентрации отражают статус и прогрессирование инфекции. При микозах образуются высокие титры AT классов IgM, IgG и IgA; при сенсибилизирующем действии грибковых Аг дополнительно образуются IgE. Значение цитотоксического действия AT в комплементзависимом цитолизе невелика, так как комплемент непосредственно действует на грибковую клетку, активирующую его по классическому и альтернативному пути. Сложность антигенной структуры возбудителей микозов приводит к появлению значительного пула AT, не участвующих напрямую в уничтожении возбудителя и не проявляющих строгой видоспецифичности.

Клеточный иммунитет при грибковых инфекциях
Клеточные реакции играют основную роль в элиминации патогенных грибов. Исключая поверхностные микозы (где нет контакта между Аг и иммунокомпетентными клетками), у заражённых лиц развивается реакция ГЗТ, обнаруживаемая уже через 10-14 сут.
Предполагается, что основная роль в формировании резистентности принадлежит именно клеточным реакциям, но клинических данных, подтверждающих это положение, нет. В эксперименте показана важная роль ЦТЛ, так как их перенос сингенным реципиентам (клетки или организмы с идентичным набором Аг МНС) приводит к состоянию резистентности; участие Т-хелперов реализуется в активации клеток макрофагально-моноцитарной системы и полиморфноядерных клеток (при респираторных микозах) и стимуляции их фагоцитарной активности.
В ряде случаев иммунные реакции не только не препятствуют, но и способствуют развитию патологических реакций (гиперчувствительность, аутоиммунные поражения), что приводит к хроническому, рецидивирующему течению многих микозов.
— Также рекомендуем «Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.»
Автор Камуллина Анна Евгеньевна На чтение 6 мин. Просмотров 2.1k. Опубликовано 01.08.2019
Данный паразит размножается с помощью спор или мицелия. У него нет белковых сигнатур (фрагментов ДНК), по которым защитные тела обычно определяют и запоминают возбудителей «животного» типа – бактерии, вирусы, микроорганизмы. Потому противогрибковый иммунитет не вырабатывается даже после многократных заражений. Но разово и в зависимости от того, какие ткани были задеты, система резистентности способна остановить его распространение.
Противогрибковый иммунитет: что это такое?
Инфекции этого типа называются микозами, их могут провоцировать свыше 30 видов грибков. У некоторых есть своя «специализация», а некоторые всеядны и вызывают системные микозы. Наибольшей устойчивостью к ним среди всех органов тела отличается кожа.

Грибкам, как и любым растениям, кровоснабжение не нужно – достаточно только тепла, влаги и питательной среды, в роли которой выступают клетки тела. Кожа способна сопротивляться распространению грибковых инфекций благодаря:
- кислому балансу пота и кожного жира – он неблагоприятен для разрастания мицелия;
- блокирующим свойствам кожного жира – он связывает споры еще до контакта с эпидермисом;
- кератиноцитам – многофункциональным клеткам, ответственным за регенерацию, устойчивость кожи к механическим воздействиям, удержание в ней влаги, синтез медиаторов, запускающих воспаление в месте инфекции;
- клеткам Лангерганса – кожной разновидности макрофагов (поглощают возбудителя и переносят его в лимфоузлы для «знакомства» с внутриклеточными «инспекторами» лимфоцитами).
Ногти и волосы подвержены грибковым инфекциям намного сильнее, поскольку образующие их кератиноциты в одиночку с возбудителем не справятся, а «позвать на помощь» другие иммунные агенты они не могут из-за отсутствия кровоснабжения.
Помимо поверхности эпидермиса, грибки также могут попасть в ротовую полость и пищеварительный тракт с пищей или загрязненными пальцами/ногтями, в дыхательную систему – с воздухом. Желудок защищает от них себя и кишечник с помощью резко кислой среды, а щелочная благоприятна для их размножения.
Ротовой полости и пищеводу тоже нечего противопоставить им, кроме слюны с ее слабым расщепителем полисахаридов птиалином. Бронхи и легкие защищены от возбудителей различных типов, но размножающиеся спорами грибки составляют несчастливое исключение из списка. Их с трудом удается связать только слизью бронхов. А удалить их из легких при кашле или блокировать с помощью антител в легочном круге кровообращения невозможно.
Почему ослабевает?
Заражение грибами внутренних органов всегда носит вторичный характер. Несмотря на наличие ряда пробелов в «познаниях» медицины об иммунитете и его механизмах, уже доказано, что максимальную эффективность против них дают:
Народными средствами
35.45%
Проголосовало: 110
- ПМЯЛ – полиморфноядерные лейкоциты (фагоциты);
- Т-лимфоциты;
- NK-лимфоциты.
Лимфоциты являются тельцами лимфы и «родными братьями» лейкоцитов крови, способными, в отличие от них, проникать внутрь клеток. Они зарождаются и обучаются в тимусе – вилочковой железе, расположенной за грудинной костью. Их особенность как одного из иммунных звеньев заключается в почти полном отсутствии «аппетита» на только попавшие в организм вирусы с бактериями.
Лимфоциты исследуют клетки на наличие любых отклонений в структуре и уничтожают подобные «находки». А уже среди спровоцировавших агрессию лимфоцитов дефектов на равных могут оказаться ДНК вируса, встроенная в код клетки, простейшее или микроорганизм, прячущиеся за ее мембраной от прочих защитных тел, врожденный порок развития. Лимфоцитарную защиту еще часто называют клеточной. Она служит единственным для тела средством избавления от потенциально злокачественных клеток и внутриклеточных инфекций. Лимфо- и фагоцитарный иммунитет может ухудшиться из-за:
- наследственных иммунодефицитов;
- ВИЧ-инфекции;
- заражения вирусом герпеса (размножается в В-лимфоцитах);
- длительной работы «на износ» (особенно физической и/или сопровождающейся недоеданием);
- голода (включая диеты, дефицит животных продуктов и вегетарианство);
- сахарного диабета;
- радиоактивного облучения (особенно тимуса, что может спровоцировать и злоупотребление рентгеном грудной клетки);
- хронического стресса;
- приема иммунодепрессантов;
- терапии антибиотиками;
- химиотерапии.
Другая сторона вопроса в том, что даже нормальное функционирование указанных звеньев иммунитета не гарантирует от заражения грибами. Так, споры криптококков защищены от поглощения защитными агентами капсулой, а гистоплазмы упорны к попыткам их разрушить. Кокцидии же сами способны захватывать и уничтожать атаковавшие их тела.
Как повысить противогрибковый иммунитет?
Приблизительная норма содержания лимфоцитов в кровотоке равна 32-40%. Повышенный (не больше 46-48%) лимфоцитоз – еще не повод для беспокойства. Такое случается при ряде инфекций, беременности, у лиц с удаленной селезенкой, питающихся однообразно, недавно перенесших хирургическое вмешательство.

Главное здесь – убедиться, что он не злокачественный (есть отдельная форма рака лимфатической системы – лимфома). А вот пониженный (меньше 18%) указывает на растущий риск рака других тканей, грибковой и герпесвирусной инфекции. Его повышению способствует употребление в пищу:
- животных белков. Лимфоциты состоят из белков и строятся из аминокислот. Животный белок содержит их все, а растительный – только часть. Потому вегетарианство иммунитет определенно не укрепляет;
- ретинола. Или его предшественников каротинов. Витамином А богаты морковь, шпинат, курага, тыква, салат. Он усваивается, только будучи растворенным в любом жире. В день нужно съедать около 300 г моркови или 400-500 г – остальных продуктов (норма витамина в сутки – 100 000 МЕ);
- токоферола. Витамин Е также жирорастворим, а самым известным продуктом среди богатых им является растительное масло, особенно подсолнечное. Подойдут также семечки и орехи всех видов, белокочанная капуста, спаржа, авокадо, манго. Суточная норма токоферола составляет 100 мг, достичь ее можно со 150 мл растительных масел или примерно 450 г овощей/фруктов в день.
- цинка. Его одинаково часто можно встретить в растительных и животных продуктах – фасоли, говядине и индюшатине, злаках, устрицах и крабовом мясе. Суточная норма цинка составляет 11 мг, получить ее можно с 300 г и больше указанных продуктов;
- селена. Им богаты медуница лекарственная, чеснок, тунец, мясо краба, устрицы. В сутки его требуется примерно 60 мкг – около 250 г указанных продуктов.
Профилактика
Особенности противогрибкового иммунитета не исчерпываются лимфоцитарной защитой. Большая часть микопаразитов хорошо размножаются на коже благодаря оптимальным условиям – влаге, темноте и теплу. Оттого кожный грибок и предпочитает области между пальцами, в подмышечных впадинах, под молочными железами. А значит, в борьбе с грибками также важно:
- соблюдать идеальную гигиену кожи (пораженные участки можно обрабатывать слабыми антисептиками, начиная с уксуса и заканчивая хлоргексидином), одежды и обуви (глажка, включая носки, обработка паром, сушка);
- чаще загорать (в том числе, в солярии);
- не касаться здоровых участков кожи пальцами и предметами, которые только что контактировали с очагами инфекции;
- отказаться от спиртного – вредного для печени и повышающего температуру кожи наряду с потливостью.
В целях предупреждения инфекций не следует колоть дрова или разбирать завалы из трухлявого дерева голыми руками, без респиратора. Требует осторожности и контакт с сеном, особенно прошлогодним. Плесень на стенах комнат, включая ванную, или кранах, раковине, в других типичных местах следует своевременно протравливать с помощью хлора и альтернативных моющих средств. При ослабленном лимфоцитарном иммунитете к употреблению в пищу не допускаются плесневые сыры и продукты, изготовленные путем сбраживания (в том числе, квас, пиво и свежий хлеб), жирная ухаживающая косметика.
За последние два десятилетия тревожными темпами росла заболеваемость грибковыми инфекциями. Большая часть этого роста обусловлена оппортунистическими грибковыми инфекциями, связанными с ростом численности людей с ослабленной иммунной системой из-за ВИЧ, рака и других заболеваний и современной медицинской практикой, такой как использование интенсивной химиотерапии и препаратов, подавляющих иммунную систему
 грибковые инфекции
грибковые инфекции
Грибы везде — они растут в домах и на еде, как на дрожжах, они найдены в еде и в наших телах. Какую бы форму не принимали грибы, они выживают, расщепляя органические вещества. Только 180 из 250 000 известных видов грибов могут вызывать заболевания у людей.
Оппортунистическая инфекция вызывается организмом, которая обычно живет в нашем теле или окружающей среде. Она не наносит никакого ущерба, но использует возможность, которую дает ослабленная иммунная система, чтобы вызвать болезнь.
Много различных видов грибков живут внутри человеческого тела в мирном равновесии с ним. Когда иммунная система тела ослаблена из-за болезни, такой как СПИД или лечение, как химиотерапия, баланс может быть нарушен, позволяя грибкам вызывать болезнь. Такие заболевания называют оппортунистическими инфекциями.
Люди чаще всего контактируют с грибами в естественной среде обитания организмов. Садоводы часто в опасности из-за грибковых инфекций, потому что много грибков живет в земле. Патогены могут проникать в организм человека через босые ноги, руки или другие открытые участки. Различные виды грибов живут и процветают в разных географических районах.
Часто бывает трудно диагностировать системные грибковые инфекции. Много раз они подтверждаются только при вскрытии. Поскольку многие системные грибковые инфекции остаются необнаруженными и необработанными, противогрибковая терапия имеет смешанный успех.
Существует целый ряд инфекций, вызванных грибками, в том числе:
Поверхностные
Кандида — это дрожжи, которые распространены в людях — сотни тысяч из них мирно живут в нашем организме. Они находятся на поверхности слизистых оболочек полости рта, кишечника и женской половой системы. Большинство инфекций кандиды происходят на одной из этих трех поверхностей. Эти инфекции обычно можно лечить противогрибковыми препаратами, но устойчивость к лекарственным препаратам становится все более распространенной, что делает эти инфекции более трудными для лечения. Кандида может также причинить более серьезные внутренние инфекции.Грибы, вызывающие инфекции у людей, делятся на три группы: дрожжи, плесень и дерматофиты. Большинство из них плесневые, но есть и много болезнетворных дрожжей. Некоторые грибы являются высоко патогенными и могут вызвать системную инфекцию у людей, подвергшихся их воздействию. Другие могут вызвать заболевание, только когда иммунная система слаба.
Эти инфекции являются оппортунистическими и происходят, когда среда в организме становится благоприятной для организма, чтобы расти и распространяться. Это может произойти, например, когда кого-то лечат антибиотиками. В этом случае, грибки, которые конкурируют за питательные вещества с бактериями в организме, могут быстро размножиться, как только бактерии будут устранены.
Кандидозный вагинит, обычно называемый «дрожжевой инфекцией», является проблемой, которую 75 процентов женщин будут испытывать в течение своей жизни. Почти половина всех женщин студенческого возраста имели по крайней мере один эпизод молочницы.
РСР была одной из первых необычных инфекций, наблюдавшихся на ранних стадиях эпидемии СПИДа, и указывала на то, что у пациентов ослаблена иммунная система. Примерно 60 процентов людей, инфицированных пневмоцистами грибов, к тому времени не смогли прожить и четыре года. После легкой инфекции в детстве организм остается латентным до тех пор, пока ослабленный иммунитет не вызовет реактивацию. Патоген живет в почве и воде.PCP имеет 40-дневный инкубационный период у больных СПИДом, и болезнь может сопровождаться потерей веса, недомоганием, диареей, сухим кашлем, одышкой и субфебрильной лихорадкой. У других типов пациентов начало заболевания незначительное, со средним инкубационным периодом 60 дней, что приводит к сухому кашлю, который может прогрессировать до более тяжелой дыхательной недостаточности. Помимо больных СПИДом, наибольшему риску заболевания подвергаются младенцы с тяжелой недостаточностью питания, дети с первичным дефицитом иммунной системы, больные раком и пациенты после трансплантации органов.
Пациенты с высоким риском развития РСР также включают младенцев с тяжелой недостаточностью питания, детей с дефицитом иммунной системы и реципиентов органов или костного мозга. PCP излечима, если пациенты с высоким риском для будут принимать профилактические препараты. Раннее выявление и лечение — ключ к победе над болезнью.
Теория по иммунологии. Оценка иммунного статуса, аллергия, иммунитет при бактериальных, вирусных, грибковых, протозойных, глистных инфекциях; новообразования.
При создании данной страницы использовалась лекция по соответствующей теме, составленная Кафедрой репродуктивного здоровья человека ИДПО с курсом иммунологии
Навигация:
- Оценка уровня естественной резистентности
- Оценка иммунного статуса
- Исследование Т-системы иммунитета
- Исследование В-системы иммунитета
- Диагностические мероприятия при аллергических заболеваниях
- Особенности иммунитета при бактериальных инфекциях
- Особенности противовирусного иммунитета
- Особенности противогрибкового иммунитета
- Особенности иммунитета при протозойных инвазиях
- Особенности противоглистного иммунитета
- Трансплантационный иммунитет
- Иммунитет против новообразований
Иммунодиагностика – это решение двух вопросов:
- Изменена ли иммунологическая реактивность организма?
- Если она изменена, в чем выражено это изменение и в какой степени?
Методы исследования иммунологической реактивности:
- оценка уровня естественной резистентности;
- оценка уровня иммунного статуса.
Оценка уровня естественной резистентности
Исследование клеточных факторов неспецифической резистентности
1. Определение бактерицидной активности кожи путем посевов-отпечатков по методу Клемпарской (N>95%).
2. Определение фагоцитарной активности лейкоцитов.
- Фагоцитарный показатель (N=79%).
- Фагоцитарный индекс (N=1,3-3,0, для частиц латекса=10,2).
- Завершенность фагоцитоза.
- НСТ-тест – способность фагоцитирующих клеток (супероксидные радикалы) восстанавливать бесцветный реактив нитросиний тетразоль в краситель, окрашивающий активную клетку в синий цвет (N=48-80%).
Исследование гуморальных факторов неспецифической резистентности:
- уровень комплемента в сыворотке крови;
- содержание лизоцима в слюне или сыворотке крови;
- титры сывороточных β – лизинов;
- С-реактивный белок в сыворотке крови;
- сывороточный интерферон.
Оценка иммунного статуса
Исследование Т-системы иммунитета
1. Количественное определение Т-лимфоцитов:
- в реакции розеткообразования с бараньими эритроцитами (ЕРОК) (N=50-76%).
- Розеткой считается лимфоцит, прикрепивший не менее 3 эритроцитов.
- по кластерам дифференцировки CD-2 и CD-3 с диагностическими меченными моноклональными антителами в непрямых вариантах реакции иммунофлюоресценции (РИФ) и иммуноферментного анализа (ИФА).
2. Определение CD4+ и CD8+ лимфоцитов и их соотношения:
- в непрямой РИФ с моноклональными антителами. (NCD4+=31-46% всех Т-лимфоцитов, а NCD8+=30-35%. Соотношение CD4+ : CD8+ = 1,0:2,2 – 1,0:1,5)
3. Функциональная активность Т-лимфоцитов:
- реакция бластной трансформации (РБТ) (N=20-100%);
- цитотоксическая функция Т-клеток в реакциях с клетками мишенями;
- реакция торможения миграции лейкоцитов (РТМЛ).
Исследование В-системы иммунитета
1. Количественное изучение В-лимфоцитов:
- в реакции розеткообразования с эритроцитами мышей (ЕАРОК);
- в реакции розеткообразования с бараньими эритроцитами, сенсибилизированными антителами и комплементом (ЕАСРОК) (N=10-20%);
- по кластерам дифференцировки CD-19, 20, 22 в непрямой РИФ и ИФА.
2. Определение функциональной активности В-лимфоцитов:
- РБТ;
- уровень нормальных антител в реакции агглютинации (РА) с эритроцитами барана и с микробными антигенами;
- содержание иммуноглобулинов классов G, М, А методом Манчини (реакция преципитации в геле), непрямым ИФА и радиоиммунным анализом (РИА). N IgM=109 МЕ/мл (0,5 – 1,9 мг/мл) N IgG=233 МЕ/мл (8,0 –16,0 мг/мл) N IgA=147 МЕ/мл (1,4 – 4,2 мг/мл).
Практическое использование методов исследования иммунной системы
- Оценка состояния иммунной системы (оценка иммунного статуса).
- Серотипирование бактериальных и вирусных культур, выделенных из организма человека.
- Серодиагностика инфекционных болезней.
- Выявление иммунопатологических состояний.
- Определение состава и характеристики тканей человека: групп крови, Rh-фактора, HLA антигенов.
- Выявление в организме человека или во внешней среде любых веществ, обладающих антигенными свойствами (гормонов, ферментов, ядов, лекарств, наркотических средств).
Оценка иммунного статуса:
I этап – клиническая долабораторная диагностика иммунодефицитных и других иммунопатологических состояний:
- иммунологический анамнез (частота инфекционных заболеваний, характер их течения, выраженность температурной реакции, наличие очагов хронической инфекции);
- клинический анализ крови (содержание лейкоцитов, в т.ч. лимфоцитов, моноцитов, сегментоядерных);
- результаты бактериологического (вирусологического) и серологического исследований на бактерио- (вирусо-) носительство.
II этап предусматривает применение тестов 2-х уровней:
Тесты первого уровня позволяют выявить грубые нарушения функций иммунной системы:
- процентное содержание и абсолютное количество Т — и В-лимфоцитов;
- уровень иммуноглобулинов сыворотки крови классов М, G, А, Е;
- титр комплемента;
- фагоцитарная активность нейтрофилов.
Тесты второго уровня проводятся при выявлении грубых нарушений функции иммунной системы и включают углубленное иммунологическое обследование для установления регуляторных нарушений и дисфункций иммунитета:
- субпопуляции Т-лимфоцитов (CD4+, CD8+), их соотношение;
- функциональная активность Т- и В-лимфоцитов в РБТ и РТМЛ;
- цитотоксическая активность лейкоцитов;
- кожные тесты.
Диагностические мероприятия при аллергических заболеваниях
- аллергологический анамнез (наличие аллергических реакций на антибиотики, пищевые продукты, пыльцу растений и т. д.);
- данные клинико-лабораторных исследований (лейкоцитоз, эозинофилия);
- при аллергических реакциях I – содержание сывороточного JgE;
- при аллергических реакциях II типа – выявление в сыворотке крови антиэритроцитарных, антилейкоцитарных, антитромбоцитарных антител, оказывающих цитолитическое действие в присутствии комплемента на клетки-«мишени»;
- при аллергических реакциях III типа – иммунные комплексы, циркулирующие в крови или фиксированные на тканях органа- «мишени»;
- для изучения клеточно-опосредованной сенсибилизации при аллергии IV типа проводят РБТ и РТМЛ;
- при реакциях I и IV типов проводят кожно-аллергические пробы.
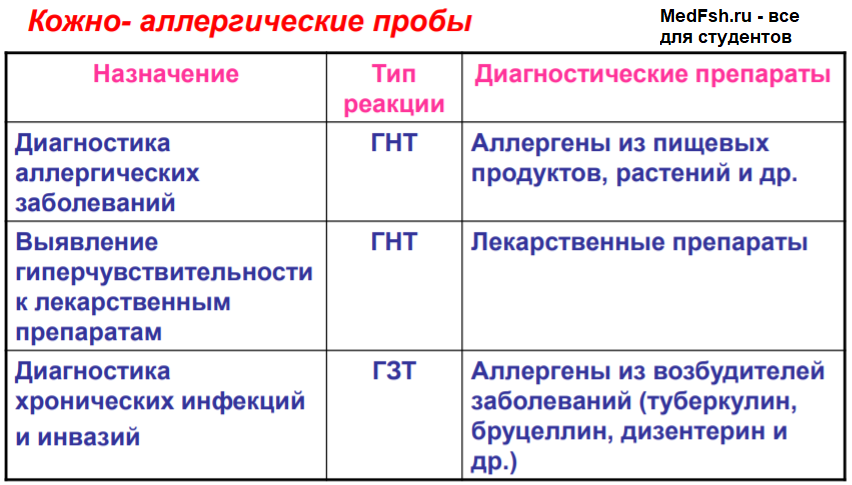
Метод кожных проб основан на том, что Ig Е находится не только в шоковом органе, но и в коже. В месте введения аллергена происходит аллергическая реакция АГ-АТ с высвобождением гистамина (через 20-30 минут – покраснение, волдырь).
Выраженность кожной реакции зависит от степени сенсибилизации организма.
В основе кожных проб на внутрикожное введение аллергена в специфически сенсибилизированный (инфицированный или вакцинированный) организм лежат аллергические реакции клеточного типа (на месте введения – через 24-48 часов образуется мононуклеарный инфильтрат, величина которого зависит от степени сенсибилизации).
Практическое применение:
- диагностика туберкулеза (проба Манту с туберкулином);
- диагностика туляремии (проба с тулярином);
- диагностика дизентерии (проба Цуверкалова с дизентерином) и т. д.
Лабораторная диагностика аутоиммунных процессов осуществляется с помощью выявления аутоантител и циркулирующих иммунных комплексов методом осаждения полиэтиленгликолем.
Особенности иммунитета при бактериальных инфекциях
- Иммунная реакция макроорганизма в ответ на бактериальную инфекцию в значительной степени определяется факторами патогенности микроба и в первую очередь его способностью к токсинообразованию. Различают иммунитет антибактериальный — против структурных компонентов бактериальной клетки и антитоксический — против белковых токсинов.
- Основными факторами антибактериальной защиты являются антитела и фагоциты. Антитела эффективно инактивируют биологически активные молекулы бактериальной клетки (токсины, ферменты агрессии и др.), маркируют их, запускают антителозависимый бактериолиз и иммунный фагоцитоз. Фагоциты непосредственно осуществляют фагоцитоз, в том числе иммунный, антителозависимый бактериолиз и внеклеточный киллинг патогена при помощи ион-радикалов и ферментов. Важная роль в борьбе с грамположительными микробами принадлежит лизоциму, а с грамотрицательными — комплементу (альтернативный путь активации), кроме того, существенное значение имеют белки острой фазы (С-реактивный и маннозосвязывающий протеин).
- Ряд бактерий, относящихся к факультативным внутриклеточным паразитам, отличается повышенной устойчивостью к действию комплемента, лизоцима и фагоцитов (незавершенный фагоцитоз). К их числу относятся микобактерии, йерсинии, бруцеллы, сальмонеллы и некоторые другие. В такой ситуации макроорганизм вынужден переключать нагрузку на клеточное звено иммунитета, что ведет к аллергизации организма по механизму ГЗТ. Особое значение приобретают активированные макрофаги и естественные киллеры, осуществляющие АЗКЦТ, а такжеТ-лимфоциты.
- Напряженность специфического антибактериального иммунитета оценивают в серологических тестах по титру или динамике титра специфических антител, а также по состоянию клеточной иммунореактивности (например, по результатам кожно-аллергической пробы).
Особенности противовирусного иммунитета
- Особенности иммунной защиты макроорганизма при вирусных инфекциях обусловлены двумя формами существования вируса: внеклеточной и внутриклеточной. Основными факторами, обеспечивающими противовирусный иммунитет, являются специфические антитела, Т-киллеры, естественные киллеры, интерферон и сывороточные ингибиторы вирусных частиц.
- Специфические противовирусные антитела способны взаимодействовать только с внеклеточным вирусом, так как у них нет доступа внутрь живой клетки. Антитела нейтрализуют вирусные адгезины и нейраминидазы, препятствуя адсорбции вирусов на клетках-мишенях и их инфицированию. Они также связывают вирусные белки и нуклеиновые кислоты, образовавшиеся после разрушения зараженных вирусами клеток. Сформировавшиеся иммунные комплексы элиминируются путем иммунного фагоцитоза.
- Клетки, инфицированные вирусом и приступившие к его репликации, экспрессируют вирусные белки на цитоплазматической мембране в составе молекул антигенов гистосовместимости — MHC I класса. Измененная структура MHC I класса этих антигенов гистосовместимости является маркером для Т-киллеров, которые распознают зараженные вирусом клетки и уничтожают их.
- Мощным противовирусным свойством обладает интерферон. Он не действует непосредственно на внутриклеточный вирус, а связывается с рецептором на мембране клетки и подавляет в ней все биосинтетические процессы.
- Напряженность противовирусного иммунитета оценивают преимущественно в серологических тестах по нарастанию титра специфических антител в парных сыворотках в процессе болезни. Определяют также концентрацию интерферона в сыворотке крови.
Особенности противогрибкового иммунитета
- Антигены грибов имеют относительно низкую иммуногенность: они практически не индуцируют антителообразование (титры специфических антител остаются низкими), но стимулируют клеточное звено иммунитета. Основными действующими факторами противогрибкового иммунитета являются активированные макрофаги, которые осуществляют АЗКЦТ грибов.
- При микозах наблюдается аллергизация макроорганизма. Кожные и глубокие микозы сопровождаются, как правило, ГЗТ. Грибковые поражения слизистых оболочек дыхательных и мочеполовых путей вызывают аллергизацию по механизму ГНТ (реакция I типа). Напряженность противогрибкового иммунитета оценивается по результатам кожно-аллергических проб с грибковыми аллергенами.
Особенности иммунитета при протозойных инвазиях
- Паразитарная инвазия сопровождается формированием в макроорганизме гуморального и клеточного иммунитета. В крови определяются специфические антитела классов M и G, которые чаще всего не обладают протективным свойством. Однако они активируют АЗКЦТ с участием макрофагов, а в случае внутриклеточного паразитирования — естественных киллеров и T лимфоцитов. Паразитарные инвазии сопровождаются аллергизацией макроорганизма по механизму ГЗТ.
- Характер противопаразитарного иммунитета определяется биологическими особенностями паразита. Многие паразиты обладают высокой антигенной изменчивостью, что позволяет им избегать действия факторов иммунитета. Например, каждой стадии развития малярийного плазмодия соответствуют свои специфические антигены.
- Напряженность противопаразитарного иммунитета оценивается в серологических тестах по титру специфических антител и в кожноаллергических пробах с протозойным антигеном.
Особенности противоглистного иммунитета
- Ведущую роль в осуществлении иммунной защиты макроорганизма от глистной инвазии играют эозинофилы, которые осуществляют АЗКЦТ. Эти клетки распознают паразитов, отмеченных специфическими IgE или IgA. Активированный эозинофил выделяет путем дегрануляции ряд токсичных субстанций (ферменты, белковые токсины), губительно действующих на гельминты.
- Антигены гельминта, связываясь также с рецепторными комплексами тучных клеток слизистой оболочки, вызывают их дегрануляцию. Экскретированные биологически активные соединения вызывают интенсивную перистальтику, удаляющую паразита или его останки из просвета кишки.
- Эозинофилы и тучные клетки синтезируют цитокины и липидные медиаторы, потенцирующие воспалительную реакцию в месте внедрения гельминта. Глистная инвазия сопровождается аллергизацией в основном по механизму ГЗТ.
Трансплантационный иммунитет
- Макроорганизм формирует иммунную реакцию, направленную против пересаженной в него чужеродной ткани (трансплантата). Это является основной проблемой, препятствующей успешной пересадке органов и тканей. Иммунная реакция на чужеродные клетки и ткани обусловлена тем, что в их составе содержатся генетически чужеродные для организма антигены. Эти антигены получили название трансплантационных или антигенов гистосовместимости. Наиболее полно они представлены на цитоплазматической мембране клеток.
- Реакция отторжения не возникает в случае полной совместимости донора и реципиента по антигенам гистосовместимости — такое возможно лишь для однояйцовых близнецов. Выраженность реакции отторжения во многом зависит от степени чужеродности, объема трансплантируемого материала и состояния иммунореактивности реципиента.
- На чужеродные трансплантационные антигены организм реагирует факторами клеточного и гуморального иммунитета. Основным являются Т-киллеры и специфические антитела. Т-киллеры осуществляют АНКЦТ тканей трансплантата (реакция реципиент против трансплантата) или реципиента (реакция трансплантат против реципиента). Специфические антитела, которые образуются к антигенам трансплантата, запускают комплемент- или клеточно-опосредованный цитолиз трансплантата.
- Возможен адаптивный перенос трансплантационного иммунитета с помощью активированных лимфоцитов или со специфической антисывороткой от сенсибилизированной особи интактному макроорганизму.
- Механизм иммунного отторжения пересаженных клеток и тканей имеет две фазы. В первой фазе вокруг трансплантата и сосудов наблюдается скопление иммунокомпетентных клеток (лимфоидная инфильтрация), в том числе Т-киллеров. Во второй фазе происходит деструкция клеток трансплантата Т-киллерами, активируются макрофагальное звено, естественные киллеры, специфический антителогенез. Затем возникают иммунное воспаление, тромбоз кровеносных сосудов, нарушается питание трансплантата и происходит его гибель. Разрушенные ткани утилизируются фагоцитами. Ткани трансплантата реагируют на ткани реципиента подобным же образом. Однако иммунная реакция трансплантата слабее, так как ограничена его ресурсами.
- В процессе реакции отторжения формируется клон клеток иммунологической памяти. Повторная попытка пересадки тех же органов и тканей вызывает вторичный иммунный ответ, который протекает очень бурно и быстро заканчивается отторжением трансплантата.
Иммунитет против новообразований
- Противоопухолевый иммунитет имеет свои особенности, связанные с низкой иммуногенностью раковых клеток. Эти клетки практически не отличаются от нормальных, интактных морфологических элементов собственного организма. Специфический антигенный репертуар опу?
