Клеточные механизмы противовирусного иммунитета в ветеринарии
Иммунитет (от лат. immunitas — освобождение или избавление от чего-либо) — состояние невосприимчивости организма к воздействию патогенных микробов, их токсинов и других чужеродных веществ биологической природы. Организмы человека и животных весьма точно дифференцируют «свое» и «чужое», благодаря чему обеспечивается защита не только от внедрения патогенных микробов, но и чужеродных белков, липополисахаридов, полисахаридов и других чужеродных веществ. Следовательно, главное значение иммунитета состоит в распознавании «своего» и «чужого», что жизненно важно. Поступление во внутреннюю среду организма веществ с признаками чужеродной информации (макромолекул белков, полисахаридов и др.) грозит нарушением структурного и химического состава этого организма. Количественное и качественное «постоянство» внутренней среды, называемое гомеостазом, обеспечивается процессами саморегулирования во всех живых системах. Иммунитет — одно из проявлений гомеостаза. В этой связи иммунитет является свойством всего живого: человека, животных, растений и даже бактерий.
Система органов и клеток, осуществляющая реагирование против чужеродных субстанций, получила название иммунной системы организма. Она распределена по всему организму, ее клетки постоянно рециркулируют по всему телу через кровоток, она обладает способностью вырабатывать сугубо специфические молекулы антител, различные по своей специфике в отношении каждого антигена.
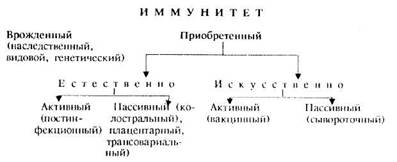
По происхождению различают два вида иммунитета: врожденный и приобретенный.

Врожденный иммунитет
Врожденный (видовой, наследственный, генетический) иммунитет — это невосприимчивость к инфекционным агентам, детерминированная в геноме и проявляемая количеством и порядком расположения ганглиозидов определенного типа на поверхности мембран клеток. Этот вид иммунитета свойственен животным определенного вида к определенному возбудителю инфекции и передается из поколения в поколение. Например, лошади не болеют ящуром, крупный рогатый скот — сапом, собаки — чумой свиней, животные — сифилисом и т. д. В основе механизмов врожденного иммунитета к определенным возбудителям лежат отсутствие в клетках организма рецепторов и субстратов, необходимых для адгезии и размножения возбудителя, наличие веществ, блокирующих размножение патогенных микробов. Последние не могут размножаться в организме, и заболевание не возникает. Например, Brucclla abortus будет размножаться в плаценте только тех видов животных, которые содержат углевод эритритол.
Врожденный иммунитет весьма прочный, но не абсолютный. Так, в естественных условиях куры не болеют сибирской язвой, однако Пастер заразил курицу сибиреязвенной бациллой после искусственного понижения температуры тела погружением ее конечностей в холодную воду. Мечникову удалось вызвать экспериментальный столбняк у лягушки (весьма устойчивой к столбнячному токсину) путем согревания ее в термостате. Врожденной резистентностью в основном обладают взрослые животные. У новорожденных во многих случаях видовая устойчивость отсутствуют. Например, кролики-сосуны и мышата чувствительны к заражению вирусом ящура. Весьма чувствительны к заражению вирусами и бактериями развивающиеся куриные эмбрионы, что в практике используют для получения вакцин.
Следует учитывать, что животные, не заболевая определенной инфекционной болезнью, могут быть носителем возбудителя и представлять опасность для других видов. Например, человек может быть носителем вируса чумы собак.
Важно отметить, что естественная невосприимчивость является не только видовым признаком, среди восприимчивых к определенным микробам видов существуют породы, популяции и линии, животных, отличающиеся высокой устойчивостью к данному возбудителю. Так, при высокой чувствительности овец к сибирской язве алжирские овцы отличаются высокой к ней устойчивостью. Свиньи йоркширской породы по сравнению с другими породами устойчивее к роже свиней. Куры породы белый леггорн более устойчивы к пуллорозу, чем птицы пород красный род-айленд и плимутрок.
Приобретенный иммунитет
Характерная особенность приобретенного иммунитета — его специфичность, т. е. устойчивость организма только к определенному возбудителю болезни. Приобретенный иммунитет подразделяют на естественный и искусственный. Естественно приобретенный иммунитет, в свою очередь, делят на активный и пассивный. Активный (постинфекционный) образуется после естественного переболевания животного. Естественно приобретенный иммунитет не обязательно должен быть связан с клинически выраженным переболеванием. Во многих случаях в организм животного систематически попадают дозы возбудителя меньше той, которая может вызвать заболевание. В этом случае происходит скрытая иммунизация, которая у животных, достигших определенного возраста, создает активный иммунитет к определенному возбудителю. Такое явление называют иммунизирующей субинфекцией.
Естественно приобретенный пассивный иммунитет — иммунитет новорожденных, приобретенный ими за счет поступления плоду от матери антител через плаценту (трансплацентарный) либо уже после рождения через кишечник с молозивом (колостральньш, или молозивный). У птиц (например, кур) материнские антитела передаются с лецитиновой фракцией желтка (трансовариальный). Важно отметить, что насыщение кровотока иммунными фракциями новорожденных жвачных, лошадей, свиней происходит в основном колостральным путем. В этой связи различают естественно и искусственно вызванный колостральный иммунитет. В первом случае иммунитет обусловлен антителами, естественно выработанными в организме матери под воздействием различных антигенов окружающей среды. Во втором случае путем направленной иммунизации организма матери определенными антигенами вырабатываются специфические антитела против определенного возбудителя болезни.
Молозиво неиммунизированных коров обладает бактериостатическими и антитоксическими свойствами в отношении многих патогенных микроорганизмов — кишечной палочки, сальмонелл, стафилококков и др. Так, в молозиве в среднем при первой дойке содержится в 100 мл Ig — 900 мг, IgG — 200, IgM — 400, IgA — 300 мг, а в том же количестве молока уже соответственно 50, 2, 5 и 8 мг. Воспринятые с молозивом иммуноглобулины (антитела) в кишечнике, например новорожденных телят, абсорбируются и неизмененными проходят через стенку кишечника в лимфатическую систему, а затем в кровеносное русло. Следует знать, что у домашних животных кишечник проницаем для молозивных антител лишь первые 24—36 ч, поэтому молозиво новорожденный должен получить как можно раньше с момента рождения.
Естественно приобретенный активный иммунитет может сохраняться 1—2 года, но в некоторых случаях — пожизненно (например, у собак, переболевших чумой, у овец, переболевших оспой). Естественно приобретенный пассивный иммунитет обеспечивает состояние невосприимчивости от нескольких недель до нескольких месяцев.
Искусственно приобретенный иммунитет также подразделяют на активный и пассивный. Активный (поствакцинальный) возникает в результате иммунизации животных вакцинами. Вакцинный иммунитет развивается через 7—14 дней и сохраняется от нескольких месяцев до одного года и более. Пассивный иммунитет создается при введении в организм иммунной сыворотки, содержащей специфические антитела против определенного возбудителя болезни. Пассивный иммунитет можно создать и при введении сывороток крови животных-реконвалесцентов (переболевших данной болезнью), например при ящуре. Пассивный иммунитет, как правило, не превышает 15 дней.
Иммунитет также принято классифицировать по направленности действия защитных механизмов организма на микроорганизмы или их продукты. Различают антибактериальный иммунитет, когда защитные механизмы направлены против патогенного микроба, в результате предотвращается размножение и распространение в нем микроба.
Противовирусный иммунитет обусловливается выработкой организмом противовирусных антител и механизмами клеточной защиты.
Антитоксический иммунитет, при образовании которого бактерии не разрушаются, но вырабатываются антитела, эффективно нейтрализующие токсины в организме больного животного.
Иммунитет при протозойных и гсльминтозных заболеваниях направлен на обезвреживание и уничтожение возбудителей болезней.
Различают также местный (локальный) иммунитет. Понятие «местный иммунитет» впервые было введено А. М. Бередка в 1925 г. Логическим выводом теории местного иммунитета явилось изыскание методов локальной иммунизации тканей и органов, являющихся воротами инфекции — первого защитного барьера против инфекционного агента. В этой связи стали широко в практике применять аэрогенный и пероральный способы иммунизации.
Если после перенесенной болезни организм освобождается от возбудителя, сохраняя при этом состояние невосприимчивости, то такой иммунитет называют стерильным. Однако при многих инфекциях иммунитет сохраняется только до тех пор, пока в организме находится возбудитель болезни. В этом случае говорят об инфекционном или нестерильном иммунитете (премуниция).
В зависимости от механизмов зашиты организма различают также гуморальный и клеточный иммунитет. Гуморальный иммунитет обусловливается выработкой в зараженном организме специфических антител, клеточный иммунитет — за счет образования специфически реагирующих с возбудителем (антигеном) Т-лимфоцитов.
Основой противовирусного иммунитета является клеточный иммунитет. Клетки-мишени, инфицированные вирусом, уничтожаются цитотоксическими лимфоцитами, а также НК и фагоцитами, взаимодействующими с Fc-фрагментами антител, прикрепленных к вирус- специфическим белкам инфицированной клетки. Противовирусные антитела способны нейтрализовать только внеклеточно расположенные вирусы, как и факторы неспецифического иммунитета — сывороточные противовирусные ингибиторы. Такие вирусы, окруженные и блокированные белками организма, поглощаются фагоцитами или выводятся с мочой, потом и др. (так называемый «выделительный иммунитет»).
Интерфероны усиливают противовирусную резистентность, индуцируя в клетках синтез ферментов, подавляющих образование нуклеиновых кислот и белков вирусов. Кроме того, интерфероны оказывают иммуномодулирующее действие, усиливают в клетках экспрессию антигенов главного комплекса гистосовместимости (МНС).
Противовирусная защита слизистых оболочек обусловлена секреторными IgA, которые, взаимодействуя с вирусами, препятствуют их адгезии на эпителиоцитах.
На основании вышеизложенного можно сделать следующие выводы.
Механизм защиты против той или иной бактериальной инфекции зависит от строения клеточной стенки возбудителя и факторов патогенности.
Нейтрализующие антитела могут полностью обеспечивать защиту, если патогенность возбудителя связана только стоксином или адгезином.
Неспецифические, филогенетически древние механизмы иммунитета (фагоцитоз, альтернативная активация комплемента и выделение цитокинов) действуют вследствие распознавания консервативных бактериальных структур.
Комплемент может уничтожать некоторые грамотрицательные бактерии, имеющие наружный липидный бислой или наружную мембрану, в составе клеточной стенки.
Фагоциты способны уничтожать клетки большинства бактерий, осуществляя последовательно хемотаксис, связывание, поглощение и лизис.
Патогенные микроорганизмы обладают разнообразными свойствами, используемыми для обхода защитного действия комплемента и фагоцитов или для направления Т-зависимой активации фагоцитоза по ложному пути.
Хроническую иммунопатологию с повреждением тканей (как, например, при туберкулезе) вызывает дисбаланс в выделении цитокинов, приводящий к неадекватным эффектам.
Иммунитет к грибам опосредован клетками и сходен с антибактериальным.
Основой противовирусного иммунитета являются клеточный иммунитет, антитела и интерферон.
- 1. Назовите структурные, клеточные и химические механизмы защиты организма от бактерий.
- 2. Укажите роль свойств бактерий в преодолении иммунной защиты организма (на примере строения клеточных стенок).
- 3. Опишите иммунологические механизмы разрушения различных микроорганизмов: хемотаксис, выделение цитокинов, антитела, фагоцитоз, комплемент, персестирование.
- 4. В чем заключается основа устойчивости к микотической инфекции?
- 5. Каковы основы противовирусного иммунитета?
- 1. Литвин В.Ю., Пушкарева В.И. Факторы патогенности бактерий: функции в окружающей среде // Микробиология. 1994. Приложение.
- 2. Румянцеве.Н. Микробы, эволюция, иммунитет. Л., 1984.
- 3. (22> Лекция «Основы учения об инфекции».
- 4. URL: https://www.myshared.ru/slide/396028/
Факторы неспецифического и специфического противовирусного иммунитета. Учение о противовирусном иммунитете является частным разделом современной иммунологии, которая занимается изучением механизмов защиты, обеспечивающих постоянство внутренней среды организма путем распознавания и взаимодействия с чуждым ему субстратом.
Особенность иммунологии вирусных инфекций обусловлена уникальными особенностями биологии их возбудителей, принадлежащих к агентам молекулярной неклеточной организации. Все вирусы представляют собой строгие внутриклеточные паразиты, отличающиеся механизмами репродукции и взаимодействия с чувствительными клетками от клеточных микроорганизмов. Своеобразие биологии вирусов и патогенеза болезней, вызываемых ими у животных и человека, непосредственно отражается на иммунологических реакциях, соответствующих каждой отдельной группе вирусных инфекций.
При вирусных инфекциях, как и при бактериальных, после пе- реболевания в организме формируется иммунитет различной напряженности и длительности. Следует отметить, что при попадании вируса в организме не всегда происходят иммунологические реакции. Этот вид невосприимчивости свойствен животным определенного вида к определенному возбудителю инфекции и передается из поколения в поколение, например лошади не болеют ящуром, крупный рогатый скот — сапом, собаки — чумой свиней и др. В основе механизмов такой невосприимчивости (врожденного иммунитета — видового, наследственного, генетического) к определенным возбудителям лежит отсутствие в клетках рецепторов и субстратов, необходимых для взаимодействия вирусов, наличие веществ, блокирующих репродукции вирусов. Последние не могут репродуцироваться в организме, и заболевание не происходит. Необходимо отметить, что у новорожденных во многих случаях видовая устойчивость отсутствует, например крольчата-сосуны и мышата чувствительны к заражению вирусом ящура.
Защитные приспособления, или факторы противовирусного иммунитета, подразделяют на неспецифические и специфические, которые разнообразны по своей природе и механизму действия (рис. 21).
Неспецифический противовирусный иммунитет. Создание иммунитета обеспечивают факторы неспецифической защиты: 1) общие физиологические; 2) гуморальные; 3) клеточные.
Перечисленные факторы обеспечивают защиту микроорганизма против вирусов на молекулярном, клеточном и организменном уровнях, которые неразрывно связаны между собой.
Общие физиологические факторы. Для проникновения в восприимчивые клетки и ткани вирусу необходимо преодолеть защитные барьеры.
Кожно-слизистые барьеры выдерживают первую атаку вирусов. Неповрежденные кожа и слизистая оболочка служат не только механической преградой, но и являются стерилизующим фактором.
Если вирусы преодолели кожные и слизистые барьеры, то начинается их массивное проникновение в ткани. В инфицированный участок быстро прибывает огромная масса фагоцитов, и таким образом создается защитный вал вокруг воспалительного очага, при этом ограничивается распространение микробов в соседние ткани и кровь.
В создании иммунитета участвуют и такие общефизиологические факторы, как температура тела и выделение вируса из организма различными секрециями. При повышении температуры тела усиливаются процессы иммуногенеза, ускоряется обмен веществ, усиливается продукция интерферона, что в совокупности способствует выздоровлению. Повышение температуры тела вызывает непосредственную инактивацию внеклеточного вируса и способствует подавлению репродукции внутри клетки, а также ускоряет обменные процессы в клетках и в организме, что сопровождается снижением рН внеклеточной и внутриклеточной среды (состояние ацидоза). Кислая среда подавляет вирусы и, наоборот, благоприятно влияет на ингибиторы, содержащиеся в тканях и жидкостях организма.
В удалении вирусов из организма принимают участие и выделительные системы. Вирусы уже через короткое время (10…30 мин) появляются в моче. В отличие от бактерий они способны проходить через почечный фильтр. Способность выделяться с мочой доказана для многих вирусов животных и человека — гриппа, кори, чумы, ящура и др.
Вирусы выделяются из организма не только почками, но и другими выделительными системами со слюной (грипп, бешенство), секретами при респираторных заболеваниях, кишечником, пораженными клетками, эритроцитами и др. Выделение вирусов в окружающую среду с мочой и другими экскретами способствует более быстрому восстановлению относительного постоянства внутренней среды организма, нарушаемого вирусной инфекцией.
Гуморальные факторы. Неспецифическую защиту организма обеспечивают пропердин, ингибиторы в сыворотке крови, гормоны.
Пропердин (гамма-глобулин) содержится в нормальной сыворотке крови и принимает участие в нейтрализации вирусов. Активность проявляется за счет не самого пропердина, а системы пропердина (комплемента и двухвалентных ионов магния).
Ингибиторы — это неспецифические противовирусные вещества белковой природы, которые присутствуют в нормальной сыворотке крови, секретах эпителия слизистых оболочек дыхательного и пищеварительного трактов, в экстрактах органов и тканей. Они обладают способностью подавлять активность вирусов внечувствительной клетки: при нахождении вируса в крови и жидкостях. Ингибиторы подразделяют на термолабильные (теряют свою активность при прогревании сыворотки крови при 60…62 °С в течение 1 ч) и термостабильные (выдерживают нагревание до 100 °С). Ингибиторы обладают универсальной вируснейтрализую- щей и антигенагглютинирующей активностью в отношении многих вирусов.
Помимо сывороточных ингибиторов различают ингибиторы тканей, секретов и экстрактов. Такие ингибиторы оказались активными в отношении многих вирусов. Например, секреторные ингибиторы респираторного тракта обладают антигемагглютини- рующей и вируснейтрализующей активностью.
Механизм действия ингибиторов заключается в соединении их с вирусами, вызывая нейтрализацию вирусных рецепторов, что выражается в понижении их физико-химических адсорбционных свойств. В результате вирусы теряют способность адсорбироваться на поверхности чувствительных клеток и проникать в них; вирусные частицы отторгаются с поверхности чувствительных клеток.
Защитная функция ингибиторов так же, как и антител, зависит от природы вируса и его количества, от активности самих ингибиторов. На активности ингибиторов сказываются индивидуальные и возрастные особенности и др. При низком содержании ингибиторов (у молоды^ организмов) вирус может освобождаться и восстанавливать свою активность. При большом содержании ингибиторов (с возрастом количество их увеличивается) и высоком их титре вирус нейтрализуется и становится объектом воздействия других иммунологических факторов.
Гормоны могут опосредованно влиять на резистентность к вирусным агентам. Например, большие дозы кортизона снижают, а малые дозы, наоборот, повышают защитные функции организма.
На проникшие же в клетки вирусы действуют так называемые киллеры, представляющие собой клетки крови (малые лимфоциты). Естественные киллеры окружают клетки собственного организма, пораженные любым вирусом, и с помощью ферментов разрушают клетку вместе с вирусом.
Клеточные факторы. В неспецифическом противовирусном иммунитете участвуют фагоцитирующие клетки (микро- и макрофаги).
Макрофаги — это полиморфная группа клеток, активно фагоцитирующих чужеродный материал, попавший в кровоток: моноциты крови, клетки костного мозга, купферовские клетки печени, гистиоциты, макрофаги селезенки, лимфатических узлов и серозных полостей. Макрофаги принимают активное участие в процессе антителообразования, вступая в кооперацию с Т- и В-клетками (лимфоцитами). Т-лимфоциты — это тимусзависимые иммуноциты. В-лимфоциты — это клетки, происходящие из клеток предшественников костного мозга, которые мигрируют в определенные участки лимфатических узлов и селезенки. Большинство В-клеток локализовано в лимфоидных тканях, другая их часть может циркулировать с лимфой и кровью.
Фагоцитозу возбудителей макрофагами способствуют специфические антитела, оказывающие опсонирующие и агглютинирующие действия на вирусы. Кроме того, фагоциты являются продуцентами антител и интерферона.
Роль лейкоцитов в противовирусном иммунитете малоэффективна (незначительна). Вирусы адсорбируются на лейкоцитах и поглощаются ими, но последующего разрушения их в клетках не происходит: весь процесс останавливается на стадии незавершенного фагоцитоза. Попытки в экспериментальных условиях перевести незавершенный фагоцитоз в завершенный не дали положительных результатов. Неспособность макрофагами переваривать вирусы — одна из основных особенностей механизма противовирусного и противобактериального иммунитета. Однако в противовирусном иммунитете фагоцитозу не отводится существенная роль.
Если вирус преодолевает действие гуморальных факторов иммунитета (антител и ингибиторов) и проникает в чувствительную клетку, то с этого момента начинается внутриклеточное развитие возбудителя и инфекции, вызванной им. Однако проникновение вируса в клетку не всегда сопровождается его внутриклеточным развитием. Клетка остается морфологически не измененной, деструктивные процессы в ней не происходят и она приобретает устойчивость к повторным заражениям другими вирусами.
Подавление процесса репродукции одного вируса другим в живых клетках называется вирусной интерференцией. Материальной основой интерференции служит особое вещество — интерферон, образующийся клеткой в ответ на проникновение в нее вируса. Он обладает антивирусной, антипролиферативной и имунномо- дулирующей активностью. По химической природе интерферон (интерфероны) представляет собой гликопротеид (белок) с молекулярной массой 20…30 кДа. Интерферон инактивируется при замораживании и оттаивании, при нагревании до 60 °С в течение 1 ч и при 100 °С в течение 5 мин, при облучении ультрафиолетовым излучением, разрушается трипсином и пепсином. На него не действуют рибонуклеаза и дезоксирибонуклеаза, специфические иммунные сыворотки. Он не обладает токсичностью и антигеннос- тью; его активность проявляется как в кислой, так и в щелочной среде (рН 2,0… 10,0).
В организме интерферон обнаруживают через 1…2 ч после введения вируса; максимальный уровень — через 4…8 ч. Индукторами интерферона являются вирусы живые и инактивированные, синтетические полинуклеотиды и бактерии, их эндотоксины.
Интерферон содержится в крови, моче, спинномозговой жидкости, смывах носоглотки, в различных органах (почки, легкие и др.) и тканях организма. Его продуцируют практически все клетки организма, но наиболее активно клетки РЭС (особенно селезенки) и лейкоциты (макрофаги и лимфоциты). Образование интерферона в клетке обусловлено двумя моментами: устойчивостью клетки к вирусу и степенью вирулентности вируса. Если клетка устойчива к вирусу и вирус маловирулентный, то в клетке начинается синтез интерферона. Интерферон подавляет синтез вирусных нуклеаз и активирует синтез другого клеточного белка, обладающего антивирусной активностью. Причем местами такого действия интерферона могут быть вирусная информационная РНК или клеточные рибосомы. Но если клетка чувствительна к вирусу и последний достаточно вирулентен, то клетка синтезирует вирусные компоненты; начинается репродукция вирусных частиц.
Интерферон обладает выраженной видовой специфичностью, т. е. он, образованный клетками одного вида животного, более эффективно защищает животных этого же вида, независимо от того, каким вирусом он был индуцирован.
В отличие от антител интерферон обладает широким спектром антивирусного действия; предохраняет клетки от заражения не только гомологичным вирусом, но и гетерологичными вирусами.
Интерферон адсорбируется другими клетками, и по мере наступления адсорбции развивается устойчивость клеток к заражению вирусом. Он не инактивирует внеклеточный вирус ин витро, что подтверждается сохранением инфекционности последнегопосле смешивания его с интерфероном, а также препятствует адсорбции вируса клеткой и лишь с наступлением интерференции предотвращает накопление вируса в клетке и развитие цитопати- ческого эффекта. При латентных инфекциях наступает равновесие между продукцией клетками вируса и интерферона. Внешне такие клетки не отличаются от здоровых.
Таким образом, антивирусное действие интерферона сводится в конечном счете к превращению инфицированной клетки в систему, в которой репродукция вируса либо невозможна, либо подавлена.
Специфический противовирусный иммунитет. Специфическая защита животных от вирусов осуществляется иммунной системой, которая обладает уникальной способностью распознавать множество разнообразных агентов (микроорганизмы, в том числе и вирусы, токсины и др.) — антигенов и вырабатывать в ответ на это распознавание специфические антитела и сенсибилизированные лимфоциты.
Иммунные механизмы обеспечивают: 1) гуморальные факторы; 2) клеточные факторы. Как известно, вирусы для макроорганизма представляют собой чрезвычайные раздражители, т. е. антигены. Антигенность их связана с белками, входящими в состав оболочек. У вирусов различают два типа антигенов: S — внутренний и Vi — внешний. Позже начинают развиваться специфические факторы, представляющие заключительный и наиболее мощный эшелон защиты организма, а именно гуморальный и клеточный факторы.
Доказано, что гуморальные факторы при вирусных инфекциях составляют основу противовирусного иммунитета. При вирусных инфекциях образуются вируснейтрализующие, компле- ментсвязывающие и преципитирующие антитела.
Специфические противовирусные антитела вырабатываются на рибосомах плазматических клеток — в лимфоцитах при тесном взаимодействии их с Т-лимфоцитами и макрофагами. Противовирусные антитела образуются в тех же клетках, что и противобакте- риальные, и механизм этого процесса один и тот же. Отличие составляет то, что к некоторым вирусам антитела образуются очень быстро — на 2…3-й сутки после заражения организма, например при гриппе. Противовирусные антитела связаны с глобулиновой фракцией сывороточных белков (Ig): А, М, G, Е, D. Наибольшее значение имеют IgG, IgA и IgM, в то время как защитная функция IgD и IgE сравнительно невелика, a IgE связывают с возникновением аллергии.
Роль антител в противовирусном иммунитете высока. Существует прямая зависимость между восприимчивостью организма и концентрацией антител в крови. Доказано, что формирование иммунитета при вирусных инфекциях зависит от сроков появления антител; степень напряженности иммунитета возрастает по мере повышения уровня антител. Действие специфических противови-русных антител направлено непосредственно на вирусную частицу или ее отдельные компоненты (Vi- и S-антигены), а не на клетки.
Формы взаимодействия антител. В основе первичного взаимодействия антител с гомологичным вирусом лежит процесс специфической адсорбции: молекула антитела присоединяется к поверхности вирусной частицы, изменяет ее физико-химические свойства. В результате вирус становится неспособным соединяться с рецепторами чувствительной клетки и проникать в нее.
Принято считать, что одна вирусная частица может нейтрализоваться одной молекулой антитела (хотя вирус может обладать несколькими адсорбционными связями). Если количество антител, вошедших в комплекс вирус—антитело, невелико, то происходит нейтрализация антителами лишь одной адсорбционной поверхности вируса, а другой, свободной стороной вирус может связываться с восприимчивой клеткой и инфицировать ее. Следовательно, антитела прежде всего разрывают контакт между вирусом и восприимчивой клеткой, препятствуя начальной фазе вирусных инфекций.
Нейтрализация вируса антителами представляет подвижный процесс, который зависит от массы, количества этих двух реагирующих систем, а также от ионной концентрации солей, температуры и других факторов, влияющих на взаимодействие вируса и антитела. При избытке антител инактивация вируса может быть полной. Скорость иммунологической реакции зависит от концентрации антител и времени их воздействия на вирус. В течение начального периода комплекс вирус—антитело непрочный и процесс может быть обратимым. С течением времени связь становится прочной и выделить из комплекса вирус невозможно. Однако различные вирусы дают неодинаково стойкие комплексы с антителами, что, по-видимому, зависит от сложности структуры и вирулентности вирусных частиц. Необходимо отметить, что действие специфических противовирусных антител направлено на инактивацию (нейтрализацию) вирусов, находящихся только вне клетки в экстрацеллюлярной среде. И это действие осуществляется на молекулярном уровне на трех линиях защиты: в местах входных ворот вирусов, на пути продвижения их к восприимчивым клеткам и на самой территории клеток с вирусами, находящимися в клетках, хотя до сих пор обоснованных доказательств этого не имеется.
Противовирусные антитела способны вступать в реакцию с вирусом, уже адсорбированным на поверхности клеток. При этом они вызывают нейтрализацию гемагглютинирующих свойств вируса, в результате чего происходит отторжение вирусных частиц с поверхности клетки.
Антитела могут изменить развитие инфекции путем воздействия на чувствительные к вирусам клетки. Это доказано в результате применения иммунных сывороток при различных вирусныхинфекциях (клещевом энцефалите, гриппе, кори, полиомиелите обезьян и др.)- Введение иммунных сывороток в ранние сроки заболевания оказывает положительный лечебный эффект. В этом случае они блокируют уже пораженные вирусом клетки, которые остаются в первичном очаге. В результате этого предотвращается распространение патологического процесса. Структуры и функции пораженных вирусом клеток антитела не восстанавливают.
Огромную роль в противовирусном иммунитете играют клеточные факторы, в основном лимфоциты: Т-лимфоциты формируются из незрелых стволовых клеток в тимусе, В-лимфоциты — в фабрициевой сумке. Т-лимфоциты первыми распознают чужеродный антиген в организме, вырабатывают особые вещества (медиаторы), которые активизируют моноциты и В-лимфоциты, убивают клетки с адсорбированными на них вирусами (или другими антигенами), вырабатывают интерферон и др. В-лимфоциты под действием переработанного моноцитами антигена и медиаторов превращаются в плазмоциты, вырабатывающие специфические антитела. Некоторые формы Т-лимфоцитов (киллеры, супрессо- ры, хелпер) и В-лимфоциты вместе с моноцитами образуют мощный клеточный фактор защиты организма от вирусов.
Таким образом, противовирусный иммунитет, как и иммунитет против других инфекционных агентов, — это комплекс защитных факторов, направленных на сохранение и восстановление постоянства внутренней среды организма в целом, гомеостаза клеток в частности. Вместе с тем противовирусный иммунитет имеет и присущее ему своеобразие, заключающееся прежде всего в том, что в нем главенствуют процессы, происходящие на клеточном и молекулярном уровнях.
Дата добавления: 2016-10-30; просмотров: 5504 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2020 lektsii.org — Контакты — Последнее добавление
