Миелоидные клетки врожденного иммунитета
Реализация врожденного иммунитета обусловлена деятельностью многих типов клеток. Основную роль при этом играют клетки миелоидного происхождения, играющие роль классических эффекторов врожденного иммунитета.
К миелоидным клеткам относят, в первую очередь, большинство лейкоцитов крови (все лейкоциты, кроме лимфоцитов). Все они развиваются в органах кроветворения (у взрослых млекопитающих, включая человека, — в костном мозгу), все проходят стадию циркуляции в составе лейкоцитов крови. Одни клетки (дендритные, тучные) циркулируют настолько кратковременно и в столь малом количестве, что при обычном определении лейкоцитарной формулы их выявить не удается. Другие клетки (нейтрофилы, моноциты) представляют основной компонент пула лейкоцитов крови. Все разновидности миелоидных клеток спонтанно мигрируют из крови в ткани, где быстро погибают (нейтрофилы) или длительно функционируют, проникая в качестве резидентных клеток практически во все органы и ткани, изменяя при этом под влиянием микроокружения свои морфофункциональные особенности (так, к тканевым формам моноцитов относят макрофаги и миелоидные дендритные клетки). Кроме того, кровоток служит депо, из которого клетки мигрируют в очаги развивающегося воспаления (например, при проникновении патогенов и т.д.), где преимущественно и реализуется их защитная функция. Таким образом, участие миелоидных клеток в обеспечении врожденного иммунитета складывается из экстренной реакции клеток, мобилизуемых из кровотока в условиях воспаления, и постоянной «фоновой» деятельности резидентных клеток. Дендритным клеткам принадлежит другая важная особенность — они обеспечивают запуск адаптивного иммунитета.
Кроветворные стволовые клетки и миелопоэз
Как уже отмечено, у взрослых млекопитающих, включая человека, миелопоэз происходит в костном мозгу. Все клетки крови происходят от гемопоэтических стволовых клеток. Стволовые кроветворные клетки проходят 3 стадии развития, различающиеся по способности восстанавливать кроветворение при переносе их облученным животным:
— стволовые клетки длительного действия;
— стволовые клетки короткого действия;
— мультипотентныеродоначальные клетки
Для всех стадий характерен мембранный фенотип Lin—Sca-l+
c-Kit+
[Lin — линейные маркеры; Sca-1 — антиген стволовых клеток (Stemcellantigen);
с-Kit — лиганд фактора стволовых клеток SCF (Stemcellfactor)]. Стволовые
клетки на 2-й и 3-й стадии развития несут на поверхности молекулу CD34.
Этот маркер чаще всего используют в качестве идентификационного для выявления стволовых клеток и их ближайших потомков. Для гемопоэтических стволовых клеток человека характерно отсутствие линейных маркеров, наличие молекулы CD34 и отсутствие молекулы CD38. Последняя появляется на стадии коммитированных предковых клеток — общих лимфоидного (CLP) и миелоидного предшественников. В костном мозгу человека содержится 0,5—5%
CD34+ клеток, только 1—10% из них лишены CD38, т.е. могут рассматриватьсякак кандидаты в стволовые клетки. Истинных стволовых клеток, т.е. клеток, способных длительно поддерживать гемопоэзinvitro или при пересадке в организм, значительно меньше — 1 на 104
Lin—CD34+
Thy-1—клеток. Стволовые клетки делятся медленно (около 5% находятся в S и G2 фазах клеточного цикла; каждая клетка делится 1 раз в 30—60 сут).
Жизнеспособность стволовых клеток обеспечивается стромальными клетками костного мозга, формирующими их нишу. Большинство стволовых кроветворных клеток расположено в эндостальной части костного мозга, а также в синусоидах (соответственно — эндостальная и сосудистая ниши).
Таких клеток мало в центральной части костного мозга. Основную роль в поддержании жизнеспособности и обеспечении функционирования стволовых клеток играют их контакты со специализированными остеобластами
В зонах контакта происходит взаимодействие многих пар молекул, включая молекулы адгезии (интегрины и их рецепторы), мембранные цитокины (SCF и его лиганд, c-Kit), хемотаксические молекулы (хемокины и их рецепторы) и т.д. Роль растворимых факторов (цитокинов) в регуляции жизнеспособности и активности стволовых клеток невелика. Стволовые клетки входят в клеточный цикл и дифференцируются только при ослаблении связи с нишей и утрате контактов с остеобластами. Важная особенность стволовых клеток — сбалансированность процессов пролиферации и дифференцировки: на уровне популяции одна из дочерних клеток продолжает делиться, тогда как другая подвергается дифференцировке, то есть созревает. В результате пролиферирующие клетки образуют как бы ствол, от которого постоянно отделяются клетки, уходящие в дифференцировку.
Дифференцируясь, стволовые кроветворные клетки дают начало двум основным ветвям клеток крови — миелоидной и лимфоидной. Несколькосхематизируя, можно сказать, что эти ветви обеспечивают развитие клеток соответственно врожденного и адаптивного иммунитета. В этой главе рассмотрим только миелоидный путь развития клеток крови, проиллюстрированный на рис. 2.2. Исходные клетки этого пути развития — общие миелоидные предшественники. Они образуются как в эндостальной, так и в сосудистой нишах и отличаются от стволовых клеток отсутствием мембранной молекулы Sca-1, а от CLP — рецептора для IL-7.
Из общего миелоидного предшественника происходят все клетки крови, кроме лимфоцитов. Рассмотрим только развитие клеток врожденного иммунитета по 3 линиям дифференцировки. Наиболее важная из них — грануло-цитарно-макрофагальная, или GM-линия. Она дает начало двум дочерним линиям — моноцитарной (М-линия) и гранулоцитарной (G-линия). Вопрос о развитии эозинофилов и базофилов до конца не решен. Есть данные оналичии у них общего предшественника, дифференцирующегося впоследствии на эозинофильную и базофильную линии. С помощью традиционного морфологического подхода выделяют несколько стадий развития миелоидных клеток: миелобласты, промиелоциты, миелоциты, метамиелоциты, палочкоядерные и сегментоядерные (зрелые) формы. Клетки на 2 последних стадиях в норме присутствуют в кровотоке. Накапливается все больше свидетельств, что традиционное представление гемопоэза в виде «дерева» не точно, поскольку описаны многочисленные отклонения от сложившейся схемы. Так, известны клетки-предшественники, общие для моноцитов и В-лимфоцитов или моноцитов и Т-лимфоцитов. Гемопоэзусвойственазначительная степень пластичности.
Для дифференцировки миелоидных (как и любых других) клеток необходима экспрессия определенного набора факторов транскрипции. Этиядерные белки обладают сродством к конкретным последовательностям ДНК в промоторных участках генов и, соединяясь с ними, обеспечивают экспрессию этих генов. Обычно с промотором соединяется целый комплекс транскрипционных факторов, среди которых есть постоянно присутствующие (конститутивные) и индуцируемые факторы; некоторые из них характерны для различных стадий развития клеток. Так, при миелопоэзедля большинства линий и стадий развития клеток выявлены относительно специфичные для них транскрипционные факторы (см. рис. 2.2). Например, экспрессия транскрипционного фактораIkaros характерна для лимфоидной, но не миелоидной ветви гемопоэза. При миелопоэзе высокий уровень экспрессии фактора PU.1 необходим для развития клеток GM-линии, низкий уровень выявляют в клетках эозинофильного ряда, а в базофилах этот фактор отсутствует. Моноцитарный и гранулоцитарный ряды различаютсяскорее комбинацией транскрипционных факторов, чем наличием одного специфичного; нейтрофилы отличаются от моноцитов экспрессией разныхизоформ фактора С/ЕВР. Спектры дифференцировочных факторов базофилов и других миелоидных клеток крови не перекрываются.
Незрелые кроветворные клетки легко подвергаются апоптозу. Для сохранения жизнеспособности им необходимо присутствие в микроокружении цитокинов. Основным цитокином, общим практически для всех миелоидных клеток, начиная от общего миелоидного предшественника, считают гранулоцитарно-макрофагальный колониестимулирующий фактор(GM-CSF). На ранних этапах миелопоэза сходную роль выполняет IL-3, называемый также полипоэтином. При созревании и специализации клеток для сохранения жизнеспособности им необходимы линейно-специфические цитокины: для моноцитарного ряда — моноцитарно-макрофагальный колониестимулирующий фактор (M-CSF), а для нейтрофильного — гранулоцитарныйколониестимулирующий фактор (G-CSF). Подобную роль приразвитии эозинофилов играет IL-5. Во всех этих случаях наряду с названными цитокинами роль фактора выживания и колониестимулирующегофактора выполняют GM-CSF и, в меньшей степени, IL-3. Базофилам для развития нужен комплекс факторов, в котором главную роль играет CSF.
Между появлением гранулоцитарно-макрофагального предшественника и его дифференцировкой на моноцитарно-макрофагальный и гранулоцитарный предшественники проходит около 5 сут — это один из самых длительных этапов миелопоэза. Следующий этап — созревание — значительно отличается по продолжительности для моноцитов и гранулоцитов: если для созревания моноцита необходимо 2—3 сут, то для созревания нейтрофильного гранулоцита — 10—12 сут. После созревания моноциты находятся в костном мозгу еще сутки и затем покидают его, поступая в кровоток. При этом клетки сохраняют способность к делению и дальнейшей дифференцировке. Нейтрофилы остаются в костном мозгу в течение 1—2 сут и выходят в кровь не просто зрелой, а старой клеткой с ограниченными способностями, неспособной к делению, индуцированной экспрессии генов и синтезу белка. Наиболее короткий промежуток времени требуется для развития в костном мозгу эозинофилов (2—4 сут). Аналогичные данные для базофилов отсутствуют. Продолжительность пребывания различных миелоидных клеток в костном мозгу, кровотоке и тканях сопоставлена на рис. 2.3.
Выход лейкоцитов из костного мозга в кровоток происходит вследствие ослабления взаимодействия хемокинов, выделяемых стромальными клетками костного мозга с рецепторами лейкоцитов. Наиболее важный хемокин, удерживающий созревающие клетки в костном мозгу, — СХС12 (SDF-1 — Stromaderivedfactor 1, фактор стромальных клеток 1), распознаваемый рецептором CXCR4 (о хемокинах и их рецепторах см. раздел 2.3.2). Под влияниемколониестимулирующих факторов (гемопоэтинов) происходит ослабление выработки хемокинов и экспрессии их рецепторов, что позволяет созревшим клеткам покинуть костный мозг. Сегментоядерные (нейтрофильные и эозинофильные) лейкоциты пребывают в кровотоке менее 12 ч; моноцитыциркулируют в течение нескольких дней. Затем клетки мигрируют из крови в ткани. Этот процесс регулируется хемокиновыми сигналами и происходит с участием молекул адгезии (селектинов, интегринов) и их рецепторов.
В норме экстравазация лейкоцитов осуществляется по тем же законам, что и при воспалении, но менее интенсивно в связи с меньшей проницаемостью сосудистой стенки и более слабой хемокиновой стимуляцией.
Длительность пребывания миелоидных клеток в тканях также существенно варьирует: для нейтрофилов и эозинофилов она значительно меньше, чем для моноцитов. Так, в тканях нейтрофилы живут всего 3—5 сут, эозинофилы — 10—12 сут, тогда как моноциты (точнее, макрофаги, в которыеони превращаются в тканевом микроокружении) могут находиться в тканях до нескольких лет (для разных субпопуляций макрофагов этот показатель существенно различается). Нейтрофилы, эозинофилы и базофилы мобилизуются из крови в ткани в особых экстренных случаях (острое воспаление,аллергические процессы). Моноциты/макрофаги, наоборот, играют преимущественно роль клеток, длительное время живущих и функционирующих в различных тканях. В связи с этим нужно отметить значительно более высокую производительность гранулоцитопоэза по сравнению с моноцитопоэзом. За сутки в организме человека образуется и поступает в кровоток около 1011 нейтрофилов, что по массе составляет около 100 г, т.е. примерно 0,1% от массы тела; такое же количество гранулоцитов ежедневно погибает. Производительность моноцитопоэза в 20 раз ниже: за сутки образуетсяи поступает в кровоток до 5х109 моноцитов. Это обусловлено значительнобольшей продолжительностью жизни моноцитов/макрофагов.
Существует еще по крайней мере 2 разновидности миелоидных клеток, происходящих из костного мозга, но использующих кровяное русло только в качестве кратковременного транзитного участка по пути в ткани — дендритные и тучные клетки.
Таблицу посмотри.
Источник
Глава 12. Развитие иммунной системы в онтогенезе
■ Большинствоклетокиммуннойсистемы образуется из гемопоэтических стволовых клеток.
■ Развитиеклетокразныхтипов (рядов, илилиний, дифференцировки) зависит от межклеточных взаимодействий и цитокинов.
■ Лимфоидныестволовыеклетки развиваются и созревают в первичных лимфоидных органах. Этот процесс называется лимфопоэзом.
■ Т—лимфоциты при развитии в тимусе подвергаются положительной и отрицательной селекции.
■ В—клеткимлекопитающих развиваются главным образом в печени плода, а после рождения — в костном мозге. Этот процесс продолжается в течение всей жизни организма. В-клетки в местах своего развития также подвергаются отбору.
■ Репертуар антител, существующий у взрослых особей, формируется в процессе лимфопоэза путем рекомбинации генных сегментов, кодирующих ТкР и Ig.
■ Вцентрахразмножения происходит олигоклональная пролиферация В-клеток, переключение изотипа антител, повышение аффинности и формирование иммунологической памяти.
Эффективное функционирование иммунной системы зависит от взаимодействия многочисленных клеточных и гуморальных компонентов, которые в пре- и постнатальный периоды созревают с различной скоростью. Многие клетки, участвующие в иммунном ответе, происходят от недифференцированных гемопоэтических стволовых клеток (ГСК). Под влиянием факторов микроокружения — взаимодействия с соседними клетками и присутствия растворимых или мембраносвязанных цитокинов — дифференцировка ГСК происходит в разных направлениях (рис. 12.1).
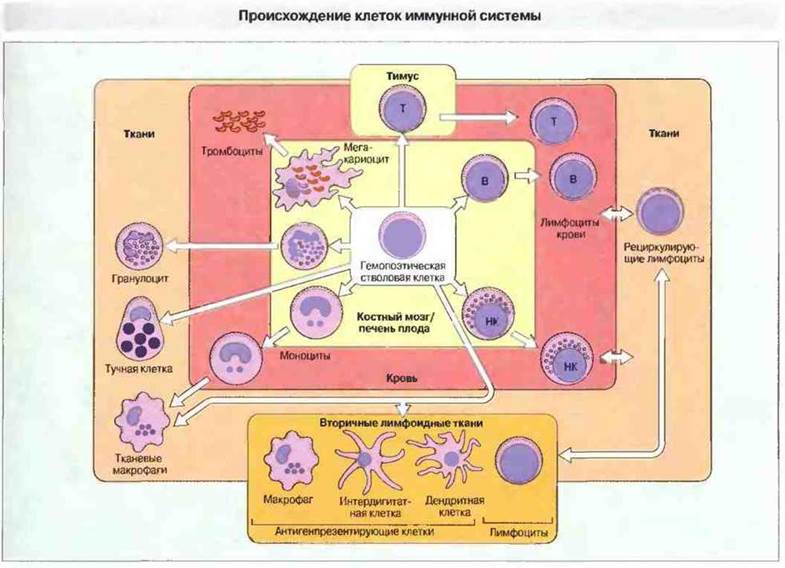
Рис. 12.1. Все изображенные на рисунке клетки происходят от гемопоэтической стволовой клетки. Тромбоциты, продуцируемые мегакариоцитами, поступают в кровоток. Гранулоциты и моноциты мигрируют из кровотока в ткани. Тучные клетки присутствуют во всех тканях. В-клетки у млекопитающих созревают в печени плода и костном мозге, а Т-клетки — в тимусе. Местом образования больших гранулярных лимфоцитов, обладающих активностью нормальных киллеров (НК), служит, вероятно, костный мозг. Лимфоциты мигрируют из кровотока, проходят через вторичные лимфоидные ткани и вновь поступают в кровоток. Роль антигенпрезентирующих клеток во вторичных лимфоидных тканях выполняют интердигитатные и дендритные клетки.
У млекопитающих в период внутриутробного развития ГСК присутствуют в желточном мешке, печени, селезенке и костном мозге. После рождения и в зрелом организме они обычно сохраняются лишь в костном мозге. Эти «самообновляющиеся» путем деления ГСК под влиянием разнообразных местных (в участках гемопоэза) факторов роста и дифференцировки дают начало большинству или даже всем клеткам иммунной системы.
Из ГСК образуются клетки четырех главных рядов (линий) дифференцировки:
• эритроидного (эритроциты),
• мегакариош(тарного (тромбоциты),
• миелоидного (гранулоииты и моноядерные фагоциты) и
• лимфоидного (лимфоциты). Антигенпрезентируюшие клетки в основном, но не исключительно, развиваются из миелоидных клеток-предшественников. Клетки миелоидного и лимфоидного рядов наиболее важны для функционирования иммунной системы.
МИЕЛОИДНЫЕ КЛЕТКИ
У человека миелопоэз начинается в печени, примерно на 6 неделе внутриутробного развития. Изучение роста колоний из индивидуальных стволовых клеток in vitro показало, что первая образующаяся из ГСК клетка-предшественник представляет собой колониеобразующую единицу (КОЕ), которая может дать начало образованию гранулоцитов, эритроцитов, моноцитов и мегакариоцитов (КОЕ-ГЭММ). Созревание этих клеток происходит под влиянием колониестимулируюших факторов (КСФ) и ряда интерлейкинов, в том числе ИЛ-1, ИЛ-3, ИЛ-4, ИЛ-5 и ИЛ-6 (рис. 12.2). Все они играют важную роль в положительной регуляции (стимуляции) гемопоэза и продуцируются главным образом стромальными клетками костного мозга, но также и зрелыми формами дифференцированных миелоидных и лимфоидных клеток. Другие цитокины (например, ТФРβ) могут осуществлять понижающую регуляцию (подавление) гемопоэза.
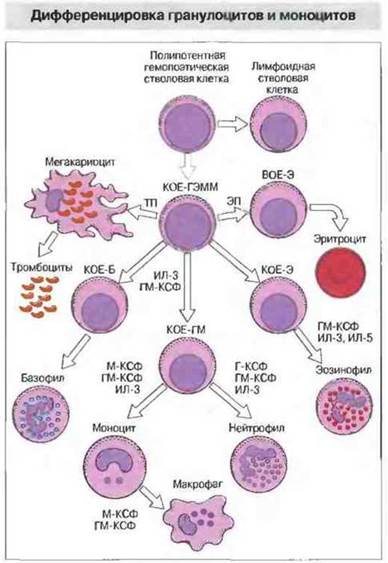
Рис. 12.2. Полипотентные гепомоэтические стволовые клетки превращаются в колониеобразующие единицы (КОЕ) КОЕ-ГЭММ может давать начало всем клеткам крови, за исключением лимфоцитов. Образование из стволовой клетки любого из пяти типов клеток [мегакариоцитов, эритроцитов — через этап предшественника, называемого взрывообразующей единицей эритроидного ряда (ВОЕ-Э), базофилов, нейтрофилов или эозимофилов] индуцирует ИЛ-3 и фактор, стимулирующий образование колоний гранулоцитов и макрофагов (ГМ-КСФ); эти же факторы необходимы для дальнейшей дифференцировки гранулоцитов и моноцитов. Образование эозинофилов (Э) и КОЕ-3 стимулируется ИЛ-5. Нейтрофилы и моноциты образуются из КОЕ-ГМ под действием соответственно Г-КСФ и М-КСФ. Оба эти фактора, как и другие цитокины (включая ИЛ-1, ИЛ-4 и ИЛ-6), стимулируют дифференцировку моноцитов в макрофаги. Образование мегакариоцитов стимулируется тромбопоэтином (ТП) (Б — базофил; ЭЛ — эритропоэтин; Г — гранулоцит; М — моноцит.)
Нейтрофилы и моноциты развиваются из общих клеток-предшественников
Образование нейтрофилов. Клеткой — предшественником нейтрофилов (вид гранулоцитов) и мононуклеарных фагоцитов (макрофагов) служит КОЕ-ГМ. При дифференцировке в нейтрофилы клетки проходят несколько морфологических стадий. Из миелобластов образуются промиелоциты и затем миелоциты, которые созревают и поступают в кровоток в виде нейтрофилов. Однонаправленная дифференцировка клеток КОЕ-ГМ в зрелые нейтрофилы обусловлена появлением у них на разных стадиях развития рецепторов для специфических факторов роста и дифференцировки.
По мере созревания гранулоцитов на их поверхности исчезают или появляются поверхностные дифференцировочные маркеры (рис. 12.3). Например, клетки КОЕ-ГМ экспрессируют молекулы МНС класса II и маркер CD38, отсутствующие на зрелых нейтрофилах. К другим молекулам поверхности, экспрессируемым в процессе дифференцировки, относятся CD13, CDI4
(представлен в небольшой концентрации), CD15 (Х-детерминанта группы крови Льюис), CD29 (β1-интегрин), VLA-4 (CD49d, α-цепь), лейкоцитарные интегрины CD11а, b, с и αD в ассоциации с β2-цепями CD18, рецепторы комплемента и Fcγ-рецепторы (CD 16) (см. рис. 2.42).
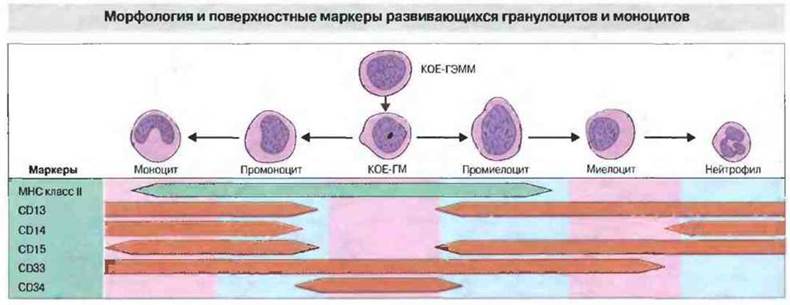
Рис. 12.3. Клетки моноцитарного и нейтрофильного линий дифференцировки образуются из общей клетки-предшественника, КОЕ-ГМ. Дифференцировка по каждому из этих путей сопровождается утратой маркера CD34. На моноцитах сохраняется CD33, тогда как на зрелых нейтрофилах эти молекулы, равно как и молекулы МНС класса It, отсутствуют. Маркер CD14 экспрессируется на моноцитах, но лишь в слабой степени на некоторых гранулоцитах, возможно при активации.
Функциональную активность гранулоцитов, находящихся на различных стадиях созревания, оценить трудно, но, по-видимому, полным функциональным потенциалом обладают только зрелые клетки. Ряд данных свидетельствует о том, что активность нейтрофилов, определяемая по фагоцитозу или хемотаксису, у плода ниже, чем в зрелом организме. Однако это может быть отчасти связано с меньшим содержанием опсонинов в сыворотке плода, а не с особенностями самих клеток. Для приобретения активности нейтрофилам необходимо непосредственное взаимодействие с микроорганизмами или с цитокинами, образующимися при иммунном ответе на антиген, (или с теми и другими вместе) в присутствии опсонинов. Это может лимитировать активность нейтрофилов на раннем этапе развития организма. Активация нейтрофилов цитокинами и хемокинами является также необходимым условием их миграции из крови в ткани.
Образование моноцитов. При дифференцировке по моноцитарному пути из КОЕ-ГМ вначале образуются пролиферирующие монобласты. Они дифференцируются в промоноциты и, наконец, в зрелые моноциты крови. Считается, что циркулирующие моноциты служат возобновляемым пулом для образования тканевых макрофагов, например макрофагов легких. Различные формы макрофагов составляют систему мононуклеарных фагоцитов (см. гл. 2).
Зрелые нейтрофилы и моноциты/макрофаги лишены CD34 и других маркеров ранних стадий дифференцировки. Однако моноциты, в отличие от нейтрофилов, продолжают экспрессировать большое количество молекул МНС класса II (рис. 12.3), необходимых для презентации антигена Т- клеткам. Моноциты синтезируют также многие из тех поверхностных молекул, которые характерны для зрелых нейтрофилов (см. рис. 2.28).
На стадиях дифференцировки определить функциональные возможности моноцитов, как и гранулоцитов, весьма трудно. Однако изучение in vitro некоторых миелоидных опухолей, клетки которых предположительно представляют собой моноциты на разных стадиях дифференцировки, свидетельствует о том, что как фагоцитарная активность, так и цитотоксичность, опосредуемая Fc-рецептором, достигают оптимального уровня только на стадии зрелых макрофагов. У новорожденного и взрослого человека моноциты вырабатывают цитокин ИЛ-1 с равной эффективностью, но у новорожденного эта функция слабее повышается под действием ИФγ, чем у взрослого.
Дендритные клетки развиваются из стволовых клеток костного мозга
Большинство классических антигенпрезентирующих клеток (АПК), включая макрофаги, клетки Лангерганса, интердигитатные и дендритные клетки, присутствует в организме уже при рождении. По всей вероятности, основная их масса образуется из стволовых клеток костного мозга. Возможно, они происходят из одной и той же клетки-предшественника CD34+(КОЕ-ГЭММ). Морфологические, цитохимические и функциональные особенности разных АПК должны тогда определяться последующим влиянием факторов микроокружения, например цитокинов. Другая возможность состоит в том, что АП К образуются из разных стволовых клеток и по разным направлениям дифференцировки. Важное исключение составляют фолликулярные дендритные клетки (ФДК), локализованные в центрах размножения внутри вторичных лимфоидных фолликулов и происходящие, возможно, от мезенхимных клеток. В первичных фолликулах периферических лимфоидных тканей ФДК присутствуют уже при рождении. В отличие от других АПК они лишены подвижности.
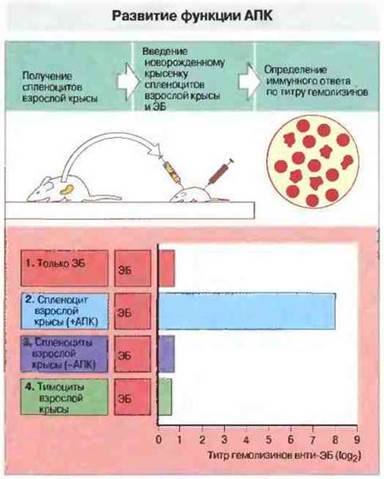
Уже на очень ранних стадиях развития организма АПК присутствуют в тимусе, причем их участие в МНС-рестрикции и селекции Т-клеток показывает, что по крайней мере некоторые из них к этому времени достигают полной зрелости. Однако активность АПК на ранних стадиях развития организма явно неоптимальна. У новорожденных крысят, например, образование антител к эритроцитам барана происходит только при одновременном введении АПК взрослых крыс (рис. 12.4).

Рис. 12.4. Развитие функции антигенпрезентирующей клетки процессинга и презентации антигена. В этом опыте новорожденным крысятам вводили: 1) только эритроциты барана (ЭБ), 2) ЭБ + клетки селезенки (содержащей АПК) взрослых крыс, 3) ЭБ + клетки селезенки, лишенной АПК, или 4) ЭБ + зрелые тимоциты. Во всех случаях взрослые крысы принадлежали к той же линии, что и новорожденные. У крысят каждой группы регистрировали гуморальный иммунный ответ — появление антител. У новорожденных крысят, которым вводили только ЭБ, антитела к ЭБ антигенам не образовывались. Однако при одновременном введении спленоцитов взрослых крыс (вариант 2) иммунный ответ развивался. Ни зрелые спленоциты в отсутствие АПК, ни тимоциты сами по себе не вызывали продукции антител. Следовательно, АПК новорожденных особей неспособны эффективно осуществлять процессинг и презентацию ЭБ-антигенов.
Источник
