Мрт при очаговых поражениях печени
Очаговые образования в печени являются одной из важных проблем современной лучевой диагностики в онкологии и хирургии. Особенно это актуально для пациентов, имеющих отягощенный анамнез по колоректальному раку и циррозу печени. Выживаемость больных в основном определяется наличием или отсутствием отдаленных метастазов. У большинства этих больных поражение печени является первым признаком распространенности поражения. Поэтому скрининговые обследования на предмет поиска метастазов являются предпосылкой для планирования дальнейшего лечения и наблюдения за больным.
Очаговые образования в печени являются одной из важных проблем современной лучевой диагностики в онкологии и хирургии. В мире колоректальным раком ежегодно заболевает 1–1,2 млн. человек. У 50–60% пациентов с течением времени развиваются метастазы. Большая часть пациентов (до 80–85%) имеют метастазы в печень, а у половины из этого числа печень является единственным органом метастазирования. Выживаемость этой группы больных определяется наличием или отсутствием отдаленных метастазов. У большинства пациентов поражение печени является первым признаком распространенности поражения. Поэтому скрининговые обследования на предмет поиска метастатического поражения являются предпосылкой для планирования дальнейшего лечения и наблюдения за больным.
Пациент М. Оперирован по поводу колоректального рака 1,5 года назад. При КТ и УЗИ выявлены очаговые образования печени (Рис. 1а). При ПЭТ исследовании — изолированное метастатическое поражение печени (Рис. 1б).
Доказана необходимость хирургического удаления метастазов печени, т.к. 5-ти летняя выживаемость таких пациентов при химиотерапии составляет не более 5%, а без лечения — 1%. В то же время, после радикальной резекции печени у 35%–40% пациентов удается продлить жизнь на 5 и более лет.
Для оценки возможности проведения оперативного вмешательства важное значение придается предоперационной оценке распространенности болезни и определения злокачественности выявленных очаговых образований. При обследовании абсолютно необходимы компьютерная томография печени, рентгенография легких, определение уровня раково-эмбрионального антигена. Для определения тактики оперативного лечения полезно выполнение компьютерной томографии печени с одновременным контрастированием печеночной артерии, т.к. доказано, что в отличие от нормальной ткани печени, кровоснабжаемой через v. porta, метастазы кровоснабжаются в основном через a. hepatica. Также показано интраоперационное УЗИ печени. Нераспознанные ранее метастазы в таком случае могут быть обнаружены в 15–25% случаев.
Пациент В. При КТ (Рис. 2а) выявлено объемное образование печени, подозрительное на метастатическое поражение. При проведении ПЭТ (Рис. 2б) подтверждена злокачественная природа выявленного образования, а также обнаружено метастатическое поражение лимфоузлов ворот печени и средостения.
Еще одной проблемой современной онкологии является развитие первичного рака печени на фоне цирроза. Вероятно, это связано с развитием новых методов, благодаря которым стало возможным диагностировать очаговые образования печени даже небольших размеров и в начальной стадии развития. По ориентировочным подсчетам в мире ежегодно регистрируется более 500000 новых случаев рака печени. Как известно, цирроз печени — «благодатная почва» для развития гепатоцеллюлярного рака (ГЦР), а ГЦР возникающий на фоне цирроза, во многих странах стал одной из проблем здравоохранения. В среднем, развитие опухоли до 2 см в диаметре проходит в течение 4–12 мес. Около 50% узлов в цирротической печени диаметром менее 1 см не имеют опухолевой природы. Наличие фиброза, регенераторных узлов, участков некроза — все это создает картину гетерогенной неоднородности паренхимы печени при циррозе и затрудняет выявление опухолей печени. Большую сложность представляет идентификация регенераторных узлов при циррозе печени, где их довольно трудно отличить от других очаговых образований печени. По данным Bolondi, Sofia, et al. (2001), ГЦР является частой причиной смерти у пациентов с циррозом печени, и любое очаговое образование печени при циррозе, прежде всего, должно наводить на мысль о ГЦР. С другой стороны важно понимать, что любое образование в печени при циррозе может выглядеть атипичным и симулировать узлы регенерации, так как последние при циррозе печени также кровоснабжаются ветвями печеночной артерии и контрастируются так же, как ГЦР.
Давно изучены семиотика гепатоцеллюлярного рака, характер контрастирования опухоли, косвенные признаки, но все это, к сожалению, не позволяет с уверенностью диагностировать цирроз-рак, если размер опухоли менее 2 см, при этом ранняя диагностика ГЦР крайне важна, так как увеличивается вероятность благоприятного результата после резекции или трансплантации печени.
Пациент Г. При УЗИ (Рис. 3а) было выявлено очаговое образование печени, расцененное как доброкачественное. При проведении КТ с болюсным контрастным усилением (Рис. 3б) характер образования не позволял исключить злокачественный процесс. При ПЭТ исследовании (Рис. 3в) — объемное образование печени злокачественного характера (ГЦР).
Следующей проблемой лучевой диагностики, хирургии и онкологии являются образования печени, обнаруженные случайно. В этом случае необходима дифференциальная диагностика выявленных очагов во избежание ненужных лечебных мероприятий и хирургических вмешательств, а получение неинвазивными методами надежных характеристик образований печени стало почти так же важно, как и само обнаружение этих образований.
Пациент Д. При КТ (Рис. 4а) и УЗИ (Рис. 4б) были выявлены очаговые образования печени неясной этиологии. ПЭТ исследование (Рис. 4в) позволило исключить злокачественный процесс. Диагноз: цирроз печени. Узлы регенерации.
В современном арсенале врачей есть большое количество диагностических методик, позволяющих установить диагноз. И в настоящее время все большее значение в диагностической практике приобретает позитронно-эмиссионная томография (ПЭТ). Не стоит рассматривать ПЭТ изолированно от других методов исследования, поскольку, только комплексный диагностический подход может дать наиболее полную картину заболевания.
Несмотря на особенности и ограничения, позитронно-эмиссионная томография заняла свое место в диагностическом алгоритме обследования пациентов, так как, являясь функциональным методом, позволяет изучать биохимические процессы организма на молекулярном уровне в томографическом режиме.
Наибольшую популярность в онкологической практике получили исследования с 18F-фтордезоксиглюкозой (ФДГ), отражающей углеводный обмен. Принцип регистрации опухолей с использованием ФДГ основан на явлении неконтролируемо повышенной утилизации глюкозы злокачественными клетками, и как следствие, повышение захвата ФДГ опухолевой тканью по сравнению с нормальной. Повышенный гликолиз в злокачественных опухолях находится в прямой зависимости от степени злокачественности новообразования. Кроме того, злокачественные опухоли характеризуются относительно высокой активностью гексокиназы и низкой активностью фосфатазы. Образующийся в результате биохимических реакций 18F-ФДГ-6-фосфат не вступает в дальнейшие реакции гликолиза и тем самым формируется «метаболическая ловушка», что приводит к повышенному содержанию 18F-ФДГ-6-фосфата в ткани опухоли и способствует ее выявлению.
В ряде случаев методы лучевой диагностики (УЗИ, РКТ, МРТ) не позволяют однозначно интерпретировать морфологическую структуру выявленных очаговых образований в печени, особенно при циррозе. ПЭТ позволяет оценить биологическую активность этих очагов, динамику их изменений в процессе лечения, определить регионарное и отдаленное метастазирование в организме за одно исследование. Это минимально инвазивная процедура, требующая только внутривенной инъекции, позволяющая атравматично выявить злокачественные образования.
Нами было обследовано 90 пациентов с очаговыми поражениями печени.
КТ проводилась на аппарате «Somatom Plus 4» фирмы Siemens в спиральном режиме с болюсным контрастным усилением. У всех пациентов были выявлены различной формы и размеров очаговые образования в печени, в большей или меньшей степени накапливающие контрастный препарат в артериальную и последующую фазы контрастирования.
УЗИ брюшной полости проводилось на аппарате «Sonoline Elegra» фирмы Siemens датчиком 3,5 MHz. На УЗИ было подтверждено наличие объемных образований в печени у 94% пациентов. У 6% пациентов очаговых изменений паренхимы печени выявлено не было.
ПЭТ обследование осуществлялось на томографе «ECAT EXACT 47» фирмы Siemens с использованием 18F-ФДГ. Сканирование проводилось в статическом режиме по протоколу Whole body в режиме 2D. Обработка полученных данных включала в себя визуальную оценку изображения «всего тела» пациента, а также измерение коэффициента дифференциального накопления ФДГ в выявленных очагах.
В результате у 37% пациентов в печени очагов повышенного захвата ФДГ выявлено не было. При последующем гистологическом исследовании пациентам был подтвержден диагноз цирроза. У 6% пациентов были обнаружены очаги гиперфиксации ФДГ, не визуализирующиеся на УЗИ и парадоксально изменяющие свои характеристики при КТ исследовании. При гистологическом исследовании у этой группы пациентов верифицирован гепатоцеллюлярный рак.
У 54% пациентов в печени были обнаружены очаги с высоким уровнем накопления ФДГ, которые соответствовали по размерам и положению объемным образованиям, выявленным при КТ и УЗИ. Из них в 44% случаях, кроме участков гиперфиксации в печени, были выявлены множественные внепеченочные очаги повышенного накопления препарата, отражающие генерализацию опухолевого процесса.
У 3% изолированные очаги гиперфиксации ФДГ при ПЭТ определялись в печени, количественно больше чем при КТ и УЗИ исследованиях. Количество очагов, их расположение и отсутствие накопления ФДГ в регионарных лимфоузлах и других органах позволило провести хирургическое лечение с последующим гистологическим исследованием, при котором было подтверждено количество выявленных очагов и их метастатическая природа.
Таким образом, позитронно-эмиссионная томография оказалась высокоэффективным методом в выявлении метастазов в печень и дифференциальной диагностике их от доброкачественных очаговых образований. ПЭТ позволяет выявить внепеченочные метастазы, тем самым, изменяя стадию заболевания и позволяя скорректировать проводимую терапию и тактику хирургического вмешательства. Метод ПЭТ позволяет неинвазивно оценивать степень поражения печени и других органов за одно исследование, сокращая время постановки диагноза.
Применение ПЭТ является необходимым методом диагностики у пациентов с очаговыми образованиями печени, несмотря на высокую стоимость исследования.
Радкевич Л.А., Зубанов А.Г., Родченко З.П., Зайцева А.Ю.
Статья добавлена 18 июля 2013 г.
Лучевая диагностика метастазов в печени
а) Определение:
• Распространение злокачественного новообразования в печеночную паренхиму
б) Визуализация:
1. Общая характеристика:
• Ключевой диагностический признак:
о Множественные образования рассредоточенные по всей печени случайным образом
• Локализация:
о Обе доли печени
• Размер:
о Варьирует от нескольких мм до >10 см
• Основные положения:
о Чаще всего являются злокачественной опухолью печени
о Печень занимает второе место по частоте метастатического поражения и уступает лишь региональным лимфатическим узлам
о Согласно данным, получаемым при аутопсии, до 55% онкологических больных имеют метастазы в печени
2. УЗИ метастазов в печени:
• Серошкальное ультразвуковое исследование:
о Округлое или овальное образование с гладкими или неровными краями
о При крупных размерах или большом числе нарушают архитектонику органа
о Гипоэхогенные метастазы:
— Обычно из гиповаскулярных опухолей
о Гиперэхогенные метастазы:
— Васкуляризированные метастазы; из нейроэндокринных опухолей (классических карциноидных), холангиокарциномы, почечноклеточного рака, меланомы
о Очаги по типу «бычьего глаза» или «мишени»:
— Чередующиеся слои гипер- и гипоэхогенных тканей
— Солидное образование с гипоэхогенным ободком или венчиком
— Обычно из агрессивных первичных опухолей
— Классический пример: бронхогенный рак
о Кистозные/некротические метастазы:
— Могут вызывать заднее акустические усиление
— Бугристая поверхность, толстые стенки, уровни жидкость-жидкость, внутренние перегородки/взвесь, отличающиеся их от простых кист
— Некротизировавшийся центр может быть окружен неровными стенками и содержать взвесь
— Кистозные первичные опухоли: цистаденокарцинома поджелудочной железы/яичника; толстой кишки
— Некротизировавшиеся/леченные метастазы: саркома; плоскоклеточный рак
о Кальцинированные метастазы:
— Выраженно гиперэхогенная поверхность с акустической тенью или маленькими диффузными гиперэхогенными очагами
— Железистая первичная опухоль: толстая кишка, яичник
— Кальцинированная/оссифицированная первичная опухоль: остеосаркома, хондросаркома, нейробластома, злокачественная тератома
— Леченные метастазы
о Инфильтративные/диффузные метастазы:
— Первичная локализация: легкие или молочная железа
— Края инфильтративной опухоли часто образуют рефракционные тени
— Могут имитировать цирроз
— Могут затрагивать или деформировать ветви воротной вены или печеночные вены
• Цветовая допплерография:
о Повторяет васкуляризацию первичной опухоли
о УЗИ с контрастированием повышает выявляемость метастазов в печени:
— Васкуляризации в ложе опухоли
— Дефект в фазу Купфера после выхода микропузырьков
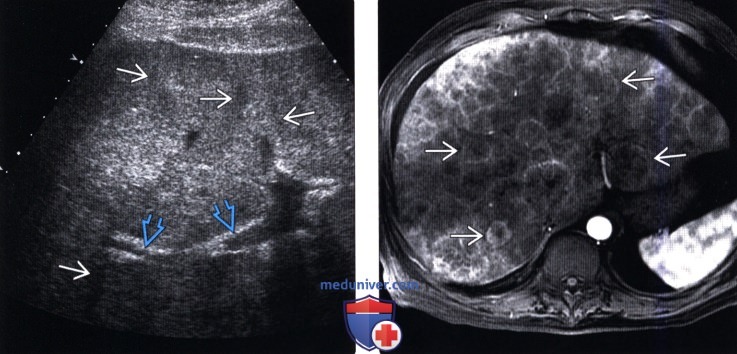
(Левый) Поперечный трансабдоминальный серошкальный УЗ срез у пациента с диффузным метастатическим поражением печени. Отмечается выраженная неоднородность печени с множеством рефракционных теней, вызванных изоэхогенными метастазами. Обратите внимание на деформацию ветвей воротной вены в результате компрессии.
(Правый) Т1-ВИ С+ FS МРТ у этого же пациента; видно, что неоднородность эхоструктуры печени при УЗИ вызвана множеством образований, практически полностью заместивших паренхиму печени.
3. КТ метастазов в печени:
• КТ без контрастирования:
о Кальцинированные: железистая аденокарцинома (толстая кишка), леченные метастазы (молочная железа), злокачественная тератома
о Кистозные метастазы (менее чем 20HU):
— Уровни жидкости, взвесь, узловатые стенки
— Может наблюдаться утолщение стенок или перегородок
— Обычно цистаденокарцинома или саркома (первичная опухоль поджелудочной железы, ЖКТ или яичника)
• КТ с контрастированием:
о Гиповаскулярные метастазы:
— Низкое затухание в центре с ободком контрастирования по периферии (например, эпителиальные метастазы)
— Видны васкуляризированные жизнеспособные участки опухоли на периферии и гиповаскулярный или некротический центр
— Ободок повышенного контрастирования также может быть обусловлен сдавливанием нормальной паренхимы
о Гиперваскулярные метастазы:
— Гиперденсивные в позднюю артериальную фазу изображения
— Могут присутствовать очаги некроза без гиперденсивного контрастирования
— Гипо- или изоденсивны при КТ без контрастирования и в портально-венозную фазу; часто в результате вымывания становятся гиподенсивными в отсроченную фазу
— Например, нейроэндокринные опухоли, рак щитовидной железы, молочной железы, почечноклеточный рак и фе-охромоцитома
4. МРТ метастазов в печени:
• Т1-ВИ:
о Метастазы меланомы: гиперинтенсивные из-за меланина
• Т2-ВИ:
о От умеренного до интенсивного сигнала
о Симптом «лампочки»: наблюдается при метастазировании кистозных и нейроэндокринных опухолей:
— Имитируют кисты или гемангиомы, но обычно с толстыми стенками или уровнем жидкости
• Т1-ВИ С+
о Гиповаскулярные метастазы:
— Картина контрастирования сходна с таковой при КТ с контрастированием
— Низкий уровень сигнала в центре и контрастирование в виде ободка по периферии
— Перифокальное усиление может быть вызвано васкуляризацией опухоли или отеком печеночной паренхимы
о Гиперваскулярные метастазы:
— Гиперинтенсивное усиление в артериальную фазу
о Гепатобилиарное контрастное вещество (гадоксетовая кислота): гепатобилиарная фаза (20 минут):
— Метастазы хорошо определяются как гипоинтенсивные очаговые поражения, в то время как не измененная паренхима печени контрастирована
— Является чувствительным, но не специфичным методом для определения наличия метастазов и их числа (особенно при нейроэндокринных метастазах в печени)
5. Рекомендации по визуализации:
• Наиболее подходящий метод визуализации:
о КТ с контрастированием для стадирования опухоли
о Интраоперационное УЗИ при небольших образованиях
о ПЭТ/КТ информативно при скрининге всего тела
о МРТ с контрастированием гадоксетовой кислотой для обнаружения мельчайших метастазов
о Трансабдоминальное ультразвуковое исследование:
— Для скрининга или динамического наблюдения за метастазами
— Легкодоступно и не дает лучевой нагрузки, но обладает низкой чувствительностью

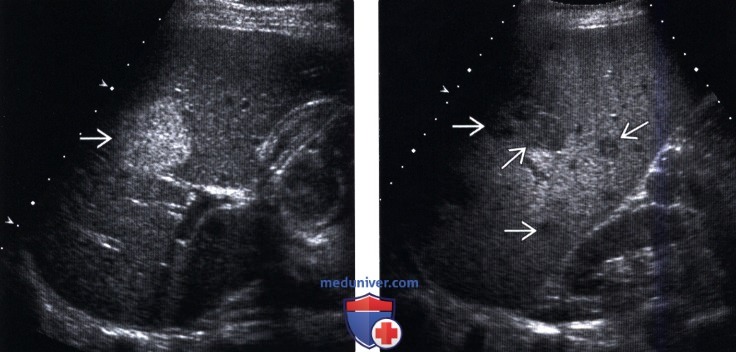
(Левый) Поперечный трансабдоминальный серошкальный УЗ срез у пациента с карциноидной опухолью. Визуализируется круглый, однородный, гиперэхогенный метастаз в правой доле печени.
(Правый) Продольный трансабдоминальный серошкальный УЗ срез у пациента с ра ком поджелудочной железы. Визуализируются множественные мелкие, гипоэхогенные метастазы на фоне стеатоза печени.
в) Дифференциальная диагностика метастазов в печени:
1. Кисты (дифференцировать от гипоэхогенных или кистозных метастазов):
• Могут содержать взвесь, возникшую в результате предшествующего кровоизлияния или инфицирования
• Не имеют ободка или центральной васкуляризации/не контрастируются
• Стенки не узловатые, не толстые, без внутренних перегородок
• Заднее акустическое усиление
2. Абсцессы (дифференцировать от гипоэхогенных метастазов):
• Могут быть солидными или кистозными (содержат взвесь/перегородки, толстые неровные стенки)
• Типичные системные проявления инфекции
• Симптом «кластера» на КТ при пиогенных абсцессах
3. Гемангиомы (дифференцировать от гиперэхогенных метастазов):
• Обычно равномерно гиперэхогенные при УЗИ
• Типично прерывающееся контрастирование периферических узлов при КТ или МРТ
• Выраженно гиперинтенсивные на Т2ВИ
4. Многоочаговый печеночноклеточный рак или холангиокарцинома (от очага по типу «мишени»):
• Печеночноклеточный рак: цирроз печени, вовлечение/тромбоз воротной вены:
о При циррозе печени метастазы из внепеченочных первичных опухолей редки из-за снижения портального кровотока:
— Таким образом, любое образование в цирротичной печени более подозрительно на печеночноклеточный рак, чем на метастазы
• Холангиокарцинома: втяжение капсулы, отсроченное контрастирование
5. Стеатоз (дифференцировать от гипо- или гиперэхогенных метастазов):
• Очаговое жировое вымывание: гипоэхогенная область на фоне гиперэхогенной паренхимы печени
• Очаговая жировая инфильтрация: гиперэхогенная область или области
• Четкие, «геометрические» границы, не искажают архитектонику и не сдавливают окружающие ткани
• При КТ без контрастирования имеют плотность жира
• Очаговое выпадение сигнала при противофазном GRET1 МРТ
6. Аденоматоз печени:
• Имитирует гиперваскулярные метастазы
• Жировое или геморрагическое содержимое; лучше всего визуализируются на МРТ
• Применение пероральных контрацептивов или анаболических стероидов в анамнезе
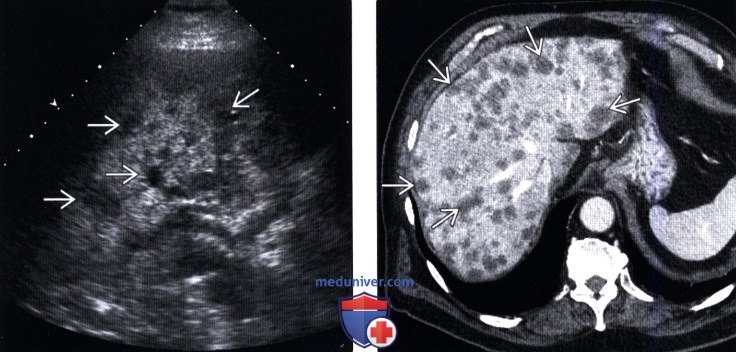
(Левый) Поперечный трансабдоминальный серошкальный УЗ срез у другого пациента с раком поджелудочной железы. Визуализируются множественные мелкие гипоэхогенные метастазы во всех сегментах печени. Обратите внимание, что эхогенность окружающей паренхимы печени повышена из-за жировой дистрофии, обычной находки после химиотерапии.
(Правый) КТ с контрастированием у этого же пациента с раком поджелудочной железы, портальная фаза, аксиальная проекция. Визуализируются множественные гиподенсивные метастатические узлы, разбросанные по всей печени.
г) Патология:
1. Общая характеристика:
• Этиология:
о Гиповаскулярные метастазы в печени
— Рак легких, ЖКТ, поджелудочной железы и большинство случаев рака молочной железы
— Лимфома, злокачественные новообразования желчного пузыря или мочевого пузыря
о Гиперваскулярные метастазы в печени:
— Нейроэндокринные опухоли, рак почки и щитовидной железы
— Некоторые типы рака молочной железы, саркомы и меланома
2. Стадирование, оценка и классификация метастазов в печени:
• Метастазы в печени указывают на IV стадию развития опухолевого процесса
д) Клинические особенности:
1. Проявления метастазов в печени:
• Наиболее распространенные признаки/симптомы:
о Бессимптомно, боли в правом верхнем квадранте живота, напряженная гепатомегалия
о Потеря веса, желтуха или асцит:
• Лабораторные данные: повышение уровней печеночных проб; в норме у 25-50% пациентов
2. Течение и прогноз:
• Зависит от расположения первичной опухоли
• 20-40% операбельных пациентов имеют хороший коэффициент пятилетней выживаемости
• У пациентов с метастазами рака толстой кишки:
о Коэффициент трехлетней выживаемости:
— 21 % у пациентов с единичными поражениями
— 6% у пациентов с множественными очагами в одной доли печени
— 4% у пациентов с распространенным поражением
3. Лечение метастазов в печени:
• Резекция или абляция при метастазировании рака толстой кишки
• Химио- или радиоэмболизация: гиперваскулярные (нейроэндокринные опухоли) метастазы
• Химиотерапия (пероральная или IV) во всех остальных случаях
е) Диагностическая памятка:
1. Следует учесть:
• Исключите другие причины образования множественных образований в печени, такие как кисты, абсцессы, гемангиомы
• Сверьтесь с историей болезни, изучите информацию о первичной опухоли
2. Советы по интерпретации изображений:
• При отсутствии других, хорошо определяемых метастазов:
о Образования в печени, которые «слишком малы, чтобы их охарактеризовать» редко представляют собой метастазы
о Образования, плотность которых при КТ без контрастирования выше плотности крови, редко представляют собой метастазы
ж) Список использованной литературы:
1. Westwood М et al: Contrast-enhanced ultrasound using SonoVue® (sulphur hexafluoride microbubbles) compared with contrast-enhanced computed tomography and contrast-enhanced magnetic resonance imaging for the characterisation of focal liver lesions and detection of liver metastases: a systematic review and cost-effectiveness analysis. Health Technol Assess. 17(16):1-243, 2013
2. Lefort T et al: Correlation and agreement between contrast-enhanced ultrasonography and perfusion computed tomography for assessment of liver metastases from endocrine tumors: normalization enhances correlation. Ultrasound Med Biol. 38(6):953-61, 2012
— Также рекомендуем «УЗИ печени при лимфоме»
Редактор: Искандер Милевски. Дата публикации: 2.11.2019
