После болезни вырабатывается иммунитет

О необходимости поддержки иммунитета сегодня не знает только ленивый. По весне он и вправду угасает — витаминов мало, вирусов — море. Тем временем, 1 марта в мире отмечают Международный день иммунитета.
Как его укреплять и нужно ли вообще это делать? Сажают ли иммунитет прививки? При каких обстоятельствах защитные силы организма значительно ослабляются? Помогают ли народные средства?
На эти и многие другие вопросы в интервью «МК» ответила детский аллерголог-иммунолог Екатерина КОРОТЕЕВА.
фото: pixabay.com
– Екатерина Николаевна, что такое иммунитет, как он работает и из чего состоит?
– Иммунитет человека – это способ защиты организма от чужеродных живых организмов и веществ, обеспечивающий наше выживание как вида в условиях постоянного агрессивного воздействия внешней и внутренней среды. Это научное определение, а если говорить популярно, то это – способность организма распознавать чужеродное и самозащищаться от всего чужого: вирусов и микробов, простейших организмов и микроскопических грибов, от образующихся в организме дефектных, стареющих и опухолевых клеток. Такую защиту обеспечивает иммунная система, которая состоит из центральных и периферических органов – они никогда не отдыхают, как и сердце. Ежесекундно иммунная система сдерживает атаки бактерий и вирусов, которых в одном кубическом сантиметре воздуха более миллиона! Органы иммунного надзора – это костный мозг, тимус, а также его помощники: селезенка, лимфоузлы, лимфоидная ткань слизистых оболочек и кожи. Главная клетка иммунной системы лимфоцит образуется, созревает и специализируется в этих органах. Каждая клетка человека имеет метку – «паспорт», определяющую ее принадлежность хозяину. Все, что не имеет такого паспорта, должно быть уничтожено иммунной системой. При возникновении необходимости защитить организм, например, при попадании инфекции, в первую очередь в «бой» вступают факторы врожденного (естественного) иммунитета. Это механические барьеры и физиологические факторы – неповрежденная кожа, слюна, слеза, мокрота и другие жидкие среды, которые способствуют выведению микробов. Для естественной иммунной защиты важна правильная работа сальных желез, наличие фермента лизоцима и нормального показателя pH мочи, желудочного сока и других сред организма. Главные клетки при врожденном иммунитете – макрофаги. Они обеспечивают очень важный процесс – фагоцитоз, предусматривающий поглощение всего чужого, его разрушение и выведение из организма. На качество врожденного иммунитета влияет способность клеток к выработке особого защитного противовирусного белка – интерферона.
Второй уровень иммунитета – специфический иммунитет. Это более сложный и тонкий процесс иммунной защиты. Его осуществляют В и Т-лимфоциты, обезвреживающие чужеродные частицы на расстоянии путем выработки молекул иммуноглобулина, которые носят название антител и могут сохраняться всю жизнь, делая человека устойчивым к некоторым инфекциям, например, к ветряной оспе, краснухе.
– Зависит ли иммунитет от возраста?
– Иммунитет, как и любая другая система, претерпевает возрастные изменения. Начиная формироваться еще до появления ребенка на свет, иммунная система достигает пика своего развития к 16 годам. В процессе становления иммунитет переживает пять критических периодов. После рождения ребенка первым критическим периодом являются первые 30 суток. В это время организм встречается с массивным воздействием различного рода раздражителей.
Второй критический период – 3-6 месяцев. В этот срок происходит резкое снижение уровня материнских иммуноглобулинов. Что приводит к риску развития респираторных инфекций у малыша. В этот срок проявляются первичные дефекты иммунной системы.
Третий критический период – 2-й год жизни. Система местного иммунитета еще незрелая, что проявляется повышенной чувствительностью к бактериальным и вирусным инфекциям.
Четвертый критический период – 4-6 годы жизни. Местный иммунитет окончательно не сформирован. Для этого периода характерна высокая частота аллергических, паразитарных заболеваний. В этот же период ребенок начинает активную социализацию: посещает детский сад, различные развивающие коллективные занятия и т.п. И даже если ребенок не относится к часто болеющим детям с нарушенным иммунитетом, за год, согласно статистике, он болеет ОРВИ более 7-8 раз.
– Дети часто болеют в саду, это известно. Что с этим делать?
– Если ребенок пошел в сад, он поначалу будет болеть респираторными инфекциями чаще «домашнего» ребенка – это данность. Любой детский коллектив – это источник вирусов и бактерий. Каждый ребенок является носителем своих, специфичных микробов, которые он получил у себя в семье и к которым у него выработался иммунитет. Период адаптации к детскому саду может длиться более 6-8 месяцев – это норма. Пока малыш не познакомится с полусотней наиболее распространенных вирусов, родителям придется запастись терпением. По статистике к 3 году только 10% детей, посещающих ДДУ, остаются в группе «часто болеющих». За несколько лет иммунитет ребенка наработает невосприимчивость к практически ко всем самым распространенным вирусам.
Методов 100-процентной защиты, конечно же, не существует, но, в любом случае, некоторые меры профилактики пойдут ребенку на пользу.
Несмотря на то что, давно известна польза закаливания как метода укрепления иммунитета, я не рекомендую использовать этот метод в классическом варианте у дошкольников. Существует риск навредить ребенку больше, чем помочь. Гораздо более эффективны, по моему опыту, методы щадящего закаливания: слегка теплый душ в теплое время года в утренние часы; одевать ребенка по погоде, чтоб он не перегревался на прогулке и в помещении; поддерживать температуру в комнате, где живет ребенок не более 22-23 градусов; регулярно ее проветривать.
Другой метод профилактики – приучение ребенка к правилам личной гигиены. Многие вирусы и бактерии весьма устойчивы во внешней среде: оседают на дверных ручках, перилах, игрушках. Рекомендую мыть руки часто – более 10 раз в день, после посещения сада умыть лицо, промыть нос солевым раствором, посморкаться.
Если ваш ребенок часто болел и до посещения садика, то есть смысл сделать ему прививку от гриппа, гемофильной и пневмококковой инфекций. Эти вакцины уберегут ребенка не только от тяжелой инфекции, но и от осложнений во время длительного течения ОРВИ.
– А как насчет народных способов укрепления иммунитета?
– «Бабушкины» методы для укрепления иммунитета – это то, что относится к ритуалам, привычкам формирования здорового образа жизни. Я за регулярное сбалансированное питание с возможным включением в рацион травяных чаев (ромашка, чабрец, зверобой), отвара шиповника, клюквенного, облепихового морса. Я против применения у детей прополиса и меда, икры черной и красной – как метода иммуностимуляции, в силу высоко аллергенных свойств этих компонентов пищи. Ограниченно применяется у детей экстракт эхинацеи ввиду ее способности стимулировать аллергический иммунный ответ. Я поддерживаю народные способы закаливания с помощью употребления мороженого, рассасывания кубиков льда замороженного сока или отвара трав.
Если ребенок все-таки заболел, не стремитесь вылечить его за 3 дня, помните, что кашель, насморк, лихорадка – защитные реакции организма. Вирусная инфекция в организме развивается по определенным законам и победить ее менее чем за 7 дней невозможно. Более того, при повышении температуры начинается более активная выработка белка интерферона, который помогает справиться с инфекцией.
Все чаще сталкиваются врачи с проблемой бесконтрольного самостоятельного назначения антибиотиков, что в конечном итоге ведет к развитию резистентности (нечувствительности) многих микробов к лекарствам, а также к дисбиозу, нарушению местного иммунитета и дисбалансу общей иммунной защиты.
Несмотря на особенности функционирования иммунной системы в детском возрасте, она в достаточной мере обеспечивает адекватность реакций на внешние и внутренние раздражители, не допускает развития угрожающих для жизни инфекционных и других заболеваний, вместе с нервной и эндокринной системами обеспечивает гармоничное развитие организма.
– От чего зависит иммунитет взрослого человека?
– Сила и стойкость иммунитета напрямую зависит от образа жизни человека. Поэтому не нужно нагружать иммунитет дополнительными и ненужными задачами, такими как переохлаждение, переутомление, недосыпание, неполноценное питание, злоупотребление алкоголем, низкая физическая активность. Существенно экономит ресурсы иммунной системы своевременное лечение хронических заболеваний будь то гастрит или, к примеру, бронхит.
У людей с сильно выраженными аллергическими реакциями, мы их называем атопиками, иммунитет не сильнее, чем у не аллергиков. Более того – у пациента с хроническим аллергическим процессом иммунитет чаще снижен, больше страдает противовирусная защита. Однако за рубежом есть исследования, подтверждающие факт более низкой заболеваемости онкологией среди атопиков.
– После каких болезней вырабатывается пожизненный иммунитет?
– После ряда вирусных заболеваний, например, оспы, кори и желтой лихорадки. Эти заболевания относятся к генерализованным инфекциям. В то же время большинство взрослых людей по много раз болеют гриппом и ОРВИ. На самом деле к гриппу вырабатывается пожизненный иммунитет. Но он, к сожалению, типоспецифический, то есть зависит от типа вируса гриппа. А этих типов известно более 2000.
Если респираторно-вирусные инфекции случаются более 10 раз в году или реже, но с осложнениями, тогда это повод обратится к врачу иммунологу за помощью для выяснения причины и подбора лекарственного средства, улучшающего защитные функции организма.
Очень важно помнить, что пациентам с аллергией, туберкулезом, аутоиммунными заболеваниями (системная красная волчанка, ревматизм, аутоиммунный тиреоидит) самостоятельно, без консультации с доктором, использовать иммунотропные препараты нельзя! Необоснованное применение иммунотропной терапии, особенно в детской практике, чревато последствиями. Одно из самых неприятных – это стимуляция дебюта аллергического заболевания. Назначать иммуномодуляторы должен только врач аллерголог-иммунолог!
– По каким причинам иммунитет слабеет?
– Причин ослабления иммунитета у современного человека множество, и все эти факторы действуют негативно в комплексе. Ведь иммунная система работает в тесной связи с нервной и эндокринной системами. Не секрет, что иммунную защиту человека ослабляют острые и хронические инфекции; не контролируемые (нелеченые) хронические заболевания; несбалансированное питание (дефицит витаминов и белка приводит к нарушению синтеза иммуноглобулинов); бесконтрольное применение лекарств, антибиотиков; наличие вредных привычек (злоупотребление алкоголем, курение); стрессы, нарушение сна, недостаточная физическая активность, дефицит инсоляции.
– Подрывают ли иммунитет прививки?
– Я не могу четко и однозначно ответить на этот вопрос. Вопрос сложный, дискутабельный, малоизученный.
– Зависит ли иммунитет ребенка от иммунитета матери?
– Ранее считали, что иммунитет ребенка по большому счету никак не связан с иммунитетом матери (если она конечно не страдает иммунодефицитом). Однако исследованиями доказано, что во внешних секретах, омывающих поверхности слизистых оболочек пищеварительного, респираторного, мочеполового трактов, преобладающим иммуноглобулином является секреторный иммуноглобулин А (SIgA). Наиболее высокая концентрация SIgA содержится в молозиве. Секреторные антитела класса IgA – главный фактор местного иммунитета пищеварительного тракта против разнообразных энтеропатогенных бактерий, вирусов и токсинов. Секрет молочной железы женщин содержит также антитела к различным антигенам: энтеробактериям, стрепто- и стафилококкам, а также к энтеровирусам, ротавирусам, вирусу гриппа и другим микроорганизмам, то есть ребенок на грудном вскармливании получает от матери временную защиту (до 3-6 мес.) в виде иммуноглобулинов А, М, G. Антитела молока и молозива соединяются с муциновым слоем, покрывающим эпителий кишечника ребенка, и тем самым предохраняют его от чужеродных антигенов. От уровня барьерной функции слизистой желудочно-кишечного тракта в значительной мере зависит риск возникновения пищевых аллергических реакций.
От мамы ребенку передаются антитела ко всем инфекциям, которыми мама болела в своей жизни, но это происходит в течение беременности. И конечно наличие этих антител у ребенка не дает 100% гарантии отсутствия заражения. Однако эти антитела долго не живут, они исчезают течение первых 6-12 месяцев.
Последние десятилетия в нашей стране и за рубежом активно развивается онкоиммунология. Взаимодействие опухолевых и иммунных клеток — предмет пристального внимания иммунологов разных стран. Ищутся пути ранней диагностики рака путем внедрения методов, основанных на молекулярной диагностике. А также иммунные способы лечения рака – как научить иммунную систему распознавать онкологическую клетку-обманщицу и своевременно уничтожать?
– Есть ли пути решения проблемы антибиотикорезистентности?
– Эта проблема стоит во всем мире остро. Во многих странах, например, в Америке и Австралии резистентность к антибиотикам макролидового ряда достигает 60%, в нашей стране некоторые авторы называют цифру в 40%. Один из путей ее решения – создание не новых антибиотиков, а современных бактериофагов (вирусов для патогенных бактерий). На Западе проводятся исследования по изучению возможности создания новых лекарственных препаратов на основе бактериофагов. Например, профессор-микробиолог Винсент Фишетти (Vincent Fischetti) из Рокфеллеровского Университета в Нью-Йорке проводит работы по использованию ферментов бактериофагов, с помощью которых разрушаются клеточные стенки патогенных микроорганизмов.
Надо отметить, что за рубежом все лекарственные препараты, действующие на иммунную систему, строго рецептурные. К сожалению, «мода» на препараты, улучшающие иммунитет, существует только в нашей стране. И в этом смысле мы – лидеры по производству иммуномодуляторов и индукторов интерферона.
В свете текущей ситуации с коронавирусом, который, по сути, вызывает пневмонию, вопрос статьи особенно актуален. Абсолютно всех интересует вопрос, реально ли заболеть пневмонией человеку, который уже ею переболел.
Чтобы ответить на такой вопрос, нужно разобраться с тем, какие виды воспаления легких существуют.

Виды пневмонии
Существует несколько видов воспаления легких. Каждая подобная патология вызывается разными возбудителями.
Пневмококковая
Пневмококк циркулирует в нормальной флоре верхних дыхательных путей. Когда иммунитет нарушается, пневмококк присоединяется к бронхиальным стенкам, через альвеолы попадает в кровь и разносится по всему организму. Тем самым вызывается клиническая картина воспаления легких.
Если у вас диагностирована подобная пневмония, иммунитет после нее не будет стойким. В кровотоке останутся клетки из “иммунологической памяти”. Если в кровь попадет пневмококк, немедленно начнется соответствующая реакция.
Имейте в виду: типов такого возбудителя существует несколько, а подобный нестойкий иммунитет вырабатывается только к одному. Это означает, что если человек заразится пневмококковой пневмонией, но вызванной другим возбудителем, реакции, описанной выше, не произойдет.
Микоплазменная
Микоплазма, по сравнению с пневмококком, легче прилипает к стенке дыхательных путей. Кроме того она ведет активную деятельность как на клеточной мембране, так и внутри самой клетки. В результате происходит активация воспалительной реакции, поскольку такая клетка воспринимается организмом как инородная.
Помимо всего прочего, микоплазма способна поражать лимфоциты – основные клетки, которые борются с болезнью – и активировать их размножение. За счет этого инфекция быстро распространяется по всему организму.
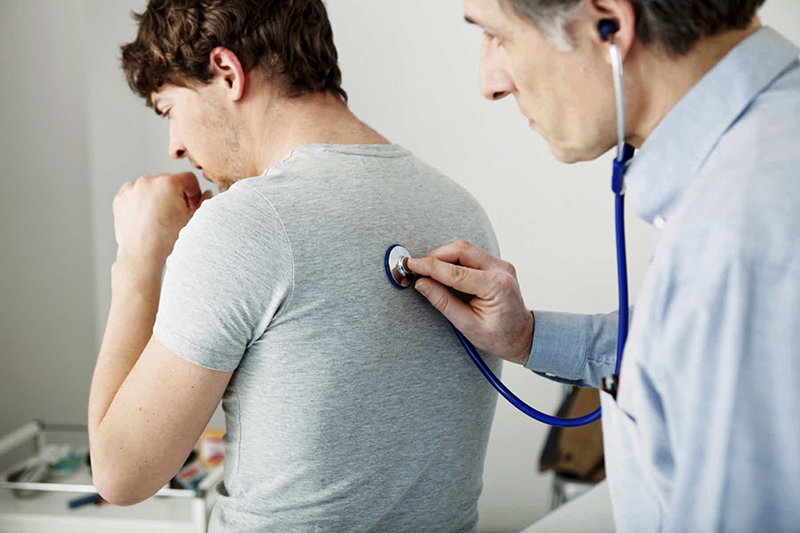
Вырабатывается ли иммунитет к пневмонии после болезни в случае микоплазменной пневмонии? Да, но кратковременный. Невозможно сказать, сколько по времени человек защищен, однако можно точно утверждать, что недолго.
Хламидийная
Хламидия живет в клетке до ее гибели, размножается в иммунных клетках альвеол и стенок сосудов. Если течение болезни тяжелое, хламидия распространяется по всему организму и вызывает при этом полное поражение иммунитета, который после перенесенной болезни не формируется.
Гриппозная
Если вирус гриппа попадает в альвеолярные мешки, развивается гриппозная пневмония. Вирус подавляет иммунитет, поэтому может развиться вторичная иммунная недостаточность.
После того, как человек переболеет гриппозной пневмонией, формируется очень прочный и длительный иммунитет, но только лишь в отношении конкретного штамма. Это означает примерно следующее: если вирус гриппозной пневмонии, которым заразится человек, будет отличаться хотя бы на один антиген от того вируса, которым он уже болел, то иммунного ответа не произойдет.

Парагриппозная
Патогенез схож с таковым при гриппозной пневмонии. Отличие заключается в том, что в данном случае вирус размножается в эпителиальных клетках.
Иммунитет от пневмонии после болезни вырабатывается, но кратковременный. Его формируют исключительно антитела, образованные во время болезни.
Поддержание иммунитета от пневмонии
Измените образ жизни, чтобы защитить себя от любого вида воспаления легких. Прекратите курить, а если это невозможно сделать, то сведите употребление табака к минимуму. Исключите употребление алкоголя. Чаще бывайте на свежем воздухе. Если вы живете в неблагополучном климате – подумайте о том, чтобы сменить регион проживания.
Не допускайте авитаминоза. Если речь идет об осенне-зимнем сезоне, когда очень сложно достать натуральные витамины, следует воспользоваться их аптечными аналогами в виде драже, таблеток, сиропов или жевательных пастилок (для детей).
Иммунитет после воспаления легких (Видео)
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 21 мая 2020;
проверки требуют 8 правок.
Иммуните́т (лат. immunitas — освобождение) человека и животных — способность организма поддерживать свою целостность и биологическую индивидуальность путём распознавания и удаления чужеродных веществ и клеток[1] (в том числе болезнетворных бактерий и вирусов). Характеризуется изменением функциональной активности преимущественно иммуноцитов с целью поддержания гомеостаза внутренней среды.
Назначение[править | править код]
Простейшие защитные механизмы, имеющие своей целью распознавание и обезвреживание патогенов, существуют даже у прокариот: например, ряд бактерий обладает ферментными системами, которые препятствуют заражению бактерии вирусом[2]. Одноклеточные эукариотные организмы применяют токсичные пептиды, чтобы предотвратить проникновение бактерий и вирусов в свои клетки[3].
По мере эволюции сложно организованных многоклеточных организмов у них формируется многоуровневая иммунная система, важнейшим звеном которой становятся специализированные клетки, противостоящие вторжению генетически чужеродных объектов[4].
У таких организмов иммунный ответ происходит при столкновении данного организма с самым различным чужеродным в антигенном отношении материалом, включая вирусы, бактерии и другие микроорганизмы, обладающие иммуногенными свойствами молекулы (прежде всего белки, а также полисахариды и даже некоторые простые вещества, если последние образуют комплексы с белками-носителями — гаптены[5]), трансплантаты или мутационно изменённые собственные клетки организма. Как отмечает В. Г. Галактионов, «иммунитет есть способ защиты организма от всех антигенно чужеродных веществ как экзогенной, так и эндогенной природы; биологический смысл подобной защиты — обеспечение генетической целостности особей вида в течение их индивидуальной жизни»[6]. Биологическим смыслом такой защиты является обеспечение генетической целостности особей вида на протяжении их индивидуальной жизни, так что иммунитет выступает как фактор стабильности онтогенеза[7].
Характерные признаки иммунной системы[8]:
- способность отличать «своё» от «чужого»;
- формирование памяти после первичного контакта с чужеродным антигенным материалом;
- клональная организация иммунокомпетентных клеток, при которой отдельный клеточный клон способен, как правило, реагировать лишь на одну из множества антигенных детерминант.
Классификации[править | править код]
Иммунная система исторически описывается состоящей из двух частей — системы гуморального иммунитета и системы клеточного иммунитета. В случае гуморального иммунитета защитные функции выполняют молекулы, находящиеся в плазме крови, а не клеточные элементы. В то время как в случае клеточного иммунитета защитная функция связана именно с клетками иммунной системы.
Иммунитет также классифицируют на врождённый и адаптивный.
Врождённый (неспецифический, наследственный[9]) иммунитет обусловлен способностью идентифицировать и обезвреживать разнообразные патогены по наиболее консервативным, общим для них признакам, дальности эволюционного родства, до первой встречи с ними. В 2011 году была вручена Нобелевская премия в области медицины и физиологии за изучение новых механизмов работы врождённого иммунитета (Ральф Стайнман, Жюль Хоффман и Брюс Бётлер)[10].
Осуществляется большей частью клетками миелоидного ряда, не имеет строгой специфичности к антигенам, не имеет клонального ответа, не обладает памятью о первичном контакте с чужеродным агентом.
Адаптивный (устар. приобретённый, специфический) иммунитет имеет способность распознавать и реагировать на индивидуальные антигены, характеризуется клональным ответом, в реакцию вовлекаются лимфоидные клетки, имеется иммунологическая память, возможна аутоагрессия.
Классифицируют на активный и пассивный.
- Приобретённый активный иммунитет возникает после перенесённого заболевания или после введения вакцины.
- Приобретённый пассивный иммунитет развивается при введении в организм готовых антител в виде сыворотки или передаче их новорождённому с молозивом матери или внутриутробным способом.
Другая классификация разделяет иммунитет на естественный и искусственный.
- Естественный иммунитет включает врождённый иммунитет и приобретённый активный (после перенесённого заболевания), а также пассивный иммунитет при передаче антител ребёнку от матери.
- Искусственный иммунитет включает приобретённый активный после прививки (введение вакцины) и приобретённый пассивный (введение сыворотки).
Органы иммунной системы[править | править код]
Выделяют центральные и периферические органы иммунной системы. К центральным органам относят красный костный мозг и тимус, а к периферическим — селезёнку, лимфатические узлы, а также местноассоциированную лимфоидную ткань: бронхассоциированную (БАЛТ), кожноассоциированную (КАЛТ), кишечноассоциированную (КиЛТ, пейеровы бляшки).
Красный костный мозг — центральный орган кроветворения и иммуногенеза. Содержит самоподдерживающуюся популяцию стволовых клеток. Красный костный мозг находится в ячейках губчатого вещества плоских костей и в эпифизах трубчатых костей. Здесь происходит дифференцировка В-лимфоцитов из предшественников. Содержит также Т-лимфоциты.
Тимус — центральный орган иммунной системы. В нём происходит дифференцировка Т-лимфоцитов из предшественников, поступающих из красного костного мозга.
Лимфатические узлы — периферические органы иммунной системы. Они располагаются по ходу лимфатических сосудов. В каждом узле выделяют корковое и мозговое вещество. В корковом веществе есть В-зависимые зоны и Т-зависимые зоны. В мозговом есть только Т-зависимые зоны.
Селезёнка — паренхиматозный зональный орган. Является самым крупным органом иммунной системы, кроме того, выполняет депонирующую функцию по отношению к крови. Селезёнка покрыта капсулой из плотной соединительной ткани, которая содержит гладкомышечные клетки, позволяющие ей при необходимости сокращаться. Паренхима представлена двумя функционально различными зонами: белой и красной пульпой. Белая пульпа составляет 20 %, представлена лимфоидной тканью. Здесь имеются В-зависимые и Т-зависимые зоны. И также здесь есть макрофаги. Красная пульпа составляет 80 %. Она выполняет следующие функции:
- Депонирование зрелых форменных элементов крови.
- Контроль состояния и разрушения старых и повреждённых эритроцитов и тромбоцитов.
- Фагоцитоз инородных частиц.
- Обеспечение дозревания лимфоидных клеток и превращение моноцитов в макрофаги.
Иммунокомпетентные клетки[править | править код]
К иммунокомпетентным клеткам относят макрофаги и лимфоциты. Эти клетки совместно участвуют в инициации и развитии всех звеньев адаптивного иммунного ответа (система трёхклеточной кооперации).
Клетки, участвующие в иммунном ответе[править | править код]
T-Лимфоциты[править | править код]
Субпопуляция лимфоцитов, отвечающая главным образом за клеточный иммунный ответ. Включает в себя субпопуляции Т-хелперов (дополнительно разделяются на Th1, Th2, а также выделяют Treg, Th9, Th17, Th22,), цитотоксических Т-лимфоцитов,NKT. Включает в себя эффектор, регуляторы и долгоживущие клетки-памяти. Функции разнообразны: как регуляторы и администраторы иммунного ответа (Т-хелперы), так и киллеры (цитотоксические Т-лимфоциты).
B-Лимфоциты[править | править код]
Субпопуляция лимфоцитов, синтезирующая антитела и отвечающая за гуморальный иммунный ответ.
Натуральные киллеры[править | править код]
Натуральные киллеры (NK-клетки) — субпопуляция лимфоцитов, обладающая цитотоксичной активностью, то есть они способны: контактировать с клетками-мишенями, секретировать токсичные для них белки, убивать их или отправлять в апоптоз. Натуральные киллеры распознают клетки, поражённые вирусами и опухолевые клетки.
Нейтрофилы[править | править код]
Нейтрофилы — это неделящиеся и короткоживущие клетки. Они составляют 65-70 % от гранулоцитов. Нейтрофилы содержат огромное количество антибиотических белков, которые содержатся в различных гранулах. К этим белкам относятся лизоцим (мурамидаза), липопероксидаза и другие антибиотические белки. Нейтрофилы способны самостоятельно мигрировать к месту нахождения антигена, так как у них есть рецепторы хемотаксиса (двигательная реакция на химическое вещество). Нейтрофилы способны «прилипать» к эндотелию сосудов и далее мигрировать через стенку к месту нахождения антигенов. Далее проходит фагический цикл, и нейтрофилы постепенно заполняются продуктами обмена. Далее они погибают и превращаются в клетки гноя.
Эозинофилы[править | править код]
Эозинофилы составляют 2—5 % от гранулоцитов. Способны фагоцитировать микробы и уничтожать их. Но это не является их главной функцией. Главным объектом эозинофилов являются гельминты. Эозинофилы узнают гельминтов и экзоцитируют в зону контакта вещества — перфорины. Эти белки встраиваются в билипидный слой клеток гельминта. В них образуются поры, внутрь клеток устремляется вода, и гельминт погибает от осмотического шока.
Базофилы[править | править код]
Базофилы составляют 0,5-1 % от гранулоцитов. Существуют две формы базофилов: собственно базофилы, циркулирующие в крови, и тучные клетки, находящиеся в ткани. Тучные клетки располагаются в различных тканях, лёгких, слизистых и вдоль сосудов. Они способны вырабатывать вещества, стимулирующие анафилаксию (расширение сосудов, сокращение гладких мышц, сужение бронхов). При этом происходит взаимодействие с иммуноглобулином Е (IgE). Таким образом они участвуют в аллергических реакциях. В частности, в реакциях немедленного типа.
Моноциты[править | править код]
Моноциты превращаются в макрофаги при переходе из кровеносной системы в ткани, существуют несколько видов макрофагов в зависимости от типа ткани, в которой они находятся, в том числе:
- Некоторые антигенпредставляющие клетки, в первую очередь дендритные клетки, роль которых — поглощение микробов и «представление» их Т-лимфоцитам.
- Клетки Купфера — специализированные макрофаги печени, являющиеся частью ретикулоэндотелиальной системы.
- Альвеолярные макрофаги — специализированные макрофаги лёгких.
- Остеокласты — костные макрофаги, гигантские многоядерные клетки позвоночных животных, удаляющие костную ткань посредством растворения минеральной составляющей и разрушения коллагена.
- Микроглия — специализированный класс глиальных клеток центральной нервной системы, которые являются фагоцитами, уничтожающими инфекционные агенты и разрушающими нервные клетки.
- Кишечные макрофаги и т. д.
Функции их разнообразны и включают в себя фагоцитоз, взаимодействие с адаптивной иммунной системой и инициацию и поддержание иммунного ответа, поддержание и регулирование процесса воспаления, взаимодействие с нейтрофилами и привлечение их в очаг воспаления, выделение цитокинов, регуляция репарации, регуляция процессов свертывания крови и проницаемости капилляров в очаге воспаления, синтез компонентов системы комплемента.
Макрофаги, нейтрофилы, эозинофилы, базофилы и натуральные киллеры обеспечивают прохождение врождённого иммунного ответа, который является неспецифичным (в патологии неспецифичный ответ на альтерацию называют воспалением, воспаление является неспецифической фазой последующих специфических иммунных).
Иммунно привилегированные области[править | править код]
В некоторых частях организма млекопитающих и человека появление чужеродных антигенов не вызывает иммунного ответа. К таким областям относятся мозг и глаза, семенники, эмбрион и плацента. Нарушение иммунных привилегий может становиться причиной аутоиммунных заболеваний.
Иммунные заболевания[править | править код]
Аутоиммунные заболевания[править | править код]
При нарушении иммунной толерантности или повреждении тканевых барьеров возможно развитие иммунных реакций на собственные клетки организма. Например, патологическая выработка антител к ацетилхолиновым рецепторам собственных мышечных клеток вызывает развитие миастении[11].
Иммунодефицит[править | править код]
См. также[править | править код]
- Иммунная система
- Врождённый иммунитет
- Приобретенный иммунитет
- Иммунотерапия рака
- Иммунитет растений
- Химера (биология)
Примечания[править | править код]
- ↑ ИММУНИТЕТ • Большая российская энциклопедия — электронная версия. bigenc.ru. Дата обращения 8 апреля 2020.
- ↑ Bickle T. A., Krüger D. H. Biology of DNA restriction // Microbiological Reviews. — 1993. — Vol. 57, no. 7. — P. 434—450. — PMID 8336674.
- ↑ Черешнев В.А. Черешнева М.В. Иммунологические механизмы локального воспаления. Медицинская иммунология 2011 т.13 №6 стр.557-568 РО РААКИ. cyberleninka.ru. Дата обращения 16 мая 2020.
- ↑ Travis J. On the Origin of the Immune System // Science. — 2009. — Vol. 324, no. 5927. — P. 580—582. — doi:10.1126/science.324_580. — PMID 19407173.
- ↑ Genetics of the Immune Response / Ed. by E. Möller and G. Möller. — New York: Plenum Press, 2013. — viii + 316 p. — (Nobel Foundation Symposia, vol. 55). — ISBN 978-1-4684-4469-8. — P. 262.
- ↑ Галактионов В.Г. Проблемы эволюционной иммунологии. cyberleninka.ru. Медицинская иммунология 2004 т.6 №3-5 РО РААКИ. Дата обращения 16 мая 2020.
- ↑ Галактионов, 2005, с. 8.
- ↑ Галактионов, 2005, с. 8, 12.
- ↑ Иммунитет // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2.
- ↑ Нобелевская премия по физиологии и медицине 2011 (англ.). www.nobelprize.org.
- ↑ Галактионов, 2005, с. 392.
Литература[править | править код]
- Галактионов В. Г. . Эволюционная иммунология. — М.: Академкнига, 2005. — 408 с. — ISBN 5-94628-103-8.
- Хаитов Р. М. . Иммунология. — М.: ГЕОТАР, 2006. — 320 с. — ISBN 978-5-9704-1288-6.
- Ярилин А. А. . Иммунология. — М.: ГЕОТАР, 2010. — 737 с. — ISBN 978-5-9704-1319-7.
