Распознавание антигена в клеточном иммунитете
Оглавление темы «Селезенка. Лимфатические узлы. Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Механизмы, контролирующие иммунную систему.»:
1. Селезенка. Функции селезенки. Лимфатические узлы. Функции лимфатических узлов.
2. Мукозно-ассоциированная лимфоидная ткань. Лимфоидная ткань слизистых оболочек.
3. Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Ранний защитный воспалительный ответ.
4. Представление антигена. Распознавание антигена. Взаимодействие Т-хелперов ( Тh1 ) с антигенпредставляющими клетками.
5. Активация Т- и В-лимфоцитов в иммунном ответе. Активация лимфоцитов. Формы специфического иммунного ответа.
6. Клеточный иммунный ответ. Гуморальный иммунный ответ. Защитные функции иммуноглобулинов ( антител ).
7. Иммуноглобулин G ( IgG ). Иммуноглобулин М ( IgM ). Функции иммуноглобулинов G и М.
8. Иммуноглобулин A ( IgA ). иммуноглобулин Е ( IgE ). Функции иммуноглобулинов А и Е.
9. Формы специфического иммунного ответа. Иммунологическая память как вид имунного ответа.
10. Иммунологическая толерантность. Механизмы, контролирующие иммунную систему. Гормональный контроль имумнной системы.
11. Цитокиновый контроль имунной системы. Местное действие цитокинов. Механизм действия цитокинов на иммунитет.
Представление антигена. Распознавание антигена. Взаимодействие Т-хелперов ( Тh1 ) с антигенпредставляющими клетками.
В случае неэффективности раннего защитного ответа и факторов врожденного иммунитета в организме накапливаются микроорганизмы, содержащие чужеродные антигены. Контакт этих антигенов с клетками иммунной системы приводит к развитию специфического иммунного ответа, который начинается с этапа представления и распознавания антигена.
Растворимые антигены в нативной форме связываются антителами и антигенраспознающими иммуноглобулиновыми рецепторами В-клеток.
Т-лимфоциты своими антигенраспознающими Т-клеточными рецепторами связывают короткие пептидные фрагменты белковых антигенов в комплексах с собственными молекулами главного комплекса гистосовместимости I или II классов на мембранах антигенпредставляющих клеток.

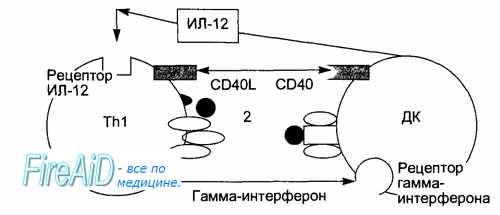
Рис. 8.8. Взаимодействие Т-хелперов (Тh1) с антигенпредставляющими дендритными клетками (ДК) опосредовано цитокинами (ИЛ-12, гамма-интерферон) и кости-мулирующими молекулами (CD40, CD40L).
В центре «иммунологического синапса» находятся: Т-клеточный антиген распознающий рецептор (1) и распознаваемый им комплекс антигенного пептида с молекулой главного комплекса гистосовместимости (2).
Молекулы главного комплекса гистосовместимости на поверхности лейкоцитов человека, получили название «человеческие лейкоцитарные антигены» (Human Leukocyte Antigens — HLA). Молекулы главного комплекса гистосовместимости I класса присутствуют на поверхности всех типов клеток, кроме эритроцитов и клеток трофобласта. Молекулы главного комплекса гистосовместимости II класса находятся на поверхности антигенпредставляющих клеток: дендритных клеток, макрофагов, В-лимфоцитов.
Антигенпредставляющие клетки играют важную роль на начальном (пусковом) этапе специфического иммунного ответа:
1) макрофаги, как правило, представляют антигены бактериального происхождения — продукты захвата и внутриклеточной переработки ими бактерий,
2) В-лимфоциты представляют микробные антигены, антигены токсинов, связанные их поверхностными иммуноглобулиновыми рецепторами,
3) наиболее универсальными антигенпредставляющими клетками являются дендритные клетки, которые необходимы для запуска первичного иммунного ответа, представляют многие, в том числе опухолевые, антигены.
После захвата чужеродного белка — антигена этими клетками и его разложения до коротких пептидов внутри клеток происходит комплексирова-ние отдельных молекул главного комплекса гистосовместимости с конкретными пептидами. Такие комплексы транспортируются на поверхность антигенпредставляющих клеток (рис. 8.8).
При встрече антигенпредставляющей клетки с Т-лимфоцитом, несущим на своей поверхности подходящий по структуре антигенраспознающий рецептор, замыкается лиганд-рецепторная связь, т. е. происходит распознавание антигена.
CD4+ T-лимфоциты способны распознавать антигенные пептиды в комплексах с собственными молекулами главного комплекса гистосовместимости II класса, a CD8+ Т-лимфоциты — в комплексах с собственными молекулами главного комплекса гистосовместимости I класса. Связывание антигена Т-клеточным рецептором служит сигналом усиления пролиферации данного Т-лимфоцита с последующей ускоренной дифференцировкой и активацией его клеток-потомков. В результате формируется клон Т-лим-фоцитов, способных при встрече с тем же антигеном быстро активироваться для участия в удалении патогенного агента.
— Также рекомендуем «Активация Т- и В-лимфоцитов в иммунном ответе. Активация лимфоцитов. Формы специфического иммунного ответа.»
Т-клетки это фактически приобретенный иммунитет, способный защитить от цитотоксического повреждающего воздействия на организм. Чужеродные клетки-агрессоры, попадая в организм вносят “хаос”, который внешне проявляется в симптомах заболеваний.
Клетки-агрессоры повреждают по ходу своей деятельности в организме все, что могут, действуя в своих интересах. А задача иммунной системы найти и уничтожить все чуждые элементы.
Специфическая защита организма от биологической агрессии (чужеродных молекул, клеток, токсинов, бактерий, вирусов, грибов и т.д.) осуществляется при помощи двух механизмов:
- продуцирования специфических антител в ответ на чужеродные антигены (потенциально опасных для организма веществ);
- выработки клеточных факторов приобретённого иммунитета (Т-клетки).
Как осуществляются иммунные реакции
При попадании в организм человека «клетки-агрессора», иммунная система распознаёт чужеродные и собственные измененные макромолекулы (антигены) и удаляет их из организма. Также при первичном контакте с новыми антигенами происходит их запоминание, что способствует их более быстрому удалению, в случае вторичного попадания в организм.
Процесс запоминания (презентация) происходит благодаря антиген-распознающим рецепторам клеток и работе антиген представляющих молекул (МНС молекул- комплексов гистосовместимости).
Что такое Т-клетки иммунной системы, и какие функции они выполняют
Функционирование иммунной системы обуславливается работой лимфоцитов. Это клетки иммунной системы, являющиеся
разновидностью лейкоцитов и способствующие формированию приобретённого иммунитета. Среди них выделяют:
- В-клетки (распознающие «агрессора» и вырабатывающие к нему антитела);
- Т-клетки (выполняющие функцию регулятора клеточного иммунитета);
- NК- клетки (разрушающие отмеченные антителами чужеродные структуры).
Однако, помимо регуляции иммунного ответа, Т-лимфоциты способны выполнять эффекторную функцию, разрушая опухолевые, мутировавшие и чужеродные клетки, участвовать в формировании иммунологической памяти, распознавать антигены и индуцировать иммунные реакции.
Справочно. Важной особенностью T-клеток является их способность реагировать только на презентированные антигены. На одном T-лимфоците находится только один рецептор к одному конкретному антигену. Это обеспечивает отсутствие реакции T-клеток на собственные аутоантигены организма.
Разнообразие функций Т-лимфоцитов обусловлено наличием в них субпопуляций, представленных Т-хелперами, Т-киллерами и Т-супрессорами.
Субпопуляция клеток, их стадия дифференцирования (развития), степень зрелости и т.д. определяется при помощи специальных кластеров дифференцировки, обозначаемых как СD. Наиболее значимыми являются СD3, СD4 и СD8:
- СD3 находится на всех зрелых T-лимфоцитах, он способствует передаче сигнала от рецептора к цитоплазме. Это важный маркер функционирования лимфоцитов.
- СD8 – это маркер цитотоксических T-клеток.
- СD4 является маркером T-хелперов и рецептором к ВИЧ (вирус иммунодефицита человека)
Т-хелперы
Около половины Т-лимфоцитов имеют антиген CD4, то есть являются Т-хелперами. Это помощники, стимулирующие процесс секреции антител В-лимфоцитами, стимулируют работу моноцитов, тучных клеток и предшественников Т-киллеров к «включению» в иммунную реакцию.
Справочно. Функция хелперов осуществляется за счёт синтеза цитокинов (информационных молекул, регулирующих взаимодействие между клетками).
В зависимости от продуцируемого цитокина, их разделяют на:
- T-хелперные клетки 1-го класса (продуцируют интерлейкин-2 и гамма-интерферон, обеспечивая гуморальный иммунный ответ на вирусы, бактерии, опухоли и трансплантанты).
- T-хелперные клетки 2-го класса (секретируют интерлейкины-4,-5,-10,-13 и отвечают за образование IgЕ, а также иммунного ответа, направленного на внеклеточные бактерии).
Т-хелперы 1-го и 2-го типа всегда взаимодействуют антагонистически, то есть повышенная активность первого типа угнетает функцию второго типа и наоборот.
Работа хелперов обеспечивает взаимодействие между всеми клетками иммунитета, определяя какой тип иммунного ответа будет преобладать (клеточный либо гуморальный).
Важно. Нарушение работы клеток-помощников, а именно недостаточность их функции, наблюдается у больных с приобретённым иммунодефицитом. Т-хелперы являются основной мишенью ВИЧ. В результате их гибели нарушается иммунная реакция организма на стимуляцию антигенов, что приводит к развитию тяжёлых инфекций, росту онкологических новообразований и летальному исходу.
Т-киллеры
Это так называемые T-эффекторы (цитотоксические клетки) или клетки убийцы. Такое название обусловлено их способностью уничтожать клетки-мишени. Осуществляя лизирование (ли́зис (от греч. λύσις — разделение) — растворение клеток и их систем) мишеней, переносящих чужеродный антиген или мутировавший аутоантиген (трансплантанты, опухолевые клетки), они обеспечивают реакции противоопухолевой защиты, трансплантационного и противовирусного иммунитета, а также аутоиммунные реакции.
Т-киллеры при помощи собственных МНС-молекул распознают чужеродный антиген. Связываясь с ним на поверхности клетки, они продуцируют перфорин (цитотоксический белок).
После лизирования клетки «агрессора» Т-киллеры остаются жизнеспособными и продолжают циркулировать в крови, разрушая чужеродные антигены.
Т-киллеры составляют до 25-ти процентов от всех Т-лимфоциотов.
Справочно. Помимо обеспечения реакций нормального иммунного ответа, Т-эффекторы могут участвовать в реакциях антителозависимой клеточной цитотоксичности, способствуя развитию гиперчувствительности второго типа (цитотоксической).
Это может проявляться лекарственными аллергиями и различными аутоиммунными заболеваниями (системные заболевания соединительной ткани, гемолитическая анемия аутоиммунного характера, злокачественная миастения, аутоиммунные тиреоидиты, и т.д.).
Подобным механизмом действия обладают некоторые лекарственные средства, способные запускать процессы некроза опухолевых клеток.
Важно. Препараты с цитотоксическим действием используют в химиотерапии онкологических заболеваний.
Например, к таким медикаментам относится Хлорбутин. Это средство применяют для лечения хронического лимфолейкоза, лимфогранулематоза и рака яичников.
Т-супрессоры и клетки памяти
Супрессоры подавляют функцию хелперов и В-лимфоцитарного звена. Однако современная классификация не выносит супрессоры в отдельную субпопуляцию. Поскольку доказано, что решающую роль в угнетении иммунной реакции играют апоптоз и специфические цитокины.
Помимо основных T-лимфоцитов, в организме человека существуют потомки клеток, контактировавших с антигеном и имеющих к нему рецепторы. Это клетки обеспечивающие иммунологическую память. Они способны в течение от десяти до 15 лет сохранять память об антигене, передавая её другим клеткам.
Справочно. Благодаря клеткам памяти обеспечивается быстрый иммунный ответ при повторном попадании «агрессора» в организм.
Нулевые лимфоциты
К ним относят лимфоциты, не имеющие T и B маркеров. Они составляют до 10% от всей популяции лимфоцитов. К ним относят NК-клетки (естественные киллеры) и K-клетки (киллерные).
Справочно. Основным отличием NK-клеток от T-киллеров является способность уничтожать не сенсибиллизированные клетки-мишени.
K-клетки отвечают за антителозависимую клеточную цитотоксичность. Они отражают взаимодействия гуморального и клеточного звеньев иммунитета, а также выступают в качестве «наводчиков» эффекторных (выполняющих функцию – в данном случае уничтожение) клеток на мишень.
NК- клетки обеспечивают контроль за качеством клеток и участвуют в формировании противовирусного иммунитета, обеспечиваютзащиту от роста опухолей и размножения мутировавших (дефектных) клеток.
Диагностика клеточного иммунитета
Диагностика T- и B-лимфоцитарного звена позволяет оценить состояние клеточного иммунитета. Базовое исследование с определением процентного содержания Т-, В- и нулевых клеток проводится с целью выявления первичных или вторичных иммунодефицитов, а также при контроле иммуностимулирующего лечения.
Исследование основных популяций при помощи маркеров CD3, 8, 19, 16+5б, а также соотношение между хелперами и киллерами, позволяет комплексно оценить иммунный статус. Для исследования используют венозную кровь.
Диагностика проводится при выявлении и контроле течения:
- аутоиммунных заболеваний (увеличено содержание CD3, CD4 хелперов);
- лимфолейкозов (повышено количество Т-лимфоцитов CD3);
- злокачественных новообразований (увеличено количество NK);
- ВИЧ (CD3, CD8);
- хронических инфекций, аллергических реакций, бронхиальной астмы и т.д.
Справочно. В зависимости от результатов анализа пациенту может быть рекомендована консультация иммунолога, гематолога, аллерголога, онколога или инфекциониста. С дальнейшим лечением у профильного специалиста по основному заболеванию.
Автор статьи Зыбина А.М.
Благодаря наличию иммунной системы организм защищен от большинства болезнетворных организмов (вирусов, бактерий, грибков, простейших, гельминтов и т. д.) и токсических продуктов их жизнедеятельности. Таким образом, иммунитет направлен на защиту организма, поддержание его целостности и индивидуальности.
Иммунитет можно разделить на клеточный и гуморальный. Клеточный иммунитет обеспечивается лейкоцитами при прямом их контакте с патогеном (фагоцитоз, повреждение патогена и т. д.). Гуморальный иммунитет обеспечивают белковые факторы, вырабатываемые клетками. К ним относят антитела и систему комплемента.
Рис. 1. Виды иммунитета.
По функциям иммунитет делят на врожденный и приобретенный. Врожденный иммунитет включает особенности индивидуума или вида, которые обеспечивают защиту от патогенов. Для проникновения вирусов и бактерий в организм и в клетки, необходимо наличие специальных белков на мембране. Такие белки чаще всего видоспецифичны, поэтому большинство болезней, от которых страдают животные, человеку не страшны. Даже внутри одного вида, существуют индивидуальные отличия белков, которые могут сделать часть популяции невосприимчивой к заболеванию.
Приобретенный активный иммунитет возникает при контакте с патогеном и последующей выработке антител. Он может произойти естественным путем (болезнь) искусственным (вакцина). В любом случае остаются клетки памяти и повторный контакт с патогеном уже не будет вызывать болезнь. Также антитела можно получить пассивно: с молоком матери или в виде сыворотки. Они защищают организм до тех пор, пока циркулируют в крови. Клетки памяти при этом не сохраняются и при повторном контакте с патогеном возможно заражение.
Иммунитет обеспечивают белые кровяные тельца – лейкоциты. Все они образуются в красном костном мозге. Лейкоциты принято делить на гранулоциты и агранулоциты.
К гранулоцитам относят нейтрофилы, базофилы и эозинофилы. Все они содержат большое количество гранул в цитоплазме, в которых запасены вещества, необходимые для борьбы с патогенами. Название гранулоцитов связано с красителями, которыми окрашиваются гранулы (гематоксилин – основный, эозин — кислый). Кроме того, они способны к фагоцитозу небольших частиц.
Нейтрофилы (рис. 2 а, г) составляют 93-96% всех лейкоцитов крови. Они имеют сегментированное (3-5 сегмента) ядро и окрашиваются и гематоксилином, и эозином. Они способны как к фагоцитозу небольших частиц, так и к образованию активных форм кислорода. Нейтрофилы могут жить и бороться с патогенами даже в анаэробных условиях. Они локализуются в крови и очагах воспаления, участвуют в образовании гноя. Эффективны против грибка, бактерий и протистов.
Эозинофилы (рис. 2 б, д) имеют сегментированное ядро (2 сегмента) и окрашиваются эозином. Они обеспечивают противогельминтный иммунитет (выделяют токсичные вещества и активные формы кислорода из гранул рядом с паразитом). Также они эффективно защищают организм от простейших. Способны к рециркуляции, то есть возвращению в кровь из тканей.
Рис. 2. Фотографии (а-в) и схематичное строение (г-е) нейтрофила (а, г), эозинофила (б, д) и базофила (в, е).
Базофилы (рис. 2 в, е) составляют 0,5-1% лейкоцитов крови. Они имеют S-образное ядро и их цитоплазма плотно набита гранулами, которые окрашиваются гематоксилином и содержат много гепарина и гистамина. Базофилы способны встраивать в мембрану IgE, благодаря этому специфически связываться и атаковать патоген. Все эти признаки характерны и для тучных клеток, из-за чего ранее базофилы считались их предшественниками. Однако, в настоящее время установлено, что тучные клетки имеют иное происхождение. Базофилы участвуют в реализации противогельминтного ответа. Они выделяют медиаторы воспаления и увеличивают проницаемость сосудов, что дополнительно привлекает другие иммунные клетки. Участвуют в аллергических реакциях немедленного типа.
Агранулоциты делятся на моноциты и лимфоциты.
Рис. 3. Фотография (а) и схематичное строение (б) моноцитов.
Моноциты (рис. 3) самые активные лейкоциты крови. Имеют клетку с крупным бобовидным ядром. Переходя в ткани, превращаются в макрофагов — профессиональных фагоцитов. Макрофаги способны поглощать даже очень крупные частицы. Мембрана этих клеток содержит Toll-подобные рецепторы, позволяющие распознавать и уничтожать консервативные структуры мембраны и клеточной стенки микроорганизмов. Если же макрофаги не способны поглотить чужеродную частицу, они облепляют ее со всех сторон и сливаются, изолируя частицу от организма. Макрофаги поглощают не только патогены, но и остатки мертвых клеток организма. Кроме того, они являются антиген-презентирующими клетками.
Лимфоциты имеют разнообразные функции. Выделяют T- и В-лимфоциты. Оба типа лимфоцитов образуются в красном костном мозге. Однако, их созревание проходит в разных местах: Т-лимфоцитов в тимусе, В-лимфоцитов – в красном костном мозге. Т-лимфоциты подразделяют на Т-киллеров, Т-хелперов. Также к лимфоцитам относят натуральных (естественных) киллеров. Как и все иммунные клетки, они образуются в красном костном мозге, однако, место их созревания до сих пор находится под вопросом. Созревание лимфоцитов проходит в детском возрасте, после чего все лимфоциты преимущественно локализуются в лимфатических узлах и в селезенке.
В-лимфоциты обеспечивают гуморальный приобретенный иммунитет и являются источником антител нашего организма. Антитела (иммуноглобулины, Ig) — белковые соединения плазмы крови (γ-глобулины), образующиеся в ответ на введение в организм человека бактерий, вирусов, белковых токсинов и других антигенов. Связываясь активными участками (центрами) с бактериями или вирусами, антитела препятствуют их размножению или нейтрализуют выделяемые ими токсические вещества. Кроме того, антитела являются своеобразной «меткой» для иммунных клеток о том, что частицу, к которой они присоединились, необходимо поглотить. При этом антитела распознают только чужеродные организму макромолекулы.
Антитела состоят из двух идентичных тяжёлых цепей (H-цепи) и из двух идентичных лёгких цепей (L-цепей) (рис. 4а). К тяжёлым цепям ковалентно присоединены олигосахариды. Каждая цепь имеет конститутивные (Fc) и вариабельные (Fab) фрагменты.
Конститутивный фрагмент консервативен и необходим для взаимодействия антитела с иммунными клетками. Базофилы и тучные клетки встраивают готовые антитела в мембрану и используют их как рецептор, что позволяет им быстро и бурно реагировать на патоген при его связывании мембранным антителом. В-лимфоциты встраивают в собственную мембрану антитела, той специфичности, которую производят сами. При связывании патогена с мембранным иммуноглобулином, становится возможна активация В-лимфоцита. При присоединении свободных (не встроенных в мембрану) антител к патогену, макрофаги и другие иммунные клетки могут провзаимодействовать с конститутивным фрагментом антитела. Это послужит сигналом к уничтожению помеченной молекулы или организма.
Вариабельный фрагмент антитела индивидуален для каждого В-лимфоцита. Именно этот участок (идиотоп) связывается с патогеном. Причем антитела разных В-лимфоцитов могут присоединяться к различным участкам одного и того же патогена, антитела одного В-лимфоцита связывают всегда один участок (эпитоп) (рис. 4 б). Благодаря вариабельности этих фрагментов, в организме одного человека может существовать до 108 вариантов антител.
Поскольку образование Fab фрагмента носит случайный характер у каждого В-лимфоцита, в период созревания в красном костном мозге они проходят селекцию. Как уже упоминалось ранее, эти клетки встраивают иммуноглобулины в мембрану и используют как рецептор. B-клетки, иммуноглобулиновые рецепторы которых способны взаимодействовать с собственными антигенами, либо погибают в результате апоптоза, либо приходят в состояние ареактивности (анергии). Таким образом, сохраняют активность только клетки, которые не реагируют на собственные антигены.
Рис. 4. Строение антитела (а) и его связывание с различными эпитопами антигена (б).
Тем не менее для активации зрелого В-лимфоцита одного контакта (связывание с рецептором) с патогеном недостаточно. Должна произойти презентация антигена.
Презентацию антигена осуществляют специальные антиген-презентирующие клетки (АПК), к которым относятся макрофаги и дендритные клетки (рис. 5), при этом В-лимфоцит должен получить сигнал к активации от Т-хелпера. Взаимодействие клеток происходит через ряд мембранных белков. Помимо иммуноглобулина, в нем участвуют главный комплекс гистосовместимости, Т-клеточный рецептор и ряд корецепторов.
Рис. 5. Взаимодействие между антиген-презентирующей (дендритной) клеткой и лимфоцитом.
Все клетки организма имеют на поверхности специальные гликопротеины – главный комплекс гистосовместимости (ГКГ, major histocompatibility complex, MHC, HLA). Этот гликопротеин существует в двух вариантах. ГКГ II имеют АПК и В-лимфоциты, ГКГ I – все остальные, в том числе и соматические, клетки. Этот комплекс индивидуален и насчитывает примерно 2000 аллельных генов. Внутри каждой клетки происходит постоянное обновление белков и других полимеров. Старые молекулы разрушаются и их фрагменты «выкладываются» на поверхность ГКГ. Иммунные клетки в процессе созревания «учатся» распознавать свой ГКГ и белки, которые на нем находятся. Таким образом, ГКГ являются «паспортом» клетки и показывают не только ее принадлежность данному организму, но и что происходит внутри клетки.
Т-лимфоциты обнаруживают патоген с помощью своих Т-клеточных рецепторов (ТКР, T—cell receptor, TCR). Это мембранный белок, ответственный за распознавание процессированных антигенов, связанных с молекулами главного комплекса гистосовместимости (рис. 6). Этот рецептор, как и антитела, имеет конститутивный и вариабельный участки. Конститутивным участком он связан с мембраной Т-лимфоцитов, вариабельный участок необходим для распознания ГКГ, антигена, и он индивидуален для каждого Т-лимфоцита.
Рис. 6. Взаимодействие Т-клеточного рецептора и главного комплекса гистосовместимости.
Для нормальной работы Т-лимфоцитов, при созревании в тимусе они проходят сложный двухэтапный отбор. На первом этапе выживают только те Т-лимфоциты, которые остаются способны связываться с ГКГ вариабельным участком ТКР (положительный отбор). На втором – уничтожаются Т-лимфоциты, которые активируются в ответ на собственные антигены, «выложенные» на ГКГ. Параллельно с этим, идет дифференцировка на Т-киллеры и Т-хелперы. Т-киллеры должны взаимодействовать с ГКГ I, в качестве корецептора такого взаимодействия выступает мембранный белок CD4, он и является маркером Т-киллеров. Т-хелперы должны связываться с ГКГ II, в качестве корецептора и маркера выступает белок CD8.
Если отбор Т- и В-лимфоцитов прошел недостаточно строго, и остались клетки, реагирующие на собственные антигены организма, то иммунитет может начать атаковать собственные клетки, что приведет к возникновению аутоиммунных заболеваний.
Презентация антигена В-лимфоцитам – это сложный процесс, в котором принимают участие Т-хелперы и АПК. В-лимфоцит, не взаимодействовавший со своим антигеном называется наивным. Если антиген взаимодействует с мембранным антителом В-лимфоцита, то происходит интернализация антитела с антигеном, антиген разрушается на фрагменты, и они выкладываются на ГКГ II. В это время, макрофаг или дендритная клетка также должны захватить антиген. Они его переваривают и выкладывают на ГКГ II. Т-хелпер должен провзаимодействовать с ГКГ II на поверхности АПК, после чего происходит его активация. Только после этого, Т-лимфоцит может провзаимодействовать с ГКГ II на поверхности В-лимфоцита, который активируется и превращается в плазматическую клетку. Плазматическая клетка пролиферирует и создает клонов, которые синтезируют антитела той же специфичности, что и исходный лимфоцит. Таким образом, происходит усиление иммунного ответа. Стоит отметить, что один патоген имеет много эпитопов, вследствие чего активируется множество В-лимфоцитов с различной специфичностью. Часть В-лимфоцитов, после контакта с патогеном, превращается в клетки памяти, которые сохраняются после болезни, и их активация происходит гораздо быстрее при повторном контакте с антигеном.
Рис. 7. Презентация антигена. Сверху: чужеродный антиген (1) захватывает и поглощает антиген-презентирующая клетка (2), которая его расщепляет и частично экспонирует на своей поверхности в комплексе с молекулами ГКГ II (3). Внизу весь чужеродный антиген связывается поверхностными антителами (5) В-лимфоцита (6), также поглощается и процессируется им (7), после чего часть чужеродной молекулы презентируются в комплексе с молекулами ГКГ II (8). После контакта (10) с Т-лимфоцитом (хелпером, 4), уже активированным антиген-презентирующей клеткой (2), В-лимфоцит начинает секретировать антитела в кровь (9).
Т-киллеры отвечают за клеточный иммунитет. Они играют важную роль в защите организма против вирусов и опухолей. Т-киллеры взаимодействуют с ГКГ I всех клеток и уничтожают клетку в случаях обнаружения чужого ГКГ или фрагмента чужого антигена на ГКГ. Таким образом, они уничтожают раковые клетки и внутриклеточных паразитов. Т-киллеры играют важную роль при трансплантации органов, ведь именно эти клетки атакуют чужеродные ткани пересаженного органа. Поэтому при трансплантации стараются подобрать донора органов, клетки которых имеют максимально похожий ГКГ на ГКГ пациента.
Т-киллеры взаимодействуют с клеткой через ГКГ, и, если он отсутствует, то клетка остается невидимой для этой системы. Поэтому, клетки без ГКГ уничтожаются натуральными киллерами. Таким образом, они обеспечивают противоопухолевую защиту.
Помимо лимфоцитов, в плазме крови присутствуют белки, способные распознавать клеточную стенку бактерий и самособираться в пору, вследствие чего нарушается ионный баланс клетки, и она погибает. Такие белки относятся к системе комплемента. Они синтезируются печенью и относятся к группе глобулинов.
Наличие на поверхности антигена антител или белков системы комплемента является сигналом для макрофагов к фагоцитозу чужеродной частицы.
Проявления иммунитета разнообразны и включает множество клеток и белков. Она обеспечивает эффективную защиту организма от различного рода заражений. Однако, приобретенный иммунитет – это эволюционно новая система, которая присутствует только у позвоночных. Именно поэтому нередки случаи некорректной работы иммунитета, что может привести к различным патологиям, например, аллергиям, опухолям и аутоиммунным заболеваниям.
