Секреторный иммунитет что такое

Иммуноглобулин А. Секреторный IgA в иммунитете слизистых оболочек.
Известно, что степень защиты от локальных вирусных инфекций респираторного и желудочно-кишечного трактов прежде всего зависит от содержания в организме специфического секреторного IgA, а не от наличия сывороточного IgG к энтеропатогенным или пневмотропным вирусам.
Стабильная структура, выраженный аффинитет к поверхности слизистых оболочек, преобладающее содержание в секрете молочной железы обусловливают биологическую роль секреторного IgA в защите организма от неблагоприятного воздействия различных патогенных агентов, в том числе вирусов.
IgA синтезируется в димерной форме в клетках lamina propria и после связывания с иммуноглобулиновым рецептором, синтезированным в эпителиальных клетках, транспортируется на поверхность слизистой оболочки. В момент выхода IgA в просвет кишечника рецептор частично расщепляется, в результате чего в составе IgA остается фрагмент рецептора, который называют секреторным компонентом.
Таким образом, секреторный IgA является продуктом кооперации двух типов клеток — плазматических и эпителиальных.
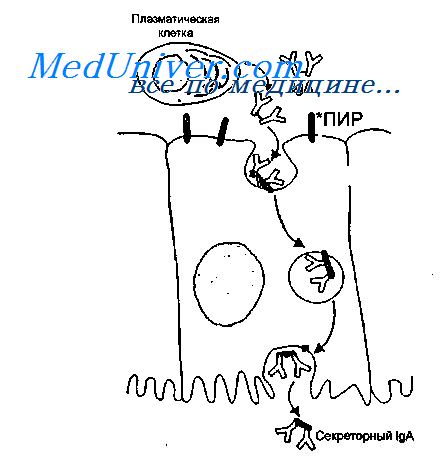
Секреторный IgA образуется не только в димерной, но и в тетрамерной форме, что усиливает его вируснейтрализующую способность. Секреторный компонент предохраняет IgA от расщепления протеолитическими ферментами, что обусловливает его значительные преимущества перед антителами других классов. Секреторный IgA нейтрализует вирус не только в просвете кишечника, но и при транспортировке его внутрь клетки. Димер IgA может нейтрализовать вирус в подслизистой оболочке кишечника, а затем, связавшись с рецептором, транспортировать его в просвет кишечника.
Димерные иммуноглобулины класса A (US IgA), соединенные посредством j-цепи в единую структуру с секреторным компонентом, представляют собой уникальный пример эволюционной адаптации иммуноглобулинов на слизистых покровах для эффективного функционирования в условиях постоянного воздействия антигенов различной природы.
Исходя из способности к локальному синтезу молекул секреторного компонента, а также димерной формы IgA-местно расположенными плазматическими клетками, ткани слизистых покровов можно разделить на три основных класса.
В слизистых оболочках индуктивная и продуктивная фазы гуморального иммунного ответа разобщены пространственно в большей степени, чем в других отделах иммунной системы.
Клеточные и гуморальные превращения, связанные с появлением IgA во внешних секретах, представлены на рисунке.
В молоко и, по-видимому, в другие внешние секреты молекулы IgA поступают из двух главных источников. Большая часть IgA, выделяемого со слюной, секретами слезной и молочной желез, а также пищеварительного и респираторного трактов, образуется плазматическими клетками. Однако IgA, обнаруживаемые в различных внешних секретах, могут иметь и системное происхождение. Продуцируясь клетками слизистых оболочек одних органов, они поступают в кровь и переносятся в слизистые покровы других органов.
Антиген после проникновения внутрь пейеровой бляшки активирует Т- и В-лимфоциты, которые по лимфатическому протоку поступают в мезентериальный лимфатический узел, а затем в кровь, селезенку, снова в кровь и селективно локализуются в лимфатических образованиях всех слизистых оболочек и экзокринных секреторных железах — молочных, слюнных и слезных. При этом Т-лимфоциты локализуются преимущественно между эпителиальными клетками слизистой оболочки, обеспечивая клеточный иммунный ответ, а В-лимфоциты — в lamina propria, где они дифференцируются в плазматические клетки и синтезируют IgA.
Около 90% плазматических клеток в lamina propria продуцируют IgA, в то время как в лимфатических узлах доля таких клеток составляет всего 2—5%.
Уникальна в этом отношении роль печени. Имеются убедительные данные, свидетельствующие о том, что гепатоциты избирательно связывают и в последующем транспортируют IgA в желчь, тем самым усиливая систему секреторного IgA кишечника.
Возможной функцией печени также является удаление комплексов антиген — IgA из циркулирующей крови с желчью в кишечник. Изучение противовирусного иммунитета убедительно продемонстрировало, что степень защиты респираторного и желудочно-кишечного трактов от локальных вирусных инфекций прямо коррелирует с уровнем специфических секреторных IgA, а не с уровнем антител сыворотки крови. В основе противовирусного действия секреторного IgA лежит инактивация вируса.
— Также рекомендуем «Кишечник и иммунитет. Роль кишечника в работе иммунной системы человека.»
Оглавление темы «Патогенез и механизмы противовирусной защиты организма.»:
1. Иммунная система слизистых оболочек. Слизистая оболочка и вирусная инфекция.
2. Строение иммунной системы слизистых. Концепция общей иммунной системы слизистых оболочек.
3. Иммуноглобулин А. Секреторный IgA в иммунитете слизистых оболочек.
4. Кишечник и иммунитет. Роль кишечника в работе иммунной системы человека.
5. Респираторные органы и вирусная инфекция. Роль дыхательной системы в противовирусном иммунитете.
6. Молочная железа и вирусная инфекция. Роль молочной железы в противовирусном иммунитете.
7. Особенности иммунитета при вирусных инфекциях. Патогенез противовирусного иммунного ответа.
8. Разрушение эффекторных клеток иммунитета и макрофагов вирусами. Устранение действия цитокинов вирусами.
9. Индукция иммунологической толерантности вирусами. Иммуносупрессия при вирусной инфекции.
10. Гуморальный противовирусный иммуннитет. Клеточный противовирусный иммунный ответ.
был выделен иммуноглобулин A (Ig), который присутствует на слизистых оболочках и выделяется плазматическими клетками, а не является продуктомсывороточной транссудации. Секреторный IgА отличается от сывороточного наличием не одного, а двух полипептидов. Было доказано, что IgА — наиболее важный иммуноглобулин внешних секретов. Общая иммунная система слизистых включает лимфоидную ткань кишечника, лимфоидную ткань бронхов, иммунокомпетентные клетки глотки, слюнных желез, респираторного тракта, молочной железы и гениталий.Особенностью иммунной системы слизистых является наличие больших количеств молекул секреторного IgА, причем выработку секреторных антител происходит не только в участках слизистых оболочек, где произошло антигенный влияние, но и на отдаленных секреторных поверхностях. Убедительно доказано, что степень защиты от локальных вирусных инфекций респираторного и желудочно-кишечного трактов прямо коррелирует с уровнем специфических секреторных IgA, а не с уровнем антител сыворотки крови. В основе противовирусного действия секреторного IgА лежит инактивация вируса.Много общих закономерностей иммунитета слизистых были обнаружены и детально изучены на примере кишечного иммунитета. Кишечник является важным иммунологическим органом, в собственной пластинке (lamina propria) которого содержится столько же лимфоидных клеток, сколько и в селезенке. Среди этих клеток идентифицированы Т-и В-клетки, малые лимфоциты и плазматические клетки. Последние синтезируют иммуноглобулины преимущественно класса А и являются источником антител, которые выделяются слизистой оболочкой кишечника. Популяция лимфоцитов в пейеровых бляшках состоит из предшественников В-(80%) и Т-клеток (20%). Лимфоциты эпителиального слоя кишечной стенки является исключительно Т-клетками, тогда как в подслизистом слое преобладают В-клетки, большинство из которых синтезируют IgA. Иммунитет против энтеротропних вирусов в основном осуществляется с помощью антител, которые секретируются в просвет кишечника. Антитела, защищающие слизистую оболочку кишечника, могут поступать из двух источников: из сыворотки крови и из плазматических клеток, расположенных в lamina propria.Секреторный компонент способствует устойчивости секреторных антител класса IgА к различным протеолитических ферментам и, возможно, помогает связывать иммуноглобулину со слизистой оболочкой. Выход секреторных антител класса А с поверхности слизистой оболочки ограничивается местом, где происходит антигенная стимуляция.Слизистые оболочки, выстилающие органы дыхания, также подвергаются воздействию чужеродных агентов. Защитные барьеры респираторного тракта — это слизистый респираторный эпителий, интерферон, лизоцим и лактоферин. Кроме того, в легких функционирует эффективная фагоцитарная система — альвеолярные макрофаги. Специфическая защита респираторного тракта обусловлена секреторным IgA. В подслизистом слое бронхов расположены скопления лимфоидной ткани — BALT (лимфоидная ткань бронхов — Bronchis associated lymphoid tissue), содержащая предшественники иммуноглобулин синтезирующих клеток. Аэрозольное и интраназальное введение различных агентов (в том числе вирусов), как правило, сопровождается локальной выработкой антител класса IgA.Высокое содержание секреторного IgА в молоке доказано при ряде инфекций. Изучение механизмов местного иммунитета выявило ряд фундаментальных закономерностей. Во-первых, иммунный статус слизистых определяется главным образом локальным содержанием специфических IgA. Во-вторых, иммунизация через слизистые покровы живыми вакцинами оказалась более эффективной по сравнению с парентеральной иммунизацией. Принципы создания местного иммунитета. Многие вирусы проникают через слизистые оболочки желудочно-кишечного и респираторного тракта. Необходимо максимальное стимулирование иммунного ответа у входных ворот инфекции. Оказалось, что уровень системных антител не является критерием для суждения
об эффективности имунизирующего агента, вводимого в организм через слизистые поверхности. На природу местного иммунитета влияет ряд факторов, из которых наиболее важными являются способ иммунизации, количество антигена в зоне аппликации, вирулентность вируса, а также способ доставки антител к слизистой поверхности.
3) 101. Ньюкаслская болезнь (НБ, псевдочума птиц) — высококонтагиозная вирусная инфекция главным образом куриных, характеризующаяся пневмонией, энцефалитом и поражением внутренних органов.Зарегистрирована на всех континентах. Наносит огромный экономический ущерб. Относится к особо опасным инфекциям. Разносится зараженной птицей, с инфицированными предметами, распространяется на большие расстояния (до 15 км) по воздуху. Характеристика возбудителя. Возбудитель ньюкаслской болезни — вирус семейства Paramyxoviridae. Вирион размером от 120 до 300 нм содержит односпиральную минус-РНК. Оболочка вирионов имеет выступы в форме нитей длиной 8 нм и содержит белки (гемагглютинин, нейраминидазу и фермент слияния). Внутренний компонент вириона — РНК с расположенными по спирали на ней капсомерами (белок S). Внутренняя поверхность оболочки представлена мембранным белком.В составе вируса обнаружены 3 основных и 5 минорных белковых компонентов. К основным относятся гемагглютинин, белок внутренней оболочки и белок S. Нейраминидаза — один из минорных компонентов. Белок F0 (слияния) играет основную роль в вирулентности вируса.Антигенная активность. Все формы НБ вызываются идентичными в антигенном отношении штаммами и протекают с образованием вируснейтрализующих, антигемагглютинирующих и комплементсвязывающих антител. Наивысший титр антител наблюдают через 3—4 нед, через 8—12 мес их не отмечают.Геммагглютинирующие и гемадсорбирующие свойства. Вирус ньюкаслской болезни обладает гемагтлютинирующими (с эритроцитами кур, морских свинок, мышей, человека), гемадсорбирующими и гемолитическими свойствами, а также высокой интерфероногенной активностью.Культивирование. Вирус НБ хорошо культивируется не только на восприимчивой птице, но и на куриных эмбрионах, изолированных ХАО, в культуре фибробластов КЭ, некоторых первичных и перевиваемых клетках. Репродукция вируса в культуре клеток сопровождается уплотнением цитоплазмы клеток, появлением в ней вакуолей; через 40 ч в цитоплазме некоторых клеток обнаруживают большое количество малых аморфных, эозинофильных включений.Патологоанатомические изменения. При остром течении болезни они характеризуются воспалением слизистых оболочек носа и ротовой полости, полосчатыми кровоизлияниями на слизистой оболочке пищевода. У 60—70 % взрослых кур отмечают точечные кровоизлияния в виде пояска на границе железистого и мышечного отделов желудка. В тонком кишечнике отмечают появление очагов некроза и эрозии, в толстом — везикулярные папулы. В селезенке, печени, лимфоузлах и тимусе обнаруживают атрофию и некроз. Головной и спинной мозг гиперемированы.Проникая в организм через слизистые оболочки, вирус попадает в кровеносные сосуды, в эндотелии которых размножается. Порозность стенок сосудов нарушается, и в них развиваются воспалительно-некротические процессы. Вирус, разнесенный с кровью по организму, вызывает расстройство гемодинамики с некрозодистрофическими изменениями.
Билет 21
Часто можно услышать о снижении местного иммунитета. Что это значит? Чем общий иммунитет отличается от местного? Как поддерживать иммунитет в активном состоянии?
Можно слышать такие понятия, как «общий иммунитет» и «местный иммунитет».
Общий иммунитет – это собственно иммунная система нашего организма.
Под местным иммунитетом следует понимать локальные защитные барьеры организма. Это, конечно же, кожа, слизистые оболочки, реснитчатый эпителий, волосики в носу, серная смазка в ушах, миндалины. Т.е. всё, что препятствует проникновению инфекции в организм. Кожа и слизистые оболочки на самом деле к собственно иммунной системе никакого отношения не имеют. Это лишь барьеры на пути проникновения микробов в организм. Понятие «местный иммунитет» – это обиходное понятие.
Можно привести такую аналогию.
Местный иммунитет – это забор и собачка, которая охраняет режимный объект.
Общий иммунитет – это автоматическая прицельная установка, которая расстреливает всех чужаков, проникших на территорию режимного объекта.
Общий иммунитет нельзя повысить. Поэтому всякие иммуностимуляторы, иммуномодуляторы, препараты для поднятия общего иммунитета и т.п. воздействовать на общий иммунитет не могут даже теоретически. Что касается специфического иммунитета против конкретных возбудителей, то тут их действие не доказано. Ведутся исследования, но на данный момент доказательств их эффективности не существует.
Еще раз: иммунитет нельзя повысить или укрепить! Но его можно натренировать/сформировать (чтобы он вел эффективную прицельную стрельбу по определенным чужакам). Как думаете, каким образом? Да, прививками – вакциной, которая содержит ослабленные либо мертвые микробы. Попадая в организм, иммунной системе не составит труда выработать против них антитела (они ведь не оказывают сопротивления или оказывают очень слабое). И эти антитела сохраняются в организме, а при последующем попадании в организм подобной инфекции у иммунной системы уже есть готовый ответ (автоматическая прицельная установка уже знает в лицо этого врага и может применить против него наиболее эффективный вид оружия).
Но общий иммунитет можно подавить. Это делается, например, при пересадке органов, чтобы иммунная система не повреждала пересаженный орган, т.к. все же он для организма чужеродный.
Сниженный общий иммунитет у больных СПИДом (ВИЧ поражает клетки иммунной системы), у хронических больных, например, диабетом.
Теперь о заборе и собачке (местном иммунитете).
Забор может сломаться в некоторых местах. Собачка может сильно ослабнуть, если ее плохо кормить. Т.е. любые повреждения кожи и слизистой (полости рта, дыхательной или пищеварительной системы) – это входные ворота для микробов.
Например, респираторные заболевания часто возникают именно из-за ухудшения слизистых оболочек дыхательных путей. Это может происходить вследствие низкой влажности воздуха, вдыхания едких паров, смазывания слизистых едкими веществами и т.п.
В жилом помещении следует поддерживать температуру 18-22 градуса и влажность 50-70%. В магазине можно приобрести увлажнитель воздуха. Либо опрыскивать водой из распылителя, ставить широкую посуду с водой, развешивать мокрую ткань. Переизбыток влаги также нехорошо, т.к. способствует распространению грибковой инфекции. Поэтому хорошо бы приобрести гигрометр (прибор для измерения влажности воздуха). Термометр и гигрометр должны быть в каждом доме, особенно если у вас маленький ребенок, за здоровьем которого нужно особенно тщательно следить.
Итак, от чего же зависит состояние местного иммунитета:
— чистое, проветренное жилое помещение с температурой 18-22 гр. и влажностью воздуха 50-70%;
— правильное сбалансированное питание;
— полноценный сон (7-8-9 часов в зависимости от потребностей, стараться ложиться и вставать в одно и то же время);
— физическая активность, закаливание, прогулки на свежем воздухе;
— своевременное лечение кожных заболеваний, заболеваний полости рта, глаз (глаза также могут быть входными воротами для инфекции);
— избегать стрессов, переутомления, оптимальный режим труда и отдыха.
Важный совет: При серьезных проблемах обращайтесь к врачу. Не занимайтесь самолечением! Это может быть очень опасно! Всегда обращайтесь к врачам специалистам.
Желаю всем здоровья и долголетия! 🙂
Понравилась статья? Подписывайтесь на канал, ставьте лайки, делитесь публикацией в социальных сетях (кнопки соц. сетей справа).
Приглашаю вас в сообщества: Facebook | Вконтакте | Одноклассники
Иммунитет — (лат. immunitas — освобождение) — защита организма от генетически чужеродных организмов и веществ, к которым относятся микроорганизмы, вирусы, черви, различные белки, клетки, в том числе и собственные изменённые клетки организма.
Иммунология — наука, изучающая иммунитет.
Иммунный ответ — это реакция организма на внедрение чужеродных агентов.
Антиген — любое чужеродное вещество или организм.
Антитело — вещество организма, распознающее антигены.
Антитела (иммуноглобулины) — особый класс гликопротеинов, присутствующих на поверхности B-лимфоцитов в виде рецепторов (рис. 1). Реагируя на присутствие антигена, они отделяются от мембраны В-лимфоцита и присутствуют в сыворотке крови и тканевой жидкости в виде растворимых молекул (антител). Антитела способны избирательно связываться с конкретными видами чужеродных молекул, которые в связи с этим называют антигенами.

Рис. 1. В-лимфоцит с мембрансвязанными рецепторами
Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов.
Антигены, как правило, являются белками или полисахаридами и представляют собой части бактериальных клеток, вирусов и других микроорганизмов.
К антигенам немикробного происхождения относятся белки пыльцы растений, яичный белок и белки трансплантатов тканей и органов, а также поверхностные белки клеток крови при переливании крови.
Аллергены — это антигены, вызывающие аллергические реакции.
История изучения иммунитета
Фундамент иммунологии был заложен изобретением микроскопа, благодаря чему удалось обнаружить первую группу микроорганизмов — болезнетворные бактерии.
В конце XVIII в. английский сельский врач Эдвард Дженнер сообщил о первой удачной попытке предотвратить заболевание посредством иммунизации. Его подход вырос из наблюдений за одним интересным явлением: доярки часто заражались коровьей оспой и впоследствии не болели натуральной оспой. Дженнер ввёл маленькому мальчику гной, взятый из пустулы (нарыва) коровьей оспы, и убедился в том, что мальчик оказался иммунным к натуральной оспе.
Работа Дженнера дала начало изучению теории микробного происхождения заболеваний в XIX в. Пастером во Франции и Кохом в Германии. Они отыскали антибактериальные факторы в крови животных, иммунизированных микробными клетками.
Луи Пастер успешно выращивал различные микробы в лабораторных условиях. Как часто бывает в науке, открытие было сделано случайно при культивировании возбудителей холеры кур. Во время работы одна из чашек с микробами была забыта на лабораторном столе. Было лето. Микробы в чашке несколько раз нагревались под солнечными лучами, высохли и потеряли способность вызывать заболевание. Однако куры, получившие эти неполноценные клетки, оказались защищёнными против свежей культуры холерных бактерий. Ослабленные бактерии не только не вызывали заболевание, а, напротив, давали иммунитет.
В 1881 г. Луи Пастер разработал принципы создания вакцин из ослабленных микроорганизмов с целью предупреждения развития инфекционных заболеваний.
В 1908 г. Илья Ильич Мечников и Пауль Эрлих были удостоены Нобелевской премии за работы по теории иммунитета.
И. И. Мечников создал клеточную (фагоцитарную) теорию иммунитета, согласно которой решающая роль в антибактериальном иммунитете принадлежит фагоцитозу.
Сначала И. И. Мечников как зоолог экспериментально изучал морских беспозвоночных фауны Чёрного моря в Одессе и обратил внимание на то, что определённые клетки (целомоциты) этих животных поглощают все инородные частицы (в т. ч. бактерии), проникающие во внутреннюю среду. Затем он увидел аналогию между этим явлением и поглощением белыми клетками крови позвоночных животных микробных телец. И. И. Мечников осознал, что это явление не питание данной единичной клетки, а защитный процесс в интересах целого организма. Учёный назвал действующие таким образом защитные клетки фагоцитами — «пожирающими клетками». И. И. Мечников первым рассматривал воспаление как защитное, а не разрушительное явление.
Против теории И. И. Мечникова в начале XX в. выступали большинство патологов, так как они считали лейкоциты (гной) болезнетворными клетками, а фагоциты — разносчиками инфекции по организму. Однако работы И. И. Мечникова поддержал Луи Пастер. Он пригласил И. И. Мечникова работать в свой институт в Париже.
Пауль Эрлих открыл антитела и создал гуморальную теорию иммунитета, установив, что антитела передаются ребёнку с грудным молоком, создавая пассивный иммунитет. Эрлих разработал метод изготовления дифтерийного антитоксина, благодаря чему были спасены миллионы детских жизней.
Теория иммунитета Эрлиха говорит о том, что на поверхности клеток есть специальные рецепторы, распознающие чужеродные вещества (антигенспецифические рецепторы). Сталкиваясь с чужеродными частицами (антигенами), эти рецепторы отсоединяются от клеток и в качестве свободных молекул выходят в кровь. В своей статье П. Эрлих назвал противомикробные вещества крови термином «антитело», так как бактерий в то время называли «микроскопические тельца».
П. Эрлих предполагал, что ещё до контакта с конкретным микробом в организме уже есть антитела в виде, который он назвал «боковыми цепями». Теперь известно, что он имел в виду рецепторы лимфоцитов для антигенов.
В 1908 г. Паулю Эрлиху вручили Нобелевскую премию за гуморальную теорию иммунитета.
Чуть раньше Карл Ландштейнер впервые доказал наличие иммунологических различий индивидуумов в пределах одного вида.
Питер Медавар доказал удивительную точность распознавания иммунными клетками чужеродных белков: они способны отличить чужеродную клетку всего по одному изменённому нуклеотиду.
Френк Бёрнет постулировал положение (аксиома Бёрнета), что центральным биологическим механизмом иммунитета является распознавание своего и чужого.
В 1960 г. Нобелевскую премию по физиологии и медицине получили Питер Медавар и Френк Бёрнет за открытие иммунологической толерантности (лат. tolerantia — терпение) — это распознавание и специфическая терпимость к некоторым антигенам.
Уничтожение генетически изменённых клеток
Одна из функций иммунной системы — это уничтожение генетически изменённых (мутантных) клеток организма. В процессе клеточного деления постоянно происходят ошибки, и одна из миллиона образовавшихся клеток становится мутантной, т. е. генетически чужеродной. В организме человека благодаря мутациям в каждый конкретный момент должно быть более 10 миллионов мутантных клеток. Мутации приводят к изменению функций клетки. Большинство мутантных клеток не способны выполнять свои функции, а многие выходят из-под контроля организма (например, при нарушении апоптоза) и становятся раковыми клетками. Появление таких клеток может привести к возникновению серьёзных заболеваний и гибели организма.
Один из механизмов иммунитета, осуществляемый лимфоцитами (НК-лимфоцитами), направлен на уничтожение именно раковых клеток.
Виды иммунитета
Иммунитет можно разделить на клеточный и гуморальный (рис. 2)
Рис. 2. Клеточный и гуморальный иммунитет
Все разнообразные формы иммунного ответа можно разделить на два типа: врождённый иммунитет и приобретённый иммунитет (рис. 3).
Рис. 3. Классификация иммунитета
Приобретённый иммунитет — это специфический индивидуальный иммунитет, т. е. это иммунитет, который имеется конкретно у определённых индивидуумов и к определённым возбудителям или агентам.
Главными характеристиками приобретённого иммунитета являются специфичность и иммунологическая память. Чем чаще организм встречается с патогеном, тем быстрее и активнее вырабатываются антитела, следовательно — сильнее защита.
Врождённый иммунитет с самого рождения (ещё до первой встречи с антигеном) защищает организм против всего чужеродного, т. е. он не специфичен.
Таким образом, повторная встреча с тем или иным патогенным микроорганизмом не приводит к изменениям врождённого иммунитета, но повышает уровень приобретённого.
Врождённый иммунитет активируется при первом появлении патогена быстрее, но распознаёт патоген с меньшей точностью. Он реагирует не на конкретные специфические антигены, а на определённые классы антигенов, характерные для патогенных организмов (белки вирусного капсида, продукты метаболизма глистов и т. п.).
Врождённый иммунитет может быть наследственным (видовым) и индивидуальным.
Наследственный (видовой) иммунитет — это невосприимчивость всех представителей данного вида к определённому антигену, приобретённая в процессе эволюции:
болезни, которыми болеет человек, но не болеют животные и птицы (корь, натуральная оспа, проказа, вирусный гепатит, холера, гонорея, дизентерия, брюшной тиф и др.);
болезни, которыми болеют животные, но не болеет человек (чума крупного рогатого скота, пироплазмоз собак);
болезни, которыми болеют птицы, но не болеет человек (куриная холера);
болезни, которыми болеют животные и человек, но не болеют птицы (сибирская язва, бешенство и др.).
Индивидуальный врождённый иммунитет определяется теми особенностями, которые передаются организму с родительскими генами и в процессе эмбрионального развития.
В процессе эмбрионального развития через плаценту плоду передаются антитела матери, которые противостоят инфекциям. Передача антител от мамы к ребёнку происходит в основном в последнем триместре беременности.
Иммунитет подразделяется на естественный и искусственный.
Естественный иммунитет возникает самостоятельно в процессе жизни организма.
Естественный иммунитет делится на активный (после перенесённых заболеваний) и пассивный (например, с молоком матери).
До 6 месяцев малыша защищают антитела, передающиеся от матери с грудным молоком. Поэтому важным является исключительно грудное вскармливание. Иммунитет матери защищает ребёнка. Дети, которые находятся на искусственном вскармливании, слабо защищены, т. к. собственных антител у них мало. Только к 6 месяцам организм самостоятельно начинает вырабатывать антитела. Собственный иммунитет ребёнка формируется только к концу первого года жизни.
Искусственный иммунитет организм приобретает в результате применения медицинских препаратов (вакцин и сывороток).
Вакцина — медицинский препарат, содержащий ослабленные или убитые микроорганизмы.
Вакцина вводится абсолютно (!) здоровому человеку для предотвращения заболевания в будущем.
Сыворотка — медицинский препарат плазмы крови без фибриногена, содержащий готовые антитела к определённому патогену (заражающему микроорганизму). Сыворотку получают из крови заражённого данным заболеванием животного (коровы, лошади и т. п.).
Сыворотка с чужими антителами вводится заболевшему человеку в случае, когда организм не способен произвести достаточное количество антител.
