Врожденный иммунитет к шоку
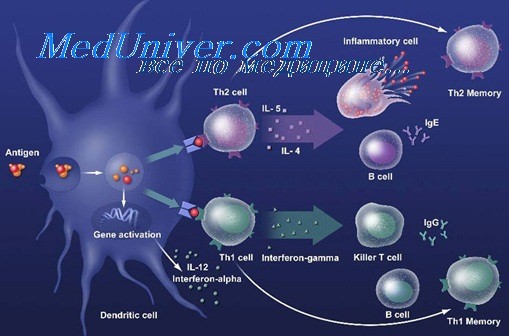
Белки теплового шока (HSPs). Эффекты врожденного иммунитета в ответ на HSPsБелки теплового шока (heat shok proteins HSPs) широко распространены в живой природе и являются одними из наиболее консервативных молекул биосферы. Основная функция HSPs — защита биологических систем от повреждающих стрессорных воздействий. В процессе эволюции эукариот некоторые HSPs приобрели функции, позволившие им интегрироваться в систему иммунитета. Белки теплового шока обеспечивают важные жизненные функции и представлены у всех живых организмов. Продукты генов, наименованные белками теплового шока или белками клеточного стресса, вырабатываемые в условиях гипертермии, изначально были идентифицированы как молекулы, вырабатываемые в ответ на присутствие в клетках белков с нарушенной конформацией. Затем было установлено, что HSPs играют роль шаперонов в нековалентной сборке и демонтаже других макромолекулярных структур, хотя сами не являются перманентными компонентами этих структур при выполнении своих биологических функций. Реакция белков теплового шока зафиксирована не только в условиях гипертермии, но также при оксидативном стрессе, ацидозе, ишемии, гипоксии-гипероксии, энергетическом истощении клеток и т п. В этих условиях HSPs высвобождаются из некротизированных клеток при разрушении ткани или лизисе инфицированных клеток. Благодаря особенности распознавания гидрофобных аминокислотных последовательностей на поверхности белков, как предупредительного сигнала о конформационной их нестабильности, HSPs способны осуществлять такие жизненно важные функции, как участие в обеспечении пространственной организации белковых молекул (фолдинге), их стабилизации, коррекции конформационных изменений (рефолдинге), транслокации белков через мембраны внутриклеточных органелл, предотвращении белковой агрегации и деградации нестабильных белков. Наряду с этим, HSPs проявляют антиапоптотическую активность. В совокупности, HSPs выполняют роль буферной системы, противодействующей стохастическим и потенциально дестабилизирующим факторам клеточного окружения. HSPs играют важную роль в индукции иммуного ответа, в особенности врожденного иммунитета: усиливают активность NK-клеток, созревание АПК и продукцию цитокинов. Пептидные фрагменты расщепляющихся белковых молекул перехватываются HSPs и, в конечном итоге, претерпевая процессинг в АПК, индуцируют реакции адаптивного иммунитета. Таким образом, через активацию АПК и участие в процессинге антигена белки теплового шока интегрируют реакции врожденного и приобретенного (адаптивного) иммунитета. Иммуностимулирующие свойства проявляют HSP про- и эукаритического происхождения. Способностью к индукции иммунного ответа обладают представители нескольких семейств HSP (кальретикулин, HSP10, HSP60, HSP70, HSP90, HSP100 и HSP170).
Шаперонная функция белков теплового шока осуществляется не только в процессе биогенеза других белков, но и при иммунном ответе на антигены. Изменение окружающей среды при инфицировании создает стрессорную ситуацию как для вторгшегося патогена, так и для клеток хозяина, что проявляется в обоюдной интенсификации синтеза и функциональной активности белков теплового шока. Молекулярные шапероны бактерий выступают в роли лигандов для рецепторов на поверхности клеток хозяина. HSPs могут быть распознаны TLR2, TLR4. Другие др96, HSP90 и HSP70, взаимодействуют с антигенпрезентирующими клетками через общий рецептор, CD91. HSP-шаперонные пептиды проникают в макрофаг/дендритные клетки через CD91, процессируются и презентируются вместе с молекулами МНС I и МНС II. Это вызывает активацию CD4 и CD8 Т-клеток. HSP-ДК взаимодействие через CD91 ведет к созреванию дендритных клеток и секреции ряда цитокинов. В результате взаимодействия рекомбинантного HSP 70 М tuberculosis с TLR-2 и TLR-4 in vitro запускается сигнальный каскад с вовлечением адапторных белков MyD88, TIRAP, TRIF и TRAM в эндотелиоцитах человека и в макрофагах мышей происходит активация фактора транскрипции NF-кВ. Представленный в эндоплазматическом ретикулуме эукариот, шаперон GRP94/gp96 через взаимодействие с TLR-2 и TLR-4 активирует дендритные клетки к инициации CD8′ Т-лимфоцитарного ответа. При этом усиливается экспрессия MICA/B молекул, взаимодействующих с NKG2D рецептором, представленным на поверхности CD8, но не СD4*Т-клеток. При взаимодействии TLR7 с HSP70, активно секретируемым, так и освобождаемым при некротической гибели клеток млекопитающих, усиливается фагоцитарная функция макрофагов. Данный эффект проявляется за несколько минут и выражается не только в стимуляции фагоцитоза, но также и функции представления антигена Т-клеткам через сигнальные пути, опосредуемые фосфоинозитид 3-киназой и р38 МАР-киназой. В осуществлении презентации антигена хелперным Т-клеткам принимают участие также зрелые В-лимфоциты, экспрессирующие TLR-2 и TLR-4. Они отвечают на LPS, пептидогликан, HSP60 повышением экспрессии МНС II и костимуляторных молекул. HSP 60 человека, но не GroEL E. coli или HSP65 М. tuberculosis индуцируют пролиферацию наивных В-клеток мышей и секрецию ими IL-6 и IL-10. На сегодняшний день многие рецепторы, распознающие паттерны известных PAMPs прокариотов, грибков, вирусов, простейших патогенов остаются еще не охарактеризованными. Существует взаимосвязь между фагоцитозом и экспрессией TLRs, поскольку активация сигналов через TLR усиливает фагоцитарные процессы, а фагоцитоз модулирует последовательность активации TLR. Является очевидным, что еще неопределенные молекулярные паттерны могут искажать или направлять адаптивный имунный ответ по Тh-2 типу Возможно, что отсутствие сигналов (например — PAMPs), подобно дефициту своих МНС I для NK-клеточной активации является стимулом для запуска иммунитета второго типа. Индукция сигналов через Toll-подобные рецепторы может обеспечивать не только защиту организма от различных инфекций. Нарушение функции проводимости данных сигналов приводит к развитию целого ряда патологических процессов в организме. Например, чрезмерная продукция провоспалительных цитокинов эндогенными лигандами может стать причиной развития хронического воспаления, аутоиммунных заболеваний, таких как болезнь Крона, диабет типа 1, атеросклероз. Изменение баланса в сторону провоспалительных цитокинов, вероятно, обусловлено развитием локальных отеков и воспалительных реакций в ЦНС инициированных провоспалительными цитокинами (TNF-a или IL-1p). В формировании длительно сохраняющихся неврологических нарушений принимают участие несколько цитокинов, которые потенцируя продукцию и действие друг друга, дольше сохраняются в циркуляции. Постоянное присутствие цитокинов поддерживает хронический воспалительный процесс в ЦНС, сопровождающийся демиелинизацией, а в ряде случаев и гибелью нейронов. — Также рекомендуем «Сигналы Toll-подобных рецепторов. Роль молекулы MyD88» Оглавление темы «Врожденный иммунитет»:
|
Иммунная система жизненно необходима для человека. Без её нормальной работы организм становится беззащитным перед опасными бактериями, вирусами, грибками и прочими вредными возбудителями. Иммунитет представлен обширной сетью клеток и тканей, которые постоянно ведут поиск патогенов, и, обнаружив врага, атакуют его. Активные элементы иммунной системы отличают наши собственные здоровые клетки и ткани от инородных по принципу «свой-чужой». Постараемся кратко рассказать о главных защитниках нашего организма.
Простуда и грипп
Лейкоциты
Белые кровяные клетки, называемые лейкоцитами, циркулируют в кровеносных и лимфатических сосудах и постоянно «патрулируют» организм, в поиске вредных возбудителей. Как только они обнаружены, количество лейкоцитов увеличивается, что означает начало борьбы с инородным телом. Кроме того, белые кровяные клетки посылают сигнал всем остальным органам и тканям подготовиться к отражению «атаки».
Наши белые кровяные клетки хранятся в разных местах, которые называются лимфоидными органами или органами иммунной системы:
- Вилочковая железа (Тимус) — железа, которая находится между легкими, где формируются Т-клетки иммунной системы.
- Селезёнка — орган, который фильтрует кровь. Находится в верхней левой части живота.
- Костный мозг — находится внутри костей. Также производит эритроциты.
- Лимфоузлы — небольшие железы, расположенные по всему телу, связанные между собой лимфатическими сосудами.
Существует два основных типа лейкоцитов, — фагоциты и лимфоциты:
Фагоциты
Они окружают, расщепляют и поглощают патогенные микроорганизмы. Есть несколько групп фагоцитов, в том числе:
- Нейтрофилы — наиболее распространенная группа фагоцитов, который, как правило, атакуют бактерии.
- Моноциты — это самый крупный и наиболее активный тип фагоцитов, который через несколько дней после циркуляции в крови проникает в ткани и трансформируется в макрофаги.
- Макрофаги — обнаруживают и пожирают патогенные микроорганизмы и отмирающие клетки.
- Тучные клетки — играют ключевую роль в борьбе с воспалением, аллергенами, травмами и др.
Лимфоциты
Лимфоциты позволяют организму запоминать патогены и распознавать их, если они снова возвращаются для атаки здоровых клеток. Это главные клетки, которые создают так называемые антитела и иммунный ответ организма на инфекции. Лимфоциты формируются в костном мозге, после чего часть из них остаётся там и превращается в В-лимфоциты (В-клетки). Вторая часть направляется в тимус, где трансформируется в Т-лимфоциты (Т-клетки).
Каждый из этих типов клеток выполняет свои задачи:
- В-лимфоциты — продуцируют антитела и сообщают Т-лимфоцитам о начале атаки.
- Т-лимфоциты — разрушают поврежденные клетки и передают сигнал опасности другим лейкоцитам.
Что такое иммунный ответ?
Кожная реакция на укус комара
Здоровый иммунитет отличает нормальные клетки от повреждённых или заброшенных в организм извне. Это происходит путём идентификации белков, которые находятся на поверхности всех клеток.
Антиген — это любое вещество, которое организм считает чужеродным и вызывает его иммунный ответ.
Часто это бактерии, грибки, вирусы, токсины или инородные тела. Но это могут быть и наши собственные клетки, которые работают неправильно или уже погибли в результате естественного процесса — апоптоза.
Роль В-лимфоцитов
Как только B-лимфоциты обнаруживают антиген, они начинают выделять антитела (антиген сокращенно «генератор антител»), — особые белки, которые связываются со специфическими антигенами.
Каждая В-клетка производит одно специфическое антитело. Например, одна создаёт антитело против бактерий, вызывающих пневмонию, а другая может распознать вирус гриппа.
Антитела являются частью большого семейства химических веществ, называемых иммуноглобулинами, которые играют важную роль в иммунном ответе:
- Иммуноглобулин G (IgG) — опознаёт и маркирует микробы, чтобы другие иммунные клетки могли их распознавать и начать борьбу с ними.
- IgM — класс антител, которые первыми свидетельствуют о начале инфекции.
- IgA — концентрируются в различных жидкостях организма, таких как слизистая оболочка носа, желудочный сок, слезы, слюна и защищают организм от проникновения патогенов, прежде всего вирусов и токсинов.
- IgE — отвечает за развитие аллергических реакций и участвуют в иммунном ответе на действие паразитов, таких как гельминты.
- IgD — помогают активировать B-лимфоциты и запуск иммунного ответа.
Антитела являются маркерами антигена, но они не убивают его, а лишь дают сигнал другим клеткам иммунной системы, таким как фагоциты, начать уничтожение патогена.
Роль Т-лимфоцитов
Существуют несколько типов Т-лимфоцитов:
T- хелперы — координаторы иммунного ответа. Часть из них передаёт сигналы опасности другим клетками, другие стимулируют В-клетки вырабатывать больше антител, третьи — привлекают к работе дополнительные Т-клетки и фагоциты.
Т- киллеры — уничтожают поражённые клетки организма, не позволяя патогену размножаться дальше. Они особенно полезны для борьбы с вирусами. Выделяя интерферон, T-киллеры ограничивают его проникновение в соседние клетки.
Сопротивляемость организма
Эхинацея пурпурная
Иммунная система каждого человека индивидуальна, но, как правило, она становится сильнее по мере взросления, так как к этому времени, каждый из нас уже подвергся воздействию большего количества патогенов и выработал иммунитет к ним. Именно поэтому подростки и взрослые болеют реже детей. Копия произведённого антитела сохраняется в организме, и если уже известный ему антиген появляется снова, он с ним быстро справляется. По этой причине, человек болеет такими заболеваниями как ветряная оспа только однажды. Это и называется иммунитет.
Существует три типа иммунитета:
- Врожденный
- Приобретённый
- Пассивный
Врожденный иммунитет
Все люди рождаются с определённым уровнем невосприимчивости к патогенам. Иммунная система атакует их с первого дня жизни. Врожденный иммунитет включает в себя внешние заградительные барьеры нашего тела, его первую линию защиты, — кожу и слизистую оболочку. Это называется общим или неспецифическим иммунным ответом. Если возбудителю удается проникнуть через эти барьеры, в дело вступает адаптивный или приобретенный иммунитет.
Приобретенный иммунитет
Этот тип защиты от болезнетворных микроорганизмов развивается по мере взросления. Перенесённые болезни или вакцинация создают архив антител к различным патогенам, — иммунологическую память.
Пассивный иммунитет
Тип иммунитета, «заимствованный» из другого источника, который не длится вечно. Например, младенец получает антитела от матери через плаценту до своего рождения и из грудного молока после появления на свет. Пассивный иммунитет защищает ребенка от некоторых инфекций в первые годы жизни.
Вакцинация
Прививка, — это ввод антигена или ослабленного патогена в организм человека при котором он не заболевает, но вырабатывает и сохраняет антитела.
Расстройства иммунитета
Поскольку иммунитет является очень сложной системой, возможны ситуации, которые не позволяют ей работать нормально. Существуют три типа иммунных расстройств:
Иммунодефициты
Возникают тогда, когда часть или несколько частей иммунной системы не функционирует. Иммунодефициты могут быть вызваны различными причинами, включая возраст, метаболические проблемы, недоедание, алкоголизм. Примером приобретенного иммунодефицита является ВИЧ/СПИД.
В ряде случаев иммунодефицит может передаваться по наследству, например, при хронической гранулематозной болезни, когда фагоциты не работают должным образом.
Аутоиммунные заболевания
При этих заболеваниях иммунная система ошибочно принимает здоровые клетки за чужеродные патогены или больные клетки и атакует их. К ним относятся целиакия, диабет первого типа, ревматоидный артрит, болезнь Грейвса и др.
Гиперчувствительность
При повышенной чувствительности наша иммунная система чрезмерно реагирует на попадание в организм какого-либо вещества, что приводит к повреждению здоровых органов или тканей. Примером гипречувствительности является анафилактический шок, — реакция организма на аллерген, которая может быть опасна для жизни.
Будьте здоровы!
Если этот материал был полезен для вас,- оцените его лайком и подписывайтесь на канал srokgodnosti. Спасибо!
Для получения дополнительной скидки 5% на сайте iHerb, при заказе воспользуйтесь этим промокодом, — BBI2773
О том, как иммунитет справляется с новым коронавирусом COVID-19, читайте здесь
#иммунитет #иммунная система #лейкоциты #лимфоциты #вирусы
prof_afv
Иммунитет к любому инфекционному заболеванию есть следствие глубоко эшелонированной обороны, состоящей из множество элементов. В норме они действуют координировано, работая на единую цель – отбить «атаку агрессора». Если не вдаваться в детали, то в «иммунной обороне» есть несколько блоков.
Первый блок это, так-называемый, врождённый иммунитет (innate immunity). Особенности врождённого иммунитета – распознавание агрессоров «по-крупному», не вдаваясь в детали, быстрое реагирование и отсутствие «памяти» — это означает, что врождённый иммунитет, встретившись с агрессором, не «запоминает» его и если происходит повторная встреча, реагирует точно таким же образом как и при первой встрече. Наши возможности избирательно влиять в нужном направлении на врождённый иммунитет очень ограничены, если они вообще есть.
Второй блок это, так называемый, адаптивный иммунитет (adaptive immunity). Эта линия обороны реагирует на агрессора медленнее, но зато она значительно лучше различает индивидуальность агрессоров и обладает «злопамятностью» — если агрессор попытается внедриться повторно, то «сдачи» он получит гораздо сильнее, чем при первом вторжении. По-научному, это называется иммунологической памятью . Ключевыми элементами индивидуального образа агрессора являются антигены. Именно антигены, а точнее их микроструктуры, находящиеся на поверхности, так-называемые, эпитопы, являются теми элементами, по которым адаптивная иммунная система отличает «своих» от «чужих». Когда агрессорами являются вирусы, то антигены это белки вирусов. В адаптивной иммунной системе есть две составные части. Первая, традиционно называется гуморальной («жидкостной»), в вторая – клеточной. Это исторически-укоренившиеся названия не совсем точны, поскольку первичными «игроками» и в гуморальном и в клеточном звене адаптивного иммунитета являются клетки, а «жидкостные факторы» играют роль не только в гуморальном, но и в клеточном звене иммунитета. Более точное название для гуморального иммунитета — «антительный или В-клеточный», так как ключевым «бойцом» здесь являются антитела (продукты В-клеток). А клеточный адаптивный иммунитет точнее называть «Т-клеточным», так как эффекторами этого звена являются Т-лимфоциты. В- и Т- клеточные звенья иммунитета работают не изолированно. Они взаимосвязаны. Но феномены, связанные с антительным иммунитетом, значительно проще исследовать и мы знаем о В-клеточном иммунитете значительно больше, чем о Т-клеточном. Большинство существующих вакцин работают, в основном или исключительно, стимулируя В-клеточный иммунитет. Единственный тип вакцин, который включает в иммунную защиту все типы иммунитета, это вакцины, состоящие из ослабленных (аттенуированных) возбудителей. Эти вакцины наиболее полно «имитируют» естественный инфекционный процесс. Но такие вакцины не полностью безопасны. Их пытаются заменить более безопасными «высокотехнологичными» вакцинами. Этот процесс идёт не очень быстро. Но это отдельная большая тема, в которую я сейчас углубляться не буду. Экскурс в иммунологию сделан для того, чтобы читатели-неспециалисты понимали, в самых общих чертах, что иммунная защита от инфекции, в частности, иммунная защита от SARS-CoV-2 не сводится только к антителам. Просто антительные иммунные ответы значительно легче изучать, чем Т-клеточные, а методы определения антител, в отличие от таковых для Т-клеточных иммунных ответов, относительно просты и легко коммерциализируются. Однако, без понимания роли каждого из этих двух звеньев адаптивного иммунитета попытки создание вакцины против SARS-CoV-2/COVID-19 это «блуждание в потемках». А ведь до сих пор не было ни одной научной публикации о Т-клеточном иммунитете при инфекции «новым коронавирусом»! Наконец она появилась.
В MedRxiv опубликован препринт статьи озаглавленной «Присутствие SARS-CoV-2-реактивных клеток у пациентов с COVID-19 и здоровых доноров» (оригинал здесь: https://doi.org/10.1101/2020.04.17.20061440). Не буду вдаваться в методические детали этой работы. Не специалисту с ходу в этом разобраться трудно. Остановлюсь на основных выводах:
1) Т-клетки, реагирующие на главный антиген SARS-CoV-2 (гликопротеин S), есть в крови 83% больных COVID-19. Частота обнаружения таких клеток коррелирует с тяжестью заболевания – у тяжелых больных COVID-19, таких клеток, как правило, было меньше или они отсутствовали (хотя размер выборки очень маленький). Существенной корреляции между антительным и Т-клеточным иммунными ответами у больных COVID-19 не обнаружено.
2) Т-клетки, реагирующие на гликопротеин S вируса SARS-CoV-2, обнаружены у здоровых людей, у которых нет никаких признаков инфицирования этим вирусом, ни в настоящем, ни в прошлом. Причём, реагирующие на вирус Т-клетки у больных COVID-19 и здоровых доноров «нацелены» на разные эпитопы гликопротеина S. Более того, эпитопы, с которыми реагируют Т-клетки от здоровых доноров, находятся в той части гликопротеина S, которая имеет наибольшее сходство с аналогичным белком «сезонных» коронавирусов.
Что это всё значит? Прежде всего, это только первая работа такого рода и количество исследованных случаев не слишком велико (больных исследовано – 18; здоровых доноров — 68). Работа выполнена в весьма авторитетной лаборатории, но независимо от авторитета, научные результаты должны пройти проверку на воспроизводимость. Если всё подтвердиться, то будут основания считать, что Т-клеточный иммунитет является важным, а возможно, и необходимым фактором для выздоровления. Остаётся открытым вопрос, насколько важен Т-клеточный иммунитет для поддержания пост-инфекционного иммунитета, если он конечно развивается (что пока не доказано). Методы, апробированные в данной работе, дают возможность этот вопрос изучить. Далее нужно разобраться, что означает неожиданно частая реактивность Т-клеток здоровых доноров с некоторыми эпитопами гликопротеина S. Действительно ли это связано с перекрёстной реакцией между «новым» и «старыми» сезонными коронавирусами? На уровне антительного ответа такой перекрёстной реактивности нет. Но может она есть на уровне Т-клеточных эпитопов. Если окажется, что это так, то можно будет, по крайней мере частично, объяснить индивидуальные различия в чувствительности к SARS-CoV-2, особенно, в зависимости от возраста. Ведь дети чаще взрослых болеют ОРВИ, вызванными обычными коронавирусами. Может в следствии этого они приобретают частичный иммунитет против SARS-CoV-2?
И в заключение «узелок на память» — при нынешнем состоянии знаний нет и не может быть научно-обоснованного «теста на иммунитет к коронавирусу» или «иммунного паспорта», подтверждающего невосприимчивость к коронавирусу. Всё разговоры об этом, по крайней мере, преждевремены.
