Роль крови в иммунитете
Состав крови
Кровеносная, она же сердечно-сосудистая система обеспечивает циркуляцию крови и лимфы в организме человека. Среди всех органов тела только поверхность глаз может получать кислород непосредственно из воздуха. Все остальные органы и ткани, даже кожа, получают кислород с током крови.
Кровь относится к соединительной ткани, клетки в ней занимают гораздо меньший объем, чем межклеточное вещество. Кровь состоит из жидкости с растворенными веществами (плазмы) и форменных элементов: лейкоцитов, эритроцитов и тромбоцитов. Плазма крови образует внутреннюю среду организма: жидкость из крови «выдавливается» в ткани и становится тканевой жидкостью, избыток тканевой жидкости попадает в лимфатические сосуды, становясь лимфой. Лимфа в итоге попадает в кровоток, возвращая жидкость в кровь.
Плазма крови содержит 0,9% хлорида натрия (поваренная соль), поэтому для внутривенных вливаний используют водный 0,9% раствор NaCl («физиологический», или изотонический раствор). Другие соли и органические вещества в сумме занимают около 9% массы плазмы. Большую роль играют белки плазмы, особенно альбумины.
Для поддержания постоянной кислотности в плазме присутствуют буферные системы. Водородный показатель крови человека (pH) в среднем равен 7,4. При его смещении в кислотную или основную сторону происходят химические реакции в буферных системах, которые уравновешивают изменения кислотности.
Поддерживать постоянство внутренней среды (гемостаз) необходимо для нормальной жизни клеток. Клеточная мембрана проницаема для молекул воды, поэтому если снаружи концентрация раствора повышается (гипертонический раствор), вода стремится выйти из клетки по закону осморегуляции. Клетка при этом скукоживается, становится неправильной формы, многие ее органеллы перестают правильно работать.
Если же концентрация соли в окружающем растворе слишком мала (гипотонический раствор), вода стремится внутри клетки, чтобы «разбавить» ее содержимое. В этом случае клетки разбухают, мембрана может не выдержать и лопнуть. Таким образом, изменение солености крови может привести к необратимым изменениям в организме.
Клетки составляют около 45% объема крови. Выделяют «белую» кровь – лейкоциты и «красную» кровь – эритроциты. Эритроциты имеют небольшой размер и двояковогнутую дисковидную форму. Такая форма дает большую площадь поверхности при минимальном объеме, что повышает эффективность газообмена. Эритроциты человека не имеют ядра, они теряют его в процессе созревания.
Эритроциты
В 1 мл крови содержится 4-6 млн эритроцитов. Их главная функция – перенос кислорода, за это отвечает крупный белок – гемоглобин. Одна молекула гемоглобина состоит из четырех полипептидных цепей (глобина) и железосодержащих групп (гема). Каждая молекула гемоглобина может перенести четыре молекулы кислорода, причем способность связывать и отдавать кислород зависит от условий среды: в более щелочной среде (легких) гемоглобин лучше связывает кислород, в то время как в более кислой среде (тканях), он лучше отдает его.
Механизм действия гемоглобина
Помимо кислорода с гемоглобином могут связываться другие газы, самым опасным из которых является угарный (СО). Он образуется при неполном сгорании органики в условиях нехватки кислорода и не имеет цвета и запаха. Сродство гемоглобина к угарному газу гораздо выше, чем к кислороду, поэтому, однажды связавшись с гемоглобином, угарный газ будет еще долго циркулировать в крови. При этом свободных сайтов связывания кислорода станет меньше и ткани начнут страдать от его нехватки. Тяжелое отравление угарным газом требует немедленной специализированной помощи.
Клетки крови
Лейкоциты
Лейкоциты являются основой клеточного иммунитета, это сферические клетки с достаточно крупным ядром. 1 мл крови содержит 4-11 тысяч лейкоцитов. Из всех клеток организма они наиболее уязвимы к действию радиации.
В зависимости от свойств лейкоциты делятся на несколько типов: содержащие гранулы, или гранулоциты (эозинофилы, нейтрофилы, базофилы) и не содержащие – агранулоциты.
Тромбоциты
Также кровь содержит тромбоциты, которые представляют собой отшнуровавшиеся куски гигантской клетки. Сами тромбоциты клетками не являются, они выглядят как мелкие пластинки неправильной формы и содержат только цитоплазму с гранулами. В гранулах находятся ферменты свертывающей системы, которые активируются при повреждении сосуда: образуется сгусток крови (тромб), который закупоривает поврежденный участок. 1 мл крови содержит 200-500 тысяч тромбоцитов.
Начало всем форменным элементам крови дают стволовые клетки красного костного мозга. Клетки крови постоянно обновляются, но у разных типов клеток обновление происходит с разной периодичностью. Эритроциты могут циркулировать 120-130 суток, в то время как лейкоциты и тромбоциты обычно живут не дольше 5-7 суток.
Иммунитет
Иммунная система защищает организм от воздействия бактерий, вирусов, грибов и паразитов, вредных веществ. В случае сбоя в работе иммунитета могут возникать аутоиммунные заболевания, в организме человека есть несколько механизмов, чтобы их предотвратить.
Органы, участвующие в формировании иммунитета
Основными органами иммунной системы являются селезенка, тимус (вилочковая железа) и костный мозг, где появляются и начинают созревать иммунные клетки. Клетки иммунитета циркулируют с кровью, располагаются в лимфоузлах и тканях, особенно много их в местах контакта с внешней средой (кожа, ЖКТ, дыхательные пути). Некоторые органы защищены от иммунного ответа барьерами, они называются иммунологически привилегированными органами. Это мозг, камеры глаза, семенники, плацента и плод и т.д. При травмах иммунологически привилегированных органов, когда нарушается целостность барьера, могут возникнуть аутоиммунные реакции.
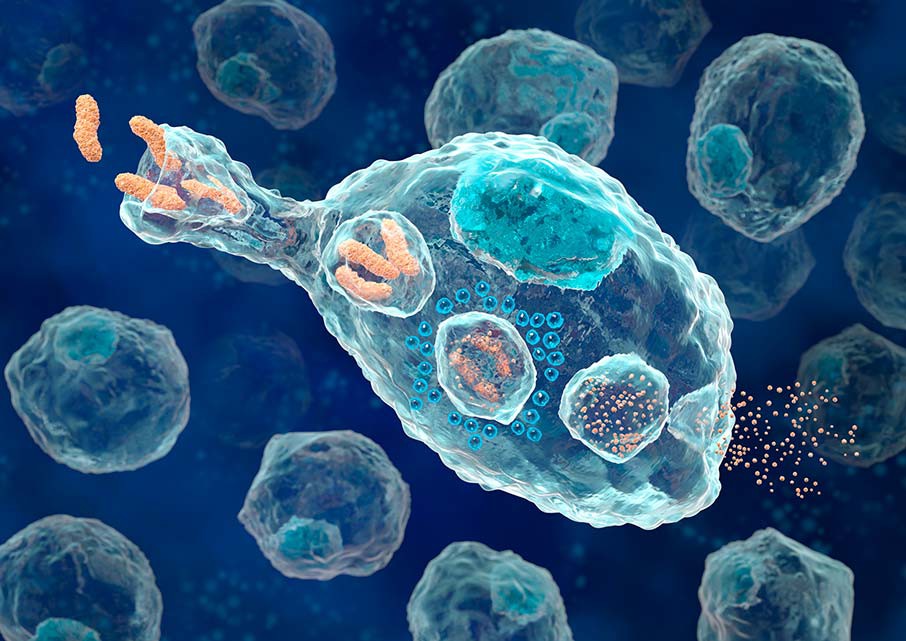
Макрофаги
Другие клетки неспецифического иммунитета, которые первыми отвечают на воздействие, – макрофаги. Это крупные клетки, которые способны к активному передвижению и фагоцитозу, они пожирают бактерии и инородные тела. Самостоятельно распознавать чужеродные белки макрофаги не способны, их действие не избирательно. «Ориентируют» макрофагов на уничтожение конкретных клеток антитела.
Макрофаг, фагоцитирующий бактерии.
Другими клетками иммунитета являются нейтрофилы и эозинофилы. Они, как и макрофаги, являются фагоцитами (то есть способны к фагоцитозу). Кроме того, в их цитоплазме есть гранулы с едкими веществами, которые высвобождаются при активации клетки. Запускается каскад химических реакций, в ходе которых образуются активные формы кислорода, это называется кислородным взрывом. Нейтрофилы и эозинофилы, а также окружающие здоровые клетки тоже погибают в результате кислородного взрыва, их остатки фагоцитируют макрофаги. Эозинофилы играют основную роль в развитии аллергий.
Нейтрофил, эозинофил, базофил
Фагоциты способны к направленному движению (хемотаксису), их можно обнаружить во многих тканях и органах, даже на поверхности кожи. Благодаря их постоянной активности большая часть атакующих агентов не вызывает инфекции, то есть системного ответа организма. Инфекция возникает в том случае, если иммунитет ослаблен (переутомление, переохлаждение, голодание и т.д.) или если инфекционный агент не был вовремя распознан фагоцитами.
Различают два вида иммунитета: клеточный и гуморальный. Гуморальный иммунитет – это система комплемента и циркулирующие с плазмой крупные молекулы – антитела. Белки системы комплемента «помечают» чужеродные агенты, вызывая направленное движение клеток иммунитета. Также система комплемента может формировать поры в мембране бактерий, что будет вести к их разрушению.
Антитела
Каждое антитело имеет на конце вариабельные домены (участки), комплементарные к чужеродному белку и специфические для конкретного возбудителя. Они прикрепляются к комплементарным участкам белков, «помечая» их для других клеток иммунного ответа, например, для фагоцитов. Также антитела могут слипаться между собой, что вызывает агглютинацию возбудителя. Особенно эффективны антитела против бактерий.
На рисунке изображены молекулы антител. Каждая состоит из двух пар цепей, синим цветом нарисованы тяжелые цепи, коричневым – легкие.
Клеточный иммунитет состоит из Т и В-лимофцитов. Т-лимофоциты могут быть двух видов: Т-хелперы и Т-киллеры. Т-киллеры клетки-убийцы, они запускают процессы апоптоза, то есть запрограммированной гибели клеток, их самоуничтожения. Это необходимо, если клетки организма заражены вирусами или бактериями или если при делении в геноме появились мутации (то есть Т-киллеры борются также с раковыми клетками).
В-лимфоциты синтезируют антитела и таким образом управляют гуморальным иммунитетом. При миграции В-клеток из крови в ткань они дифференцируются в плазматические клетки.
Лимфоциты действуют избирательно, они «настроены» на уничтожение возбудителя с конкретными антигенами. Чтобы правильно «настроить» лимфоциты, нужны антиген-презентирующие клетки (АПК). АПК фагоцитируют чужеродных агентов и выставляют на своей поверхности участки их молекул в комплексе с МНС II (главный комплекс гистосовместимости II). Т-хелперы способны распознавать чужие молекулы на поверхности АПК и активировать иммунный ответ.
Специфический иммунитет очень эффективен, но требует времени на развертывание. От попадания возбудителя в кровь до выработки антител может пройти несколько дней.
К неспецифическому иммунитету относят в основном фагоциты, которые пытаются поглотить или разрушить любое инородное тело или подозрительную клетку, которую встречают.
Немаловажную роль в иммунной защите организма играет воспаление. Это сложный стадийный процесс, который имеет следующие признаки: отек, местное повышение температуры, покраснение, боль и утрата функции органа. Благодаря отеку затрудняется распространение возбудителей по организму, место проникновения ограничивается. При повышении температуры повышается активность некоторых белков гуморального иммунитета, в то время как активность бактерий и скорость их размножения снижаются. Воспалительный процесс особенно эффективен против паразитов.
N-киллеры (натуральные киллеры), как и Т-киллеры могут запускать процессы клеточной гибели. Однако они, в отличии от Т-клеток, не требуют специальной подготовки – презентации антигена и активации. N-киллеры хорошо борются с опухолями.
Интерфероны – белки крови, которые составляют основу противовирусного гуморального иммунитета. Вирусы проникают в клетки организма, после чего здоровые клетки перестают синтезировать необходимые белки и начинают воспроизводить белки и генетическую информацию вирусов. Чтобы остановить распространение вирусных частиц и выиграть время на формирование специфического иммунитета, интерфероны замедляют или даже останавливают синтез белка в зараженных клетках.
Неспецифический иммунитет не требует времени на развертывание, его действие начинается уже в первые минуты после воздействия. Однако и точность неспецифического иммунитета низкая, при развитии иммунного ответа могут страдать здоровые клетки.
Синтез клеток специфического иммунитета (лимфоцитов) включает в себя элемент случайности, только так можно достигнуть неимоверного разнообразия иммунных клеток. Чтобы в кровоток не выходили клетки, которые способны атаковать собственный организм, они проходят строгий отбор в органах иммунной системы, где происходит созревание лимфоцитов (тимус, лимфоузлы). Если в результате отбора оказывается, что юный лимфоцит распознает клетки своего организма в качестве «врагов», в нем запускается процесс апоптоза, самоуничтожения.
Группы крови. Гемотрансфузия.
На поверхности эритроцитов могут находиться белки-агглютиногены А и В. В зависимости от того, какие агглютиногены есть в организме, выделяют: I группу крови (без агглютиногенов), II (только А), III (только В) и IV (оба агглютиногена).
При гемотрансфузии (переливании крови) необходимо учитывать группу, чтобы избежать возникновения иммунного конфликта. Если человеку с I группой крови перелить любую другую, клетки его иммунитета распознают чужеродные белки-агглютиногены и выработают антитела. В результате все чужие эритроциты «слипнутся» (агглютинируют), что может быть очень опасно для организма хозяина. Поэтому людям с I группой крови можно переливать только кровь такой же группы.
Если же перелить кому-нибудь эритроциты I группы крови, не имеющие белков-агглютиногенов, реакции иммунитета не последует. Можно сказать, что обладатели I группы самые «щедрые», потому что могут поделиться своей кровью со всеми. Также их называют универсальными донорами.
Обратная ситуация с IV группой: в крови таких людей нет антител ни к агглютиногену А, ни к агглютиногену В, поэтому им можно перелить кровь любой группы. Однако при попадании эритроцита группы IV в организм с другой группой произойдет агглютинация, поэтому обладателей IV группы крови можно назвать самыми «жадными» или универсальными реципиентами. Соответственно, II группу крови нельзя перелить обладателю III и наоборот.
Помимо агглютиногенов А и В существует много других белков, которые могут привести к возникновению иммунного конфликта. Международное общество трансфузиологов в настоящее время признает всего 36 систем деления крови на группы. Наиболее часто применяют систему АВО, в которой также учитывают резус-фактор. Впервые этот белок был описан у макак-резусов, за что и получил свое название.
Большая часть людей резус-положительна (Rh+), то есть имеет на эритроцитах белок-резус. Им можно переливать кровь с любым резусом. Людям же с резус-отрицательной кровью (Rh-) можно переливать только резус-отрицательную кровь.
Резус-фактор может стать причиной резус-конфликта между матерью и плодом. Если у резус-отрицательной матери будет резус-положительный ребенок, то при попадании крови плода в кровоток матери сформируются антитела к Rh+ белку. Чаще всего смешение крови происходит при родах и не несет опасности для ребенка. Если же антитела каким-то образом появились до родов, они могут проникнуть через плаценту и вызвать агглютинацию эритроцитов плода, что приведет к его гибели. Такая опасность часто возникает при повторной беременности резус-отрицательных женщин.
Распространенность групп крови варьирует в разных популяциях. На картинке приведена частота встречаемость разных групп по системе АВО в мире.
Распространенность групп крови
Как устроен иммунитет: Объясняем по пунктам
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
Кто отвечает за работу различных видов иммунитета?
- Костный мозг. Это центральный орган иммуногенеза. В костном мозге образуются все клетки, участвующие в иммунных реакциях.
- Тимус (вилочковая железа). В тимусе происходит дозревание некоторых иммунных клеток (Т-лимфоцитов) после того, как они образовались в костном мозге.
- Селезенка. В селезенке также дозревают иммунные клетки (B-лимфоциты), кроме того, в ней активно происходит процесс фагоцитоза — когда специальные клетки иммунной системы ловят и переваривают проникших в организм микробов, фрагменты собственных погибших клеток и так далее.
- Лимфатические узлы. По своему строению они напоминают губку, через которую постоянно фильтруется лимфа. В порах этой губки есть очень много иммунных клеток, которые также ловят и переваривают микробов, проникших в организм. Кроме того, в лимфатических узлах находятся клетки памяти — это специальные клетки иммунной системы, которые хранят информацию о микробах, уже проникавших в организм ранее.
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
- Т-лимфоциты. Названы так, потому что после образования в костном мозге дозревают в вилочковой железе — тимусе. Разные подвиды Т-лимфоцитов отвечают за разные функции. Например, Т-киллеры могут убивать зараженные вирусами клетки, чтобы остановить развитие инфекции, Т-хелперы помогают иммунной системе распознавать конкретные виды микробов, а Т-супрессоры регулируют силу и продолжительность иммунной реакции.
- B-лимфоциты. Название их происходит от Bursa fabricii (сумка Фабрициуса) — особого органа у птиц, в котором впервые обнаружили эти клетки. В-лимфоциты умеют синтезировать антитела (иммуноглобулины). Это специальные белки, которые «прилипают» к микробам и вызывают их гибель. Также антитела могут нейтрализовывать некоторые токсины.
- Натуральные киллеры. Эти клетки находят и убивают раковые клетки и клетки, пораженные вирусами.
- Нейтрофилы и макрофаги умеют ловить и переваривать микробов — осуществлять фагоцитоз. Кроме того, макрофаги выполняют важнейшую роль в процессе презентации антигена, когда макрофаг знакомит другие клетки иммунной системы с кусочками переваренного микроба, что позволяет организму лучше бороться с инфекцией.
- Эозинофилы защищают наш организм от паразитов — обеспечивают антигельминтный иммунитет.
- Базофилы — выполняют главным образом сигнальную функцию, выделяя большое количество сигнальных веществ (цитокинов) и привлекая этим другие иммунные клетки в очаг воспаления.
Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
